您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2020-05-18 09:35
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
「本文共:15条资讯,阅读时长约:3分钟 」
今日头条
利拉鲁肽心血管适应症获批。诺和诺德利拉鲁肽注射液(诺和力)获NMPA批准新适应症,用于降低伴有心血管疾病的2型糖尿病成人患者的主要心血管不良事件风险。2011年该药在中国已获批用于成人2型糖尿病患者控制血糖。在一项LEADER研究中,对于伴有心血管疾病的2型糖尿病患者,在标准治疗基础上,相比安慰剂,利拉鲁肽显著降低主要心血管不良事件发生风险达13%,显著降低全因死亡风险达15%,显著降低心血管死亡风险达22%。而且中国受试者的心血管安全性结果总体也与全部受试者的试验结果一致。
国内药讯
1.甘李药业门冬胰岛素注射液首仿获批上市。甘李药业三代胰岛素类似物门冬胰岛素注射液获国家药监局批准上市,用于治疗糖尿病。该药原研药由诺和诺德开发,最早于1999年在欧洲获批上市,2000年在美国获批上市,2002年获批进口中国,其2018年全球销售额达到29.7亿美元,中国市场销售额达2.3亿美元。甘李药业为首家拿到该品种仿制药上市资格的企业。
2.恒瑞钆布醇注射液首家申报上市。恒瑞新4类仿制药钆布醇注射液上市申请获CDE受理。钆布醇是一款核磁共振造影剂,原研产品由拜耳开发,于2009年9月在中国获批,2011年3月在美国获批。2019年,拜耳钆布醇全球销售额达4亿欧元。钆布醇属于第一批鼓励仿制药品目录建议清单中的产品,目前,钆布醇在国内尚无仿制药获批上市。恒瑞为国内首家提交该药上市申请的厂家。
3.Opdivo治疗经治非小细胞肺癌达到Ⅲb期临床终点。百时美施贵宝欧狄沃(Opdivo)治疗经治非小细胞肺癌的ⅢB期临床CheckMate 870获积极结果。该研究共入组400例亚裔患者(394例为中国患者),主要研究终点是评估Opdivo在晚期非HBV感染的经治患者中高级别(3-5级)不良反应的发生率。研究结果显示,欧狄沃在治疗人群中的安全性特征与既往基于体重剂量的关键性研究一致,未发现新的安全性风险。详细研究结果将于国际医学会议上公布。
4.徐诺药业艾贝司他中国注册研究进展。徐诺药业1类抗肿瘤新药艾贝司他(abexinostat) 单药治疗复发/难治性弥漫大B细胞淋巴瘤的中国注册关键性Ⅱ期临床首例患者给药。该研究由中国医学科学院肿瘤医院副院长、肿瘤内科主任石远凯教授担任主要研究者,预计在12个月或更早时间内完成患者招募。艾贝司他是一款具best-in-class潜力的新型HDAC抑制剂,目前已在美国、中国、欧洲等地同时开展临床试验,适应症涉及血液肿瘤、肾癌、肉瘤、甲状腺癌、乳腺癌、卵巢癌等。
5.葛兰素史克ICOS激动剂药物抗体在华获批两项临床。葛兰素史克(GSK)在研ICOS激动剂抗体GSK3359609注射液获国家药监局两项临床试验默示许可。拟开发单药用于治疗复发/难治性实体瘤类恶性肿瘤;以及联合默沙东PD-1抑制剂Keytruda用于治疗头颈癌。在一项既往未接受过PD-1/L1免疫检查点抑制剂的头颈部鳞状细胞患者接受GSK3359609与Keytruda的联合治疗的临床中,接受联合治疗组的可评估患者中的总缓解率为24%;所有应答患者缓解持续时间≥6个月;中位无进展生存期为5.6个月。在PD-L1表达患者中,大多应答者和疾病稳定患者的PD-L1评分<20。目前全球尚无同靶点药物获批上市。
国际药讯
1.PARP抑制剂获FDA批准治疗前列腺癌。Clovis Oncology公司PARP抑制剂Rubraca(rucaparib)片剂获FDA批准扩展适应症,用于治疗携带有害BRCA基因突变的转移性去势抵抗性前列腺癌(mCRPC)成人患者,这些患者已经接受了雄激素受体靶向疗法和紫杉烷类化疗。Rubraca也是FDA批准治疗前列腺癌的首款PARP抑制剂。在一项名为TRITON2的试验中,Rubraca对于携带BRCA突变的mCRPC患者达到44%的客观缓解率(ORR),而且无论患者携带的是种系还是体系BRCA基因突变,ORR都很相似。患者的缓解持续时间在数据截止时尚无法评估。
2.FDA批准首款4线治疗晚期GIST创新疗法。Deciphera Pharmaceuticals公司开发的蛋白激酶抑制剂Qinlock(ripretinib)片剂获FDA批准上市,用于4线治疗晚期胃肠道间质瘤(GIST)成年患者。Qinlock也是首款用于4线治疗GIST的创新疗法。在一项Ⅲ期临床INVICTUS中,与安慰剂相比,Qinlock显著延长患者的中位无进展生存期(6.3个月vs 1.0个月),将患者疾病进展或死亡风险降低85%。而且Qinlock组患者中位总生存期为15.1个月,显著优于对照组(6.6个月),将患者死亡风险降低64%。
3.BMS免疫调节剂Pomalyst获批治疗卡波西肉瘤。百时美施贵宝(BMS)开发的沙利度胺类似物Pomalyst(pomalidomide,泊马度胺)获FDA批准,用于治疗与艾滋病相关且对抗逆转录病毒疗法(HAART)耐药的卡波西肉瘤患者,以及HIV阴性的卡波西肉瘤患者。在一项Ⅰ/Ⅱ期临床(12-C-0047)中,Pomalyst的客观缓解率达71%(95% CI:51,87),其中14%(4/28)的患者达到完全缓解,57%的患者达到部分缓解;患者中位缓解持续时间为12.1个月,而且有50%的患者缓解持续时间超过12个月。Pomalyst此前已获FDA批准,与地塞米松联用,治疗经治多发性骨髓瘤患者。
4.赛诺菲补体C1s靶向抗体疗法获优先审评资格。赛诺菲补体C1s靶向抗体sutimlimab递交的上市申请获FDA授予优先审评资格,预计11月13日前做出回复。如果获批,sutimlimab将成为首款治疗冷凝集素病成人患者溶血的获批疗法。一项Ⅲ期研究CARDINAL结果显示,sutimlimab达其主要和次要终点指标。主要终点定义为在治疗评估时间点(第23、25和26周的平均值),患者的血红蛋白(Hgb)水平较基线时增加至少2 g/dL,或Hgb水平达到12 g/dL以上的正常化水平,且从第5周到第26周无需输血的患者比例。
5.罗氏TIGIT抑制剂联合PD-L1Ⅱ期临床数据积极。罗氏TIGIT抑制剂tiragolumab与PD-L1抑制剂Tecentriq联用,一线治疗PD-L1阳性转移性非小细胞肺癌(NSCLC)的Ⅱ期临床CITYSCAPE达两个主要共同终点。与Tecentriq相比,该组合疗法显著改善患者的客观缓解率(ORR)(31.3%vs16.2%),将患者疾病恶化或死亡风险降低43%;患者的无进展生存期分别达到5.4个月和3.6个月。在PD-L1高表达的患者群中,与Tecentriq相比,组合疗法显著改善患者ORR(55.2%vs17.2%),将患者疾病恶化或死亡风险降低67%。
6.Blueprint公布RET抑制剂最新临床结果。Blueprint Medicines公司在ASCO年会上,公布其RET抑制剂pralsetinib治疗非小细胞肺癌(NSCLC)的注册性临床结果,以及它治疗其它携带RET融合实体瘤的最新结果。截至2019年11月18日,29例携带RET融合的转移性实体瘤患者(非NSCLC)接受pralsetinib的治疗,在2019年7月11日之前注册的患者的疗效数据表明,pralsetinib在甲状腺癌患者中的ORR达到75%,中位DRO为14.5个月,67%获得缓解的患者仍在接受治疗。其它癌症类型患者中,ORR为60%(3/5)。
医药热点
1.25%英国人可能已感染新冠病毒。来自英国曼彻斯特大学等机构的研究人员分析了英国不同地方政府部门发布的相关疫情数据,比较和分析病毒在人群中的感染状况。他们发现,3月中旬,英国疫情蔓延比较快,但随着政府出台措施要求人们保持社交距离等因素,感染状况随之好转;到了4月下旬,英国人口中估计已有超过25%的人被新冠病毒感染过。相关研究结果已刊登在英国《国际临床实践杂志》上。英国卫生部14日发布的疫情数据显示,该国累计确诊病例233151例,累计死亡病例33614例。
2.武汉最后一所新冠定点医院恢复正常诊疗。历经近4个月抗击新冠肺炎斗争后,武汉大学人民医院东院区于5月16日全面恢复正常诊疗秩序。这也是武汉市内最后一所恢复正常诊疗秩序的新冠肺炎重症救治定点医院。武汉大学人民医院东院区病员服务中心主任裴大军介绍,院区所有门诊科室实行网上分时段、实名制挂号,患者在医院官方微信上提前一周即可开始预约。为避免患者扎堆,同时起到分流缓冲作用,院区特意搭设预检分诊大棚,保证患者就医安全。
3.吉林市丰满区调整为高风险疫区。5月16日0—24时,国内新增确诊病例5例,其中境外输入病例2例(天津1例,广东1例),本土病例3例(均在吉林市丰满区);无新增死亡病例;新增疑似病例2例,均为境外输入病例(内蒙古1例,上海1例)。自5月7日吉林舒兰报告1例本地确诊病例至今,吉林省吉林市丰满区累计报告本地确诊病例12例。17日,按照国家新冠肺炎疫情分区分级标准,吉林市丰满区风险等级由中风险调整为高风险。
股市资讯
【安图生物】公司于近日收到国家药品监督管理局颁发的《医疗器械注册证》,具体产品为:新型冠状病毒(2019-nCoV)IgM抗体检测试剂盒(磁微粒化学发光法),新型冠状病毒(2019-nCoV)IgG抗体检测试剂盒(磁微粒化学发光法)。
【华北制药】拟通过发行股份及支付现金方式购买华北制药集团爱诺公司51%股权、华北制药集团动物保健品公司100%股权及华北牌系列商标资产;并拟非公开发行股份募集配套资金。
【上海医药】杭州市西溪谷建设指挥部同意向公司附属企业正大青春宝支付人民币20.09亿元,以补偿正大青春宝因目标物业收储所产生的土地及房屋损失。
审评动向
1. CDE最新受理情况(05月17日)
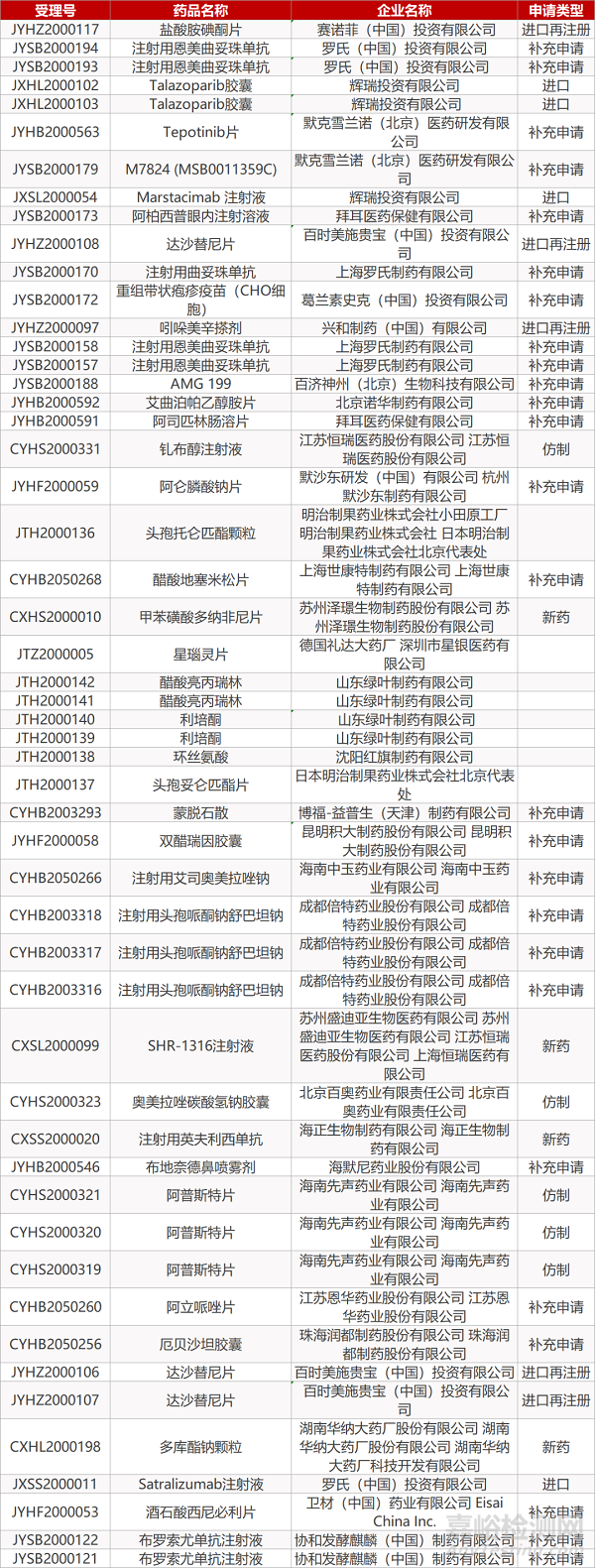
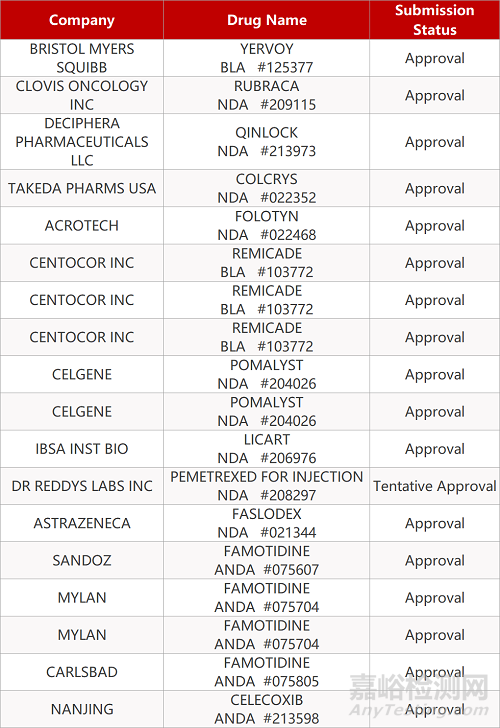
- The End -

来源:药研发


