您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2019-07-04 09:13
QA来检查原始记录了,您的记录完善了吗?有缺项吗?
在药品研发这一行,无论任何形式的核查,原始记录都是重点检查项。因为原始记录是每个实验数据溯源的根本。
核查时单纯因为原始记录不规范造成的问题,也是让人有苦说不出。
啥,原始记录?
药品研究试验记录是指在药品研究过程中,应用实验、观察、调查或者资料分析等方法,根据实际情况直接记录或者统计形成的各种数据、文字、图表、声像等原始资料。
从定义不难看出,原始记录不止手写手写记录,随着科技的发展我们记录中,照片、图像、录像仪器设备自动记录的部分会占越来越大的比重。但是无论如何手写记录不可缺少。
小编个人的理解,手写记录就是把我的实验思路原原本本地记录到纸面上,总体概括为“写我所做,做我所写”。在所有记录中,手写记录才是灵魂,其他的只是原始记录的不同表达形式。
所以今天手写记录是我们的重点。
原始记录的书写原则
(1)真实性
(2)及时性
(3)准确性
(4)完整性
(5)可追溯性
说起来容易做起来难,所以接下来这几条原则会贯穿本文的始终,请大家仔细体会。
原始记录书写要素
实验记录的10项基本要素是
(1)实验名称
(2)实验目的
(3)实验设计或方案
(4)实验时间
(5)实验材料
(6)实验方法
(7)实验过程
(8)观察指标
(9)实验结果和结果分析等内容。

实验名称
这个很好理解,每个实验都有自己的名字。
一般书写格式为“项目名称+实验名称”
可以使用代号代替整个项目,但在具体某一项实验中应该尽可能详细、准确地记录名称,不能过于笼统,以便审查与核对。如:XXX片标准介质中的溶出曲线测定。
实验目的
就是写明白自己做这个试验是为了什么。
很多同学记录写到这里就卡住了,小编见过太多号称做研发的“实验机器”。
都是按照流程和经验一个实验一个实验往下做,根本没思考过做这个试验到底是为了什么。
所以很多同学的记录,压根不写这一块,或者写得特别简单,一笔带过,只是为了老师说记录里要写这块而写。
试验目的应该怎么写?
(1)首先,理解这个试验存在的目的,不明白就问前辈,不好意思问就翻书。
(2)其次,结合自己项目当前的情况,结合试验本身的目的,写明自己做的这个实验想达到的目的。
(3)如果实验为复测,要分析明白复测的原因,比如上次做失败了、上次出现了问题需要进一步研究,等等。
(4)注意专业术语的使用。
实验方案和设计
实验方案对于一个实验的成败非常关键。好的方案可以降低实验失败的概率。坏的方案只要一开始执行就注定你今天的活是白干的。
所以,身为研发的我们,必须发动我们科学家的大脑,设计一个详细、全面并且具有一定预案性的实验方案,而不是急于动手。
比较全面的方案一般包括如下内容:
(1)前期实验的总结
(2)问题分析
(3)初步拟定的方法
(4)拟解决的问题
实验方案应该经过审核、批准后才能开始。
实验方案一旦拟定,可能很多天我们都是用同一个方案来进行实验,比如测定溶出、含量和有关物质。所以对于手写记录的书写,我们也没必要每天重新抄一遍实验方案,搞得自己像个抄作业的,一点都不像科学家。
这时候的方案应该是,将实验方案作为实验记录本的附件保存,参考文献等资料以电子版形式保存。手写的原始记录本上,只需填写方案上面的编号,生效日期和方案名称即可。

而没有实验方案的,以下几种情况也不用全部抄一遍:
1.如有明确来源,只需写明所用实验方法来源、参照文献、资料来源。
2.实验方法若为自拟标准,则需写明自拟质量标准编码,若无编码,需要写明质量标准名称和制定日期或是版本号。
3.若是引用药典标准中的检测方法,需要写明引用的具体是什么内容,如“本次检测采用EP7.0阿托伐他汀钙质量标准中有关物质检测方法”。
实验时间
试验记录本上除了写明年月日外,对于时间要求严格的实验需要记录详细的时间。
遇到下列试验,记得设计个时间统计表:
(1)干燥失重、炽灼残渣需记录冷却时间。
(2)降解实验中样品破坏的具体时间。
(3)沉积体积比的静置时间等。
……
小编只写了代表性的,其余请大家根据项目自行补充,根据项目不同,时间需要记录的精度也不同,有的需要精确到分钟,这时就需要实验人员特别注意。
实验环境
所有实验均应记录实验场地温湿度,一般实验记录大概即可。
对于下列温湿度敏感的试验,必须记录实验实时进行时的温湿度:
(1)比旋度
(2)脆碎度
(3)避光操作
(4)非水滴定
(5)水分测定
(6)称量时可能的波动
(7)红外测定时的环境等
若同一实验在不同的场地进行,可以书写主要实验场地的温湿度。
小编只写了代表性的,其余请大家根据项目自行补充。
实验材料
原则:所有试验中用到的材料应尽可能记录详细的信息。
样品应写明:
(1)样品来源
(2)样品批号

对照品应写明:
(1)来源
(2)批号
(3)含量
(4)流水号
(5)有效期
(6)贮藏条件(如冷藏、冷冻、室温)
(7)若有其他要求需要或特殊对照品应写明使用注意事项
说到对照品,特别提一句:对照品标签、报告书、使用说明书、照片等文件(原件/复印件)须妥善保管,并且保留所有空瓶。
参比制剂应写明:
(1)名称
(2)规格
(3)来源
(4)有效期等
原料应写明:
(1)名称
(2)型号(如有)
(3)批号
(4)级别(如有)、
(5)厂家
(6)含量
(7)水分/干燥失重(如有)等
辅料、包材应写明:
(1)名称
(2)规格
(3)批号
(4)来源
试验所用仪器应写明:
(1)编号
(2)型号
(3)主要参数
(4)是否经过校验或校验日期(天平、溶出仪、液相、紫外、气相等)
色谱柱应写明:
(1)品牌
(2)型号
(3)货号
(4)编号
(5)规格等

试剂应写明:
(1)名称
(2)级别
(3)批号
(4)来源等
滤膜应写明:
(1)名称
(2)孔径
(3)直径
(4)来源等
实验方法
原则:凡实验中各种实验条件,均应进行详细描述。
试验中所用方法要注明来源,如USP、EP、ChP等。
如果用到USP等国外标准,可以做进一步检索,匹配查到的色谱柱信息、试剂信息、参考图谱,便于开展实验和后期审核。
方法中首次用到时应附相关的专利、期刊文献(题目、来源、出版信息等),英文文献应做翻译。

|
常用试验方法 |
需包含信息 |
|
液相色谱 |
(1)仪器信息 (2)色谱柱信息(型号、固定相、内径、柱长、粒径、编号) (3)柱温 (4)流速 (5)检测器、检测波长等 (6)洗脱时间或程序 (7)流动相组成 (8)进样量 |
|
气相色谱 |
(1)仪器信息 (2)进样方式(直接进样或顶空进样) (3)检测器 (4)载气 (5)载气流速 (6)色谱柱信息(型号、固定相、内径、柱长、膜厚、编号) (7)分流比 (8)进样口 (9)检测器温度 (10)升温程序 (11)运行时间 (12)进样量 |
|
溶出 |
(1)溶出装置的来源 (2)转速 (3)温度 (4)介质体积 (5)取样体积 (6)取样点 (7)运行时间等 |
|
其他实验方法 |
(1)紫外检测的波长或波段 (2)不溶性微粒检测的通道 (3)原子吸收光谱波长选择等 |
实验过程
对分析实验来讲,实验过程非常重要,实验人员应熟悉实验步骤,保证实验的顺利完成。
过程中的每一个数据、现象都是非常重要的,要善于观察、分析,缺失任何一个数据都可能导致实验链条的断裂。
一些我们认为很诡异的、莫名其妙的问题,往往可从详细的或错误的记录中发现根源、找到原因。

流动相、溶剂配制:
应按照实际配置过程进行书写,记录要点包括:
(1)化学试剂称量数据
(2)加入的纯化水/有机溶剂等的体积
(3)调节的具体pH值和调节剂
(4)溶解方式
(5)脱气方式及时间
(6)有效期等
若为引用,必须写明实验记录本编号和页码。
重新配置的流动相,必须重新书写配制过程。

样品配制:
应根据实际配置过程进行书写,记录要点包括:
(1)样品处理方式(研细或去除包衣层)
(2)称样量
(3)移取体积(液体样品)
(4)配制过程
(5)稀释剂
(6)超声时间
(7)滤过用滤膜的材质和孔径
(8)离心的转速与时间和温度等
若配制过程与本实验内容前面的记录中完全一致,需写明实际称样量,配制过程可简写“同XX页XXX项下XXX批号样品溶液配制”。多批次样品配制过程相同时,第一份配制样品需写详细配置过程,其他可只写称样量,配制过程写“同第一份样品”,如影响因素考察项下各条件下样品的配制。
TLC实验:
记录要点包括:
(1)展开剂信息
(2)薄层板信息
(3)展开剂饱和时间
(4)展时
(5)展距
(6)展稳
(7)点样量等
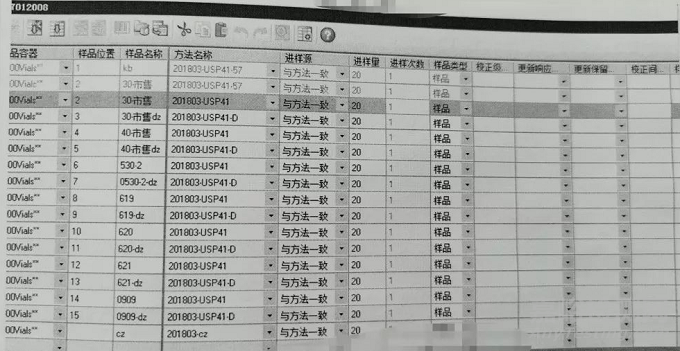
液相、气相、紫外等:
均需打印进样序列,完整体现本次实验的所有进样内容,并粘贴在记录本上。
其他:
(1)使用放置时间过长的溶液,需注明储存条件、有效期、溶液配置日期及配制操作所在记录本编码和页码,并需有证明性材料证实其稳定性。
(2)虽然实验记录的书写与质量标准的书写格式有不同之处,但仍需注意准确运用专业术语。
如:
取样过程中,正确表述为“取本品”,而不是“用本品”;
稀释剂的书写,正确表述为“乙腈-水(1:1)”,而不是50%乙腈水溶液;
溶解过程中,正确表述为“加XX溶解”,而不是“用XX溶解”;
定容的正确表述应为“稀释至刻度”,
溶液名称,正确表述为“供试品溶液”,而不是“样品溶液”等。
实验结果
试验结果就是根据采集的数据和图谱,要对实验结果进行统计分析,并将实验结果与实验目的和要求进行对比。
如“XX片中杂质A精密度试验中,连续6针峰面积的RSD小于等于2.0%,精密度符合要求”。
试验结果注意事项如下:
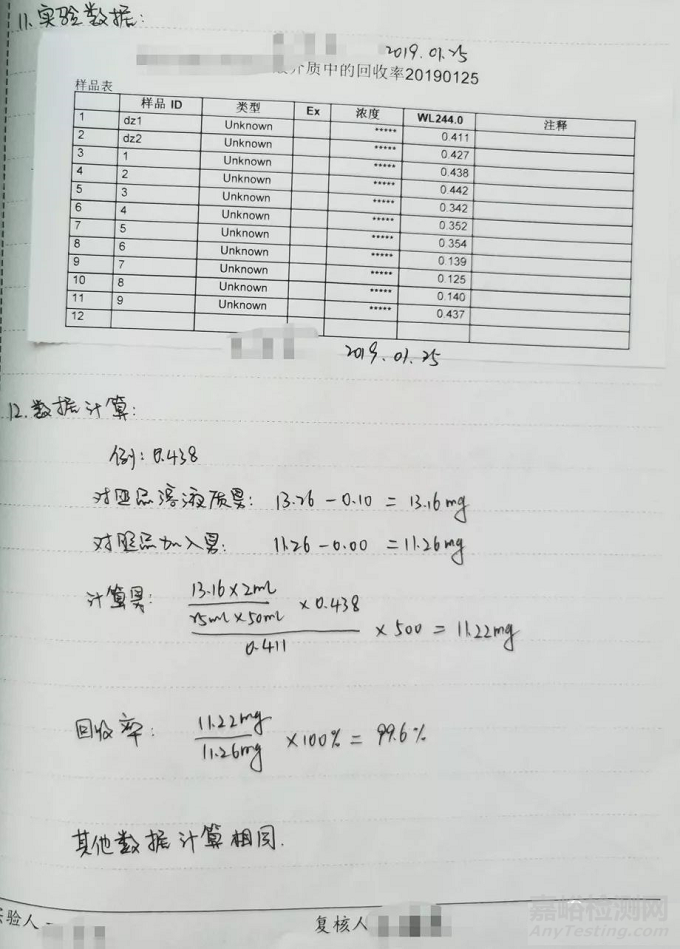
公式的运用:
在采用计算公式进行计算时,应保证公式的正确性并标明公式中每个符号代表的意义。
如累积溶出量计算公式,校正因子计算公式等,并需至少代入一组数据手动计算,以核对计算模板的准确性。
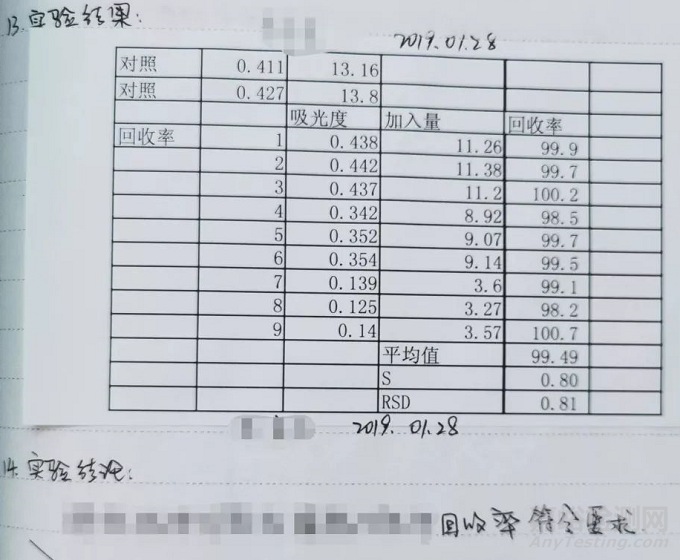
表格的运用:
结果用表格进行表示的,需有表头说明是何种结果,如“XX片在标准介质中的溶出曲线结果”。
表中的数据需说明代表何种意义,表示浓度的,需表明计量单位。
结果统计表可手写在记录本上,也可将结果打印粘贴在记录本上,打印粘贴的结果统计表尽量不要超过一页纸大小,粘贴后骑缝签名、写日期。
仪器自带打印记录:
某些测定结果,如滴定、水分、天平称量等可以使用仪器自带的打印功能直接打印出来。
自动打印的记录贴在记录本上,骑缝签名和日期。如果使用的是热敏纸打印的信息,需要复印并和原图一起粘贴在实验记录本上,并骑缝签名、写日期。
实验图谱信息
实验图谱信息应准确完整,并与实际内容相符。HPLC、GC等图谱中应包括样品名称、批号、进样时间、图谱处理时间、序列号、进样次数、色谱仪器编码、进样体积、峰保留时间、峰面积、存储路径、实验者姓名等信息,若信息不完整需手写补充,并签名、写日期。

TLC信息记录
对于TLC图,并注明样品信息、展开剂、显色条件,计算Rf值,同时需拍照保留电子版,电子版照片按照“实验日期-实验记录本编号-页码”命名,方便调看。
其他
(1)原始记录应保持规范、整齐、美观。如后续实验引用到了之前的原始数据,如果不在相同的记录本上,应该注明之前数据的出处。比如记录本编号:XXXX,页码XX。
(2)异常数据不得删除,需进行异常原因分析,涉及复测的应该复测。
(3)大部分实验员会一天进行多项试验,一般都会是液相或是气相与理化鉴别同时进行,那么在记录本上要注意实验内容的前后衔接问题。
例如在一本原料测定实验记录本中第9页书写的是“2019年6月1日原料有关物质测定”的实验记录,第10页书写的是“2019年6月2日炽灼残渣测定实验”的实验记录,第11页书写的是“2019年6月1日原料有关物质测定试验的结果与结论”的实验记录,那么应该在第9页实验记录的最后写明“下接第11页”,并在第11页实验记录的最开始写明“上接第9页”。
结果分析
每次实验结果都应有确切的数据分析和文字总结。但是,存在一些实验暂时无法给出明确的结论,甚至有可能是错误的结论,对于这种情况,分析工作中可以不用写下明确的结论。
对于异常的数据,如个别峰面积异常偏大或偏小、峰位或基线漂移、重复性不好、溶出曲线均一性差等,要分析原因,进行异常调查,提出解决思路和方法,以便为下一步的实验制定实施方案。
实验人、复核人
实验人应是所有参与试验的人员,合作研究的人员也应该签名,应注明每个人具体做了哪部分工作,便于日后核对。

例如,含量测定中,一人负责配流动相,一人负责配制样品,还有液相测定、处理数据等,这些人应清楚记录自己负责的部分。
复核人为项目负责人或项目负责人指派的其他复核人。复核人应及时对实验记录进行复核,复核合格后签名。如有问题,要及时反馈给实验者或复核人员进行修改,并签名,写日期。
参考文献:《药品研究实验记录暂行规定》

来源:喬小木、药研江湖


