您当前的位置:检测资讯 > 实验管理
嘉峪检测网 2025-08-04 19:15
二氯乙酸(DCAA)、三氯乙酸(TCAA)作为氯化消毒副产物,具有肝毒性,能引发肝腺瘤和干细胞癌等。2001 年,我国发布的《生活饮用水卫生规范》中规定DCAA和TCAA分别不得超过0.05,0.1mg·L−1;2006年,GB 5749—2006《生活饮用水卫生标准》中将这两种组分划分为非常规检测指标,并且发布了配套检测标准GB/T 5750.10— 2006 《生活饮用水标准检验方法 消毒副产物指标》;2022年,更新后的GB 5749—2022 《生活饮用水卫生标准》直接将DCAA和TCAA划分为常规检测指标,导致这两种组分的检测需求大大提升。目前检测这两种组分的方法主要有离子色谱法、气相色谱法和高效液相-串联质谱法等。与另外两个检测方法相比,离子色谱法具有操作简单、价格低廉等优势。F−、Cl−、NO3−―N(硝基氮)、SO42−为GB 5749—2022规定的常规阴离子检测指标,但是采用离子色谱法检测时,通常需要将氯化物及硫酸盐除掉,无法实现DCAA、TCAA以及上述4种常规阴离子的同时检测,这给日常水质检测带来了诸多不便。鉴于此,研究人员采用 A SUPP 7-250色谱柱为固定相,含5.0mmol·L−1碳酸钠的8%(体积分数,下同)乙腈溶液为淋洗液,在离子色谱仪上以等度洗脱方式实现了生活饮用水中这 6种组分的准确定量分析。
1试验方法
采用棕色螺口玻璃瓶采集水样,于 0~4℃冷藏保存7d,通过英蓝超滤进样装置进样测定。
2结果与讨论
2.1 淋洗液的选择
结合A SUPP 7-250色谱柱填充材料的性质,应采用碳酸盐体系的淋洗液,因此试验先采用3.6,5.0,6.4mmol·L−1 碳酸钠溶液进行淋洗。结果显示,各组分的保留时间均较长(TCAA的保留时间大于40min),且保留时间随碳酸钠溶液浓度的增加基本不变;TCAA的峰形不够理想,同时响应值较低,在低浓度水平时可能难以识别。其中,5.0mmol·L−1碳酸钠溶液淋洗后的色谱图见图1。
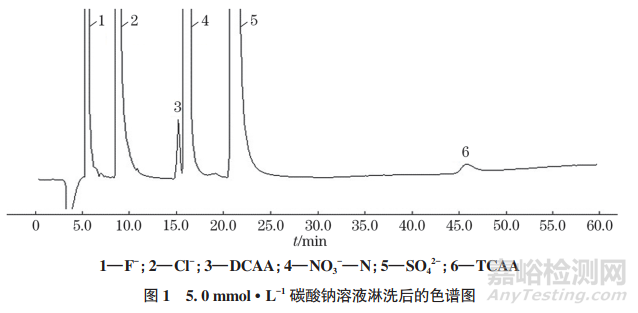
考虑到A SUPP 7-250色谱柱对有机溶剂具有一定耐受性,试验采用含3.6,5.0,6.4mmol·L−1碳酸钠的5%(体积分数,下同)乙腈溶液进行淋洗。结果显示,随着碳酸钠浓度的增加,检测时间有效缩短,但是背景电导增加,影响低浓度水平的DCAA和TCAA的检测,同时 DCAA和NO3−―N的色谱峰有重叠的风险。综合比较,含5.0mmol·L−1碳酸钠的淋洗液对6种组分的分离效果最好,因此试验进一步比较了分别以含5.0mmol·L−1碳酸钠的5%,8%,10%(体积分数,下同)的乙腈溶液淋洗时6种组分的分离效果。结果显示,随着乙腈体积分数的增加,TCAA的保留时间逐渐缩短。考虑到乙腈体积分数为8%,10% 时各组分的保留时间差异不大且色谱峰峰形及分离度均较好,试验选择有机试剂含量更低的含5.0mmol·L−1碳酸钠的8%乙腈溶液为淋洗液,并在A SUPP 7-250 色谱柱的最大耐受流量(0.8mL·min− 1)下检测,各组分可在35min内完成有效分离。
2.2 柱温的选择
A SUPP 7-250色谱柱的温度使用范围为20~ 60℃,因此试验比较了柱温分别为35,45,55℃时色谱柱的 响 应 情 况。 结果显示:柱温为35℃时,柱压明显升高,超过色谱柱的最大耐受压力 (15MPa),仪器会强制停止试验;升高柱温,DCAA、F−、Cl−、NO3−― N、SO42−的保留时间缩短,TCAA的保留时间没有明显变化。考虑到柱温较高会加速色谱柱的柱效下降和使用寿命缩短,试验选择的柱温为45℃。
在优化的仪器工作条件下,混合标准溶液的色谱图见图2。
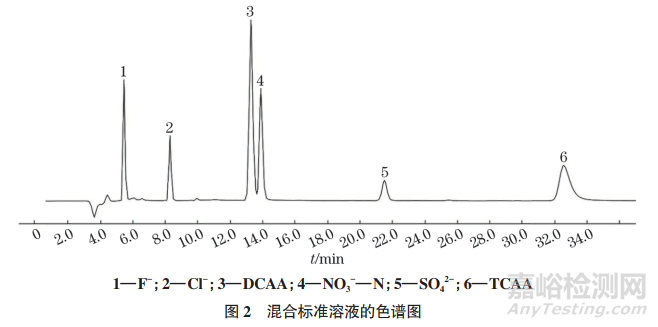
2.3 标准曲线和检出限
按照仪器工作条件测定混合标准溶液系列,以各组分的质量浓度为横坐标,对应的峰面积为纵坐标绘制标准曲线,线性参数见表1。
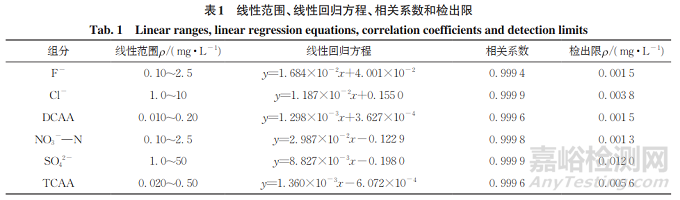
按照仪器工作条件对标准曲线最低浓度点的混合标准溶液重复测定6次,以3倍测定值的标准偏差s计算检出限(3s),结果见表1。
2.4 精密度和回收试验
按照试验方法对阴性水样进行低、中、高等3个浓度水平的加标回收试验,每个浓度水平平行测定6次,计算回收率和测定值的相对标准偏差(RSD),结果见表2。
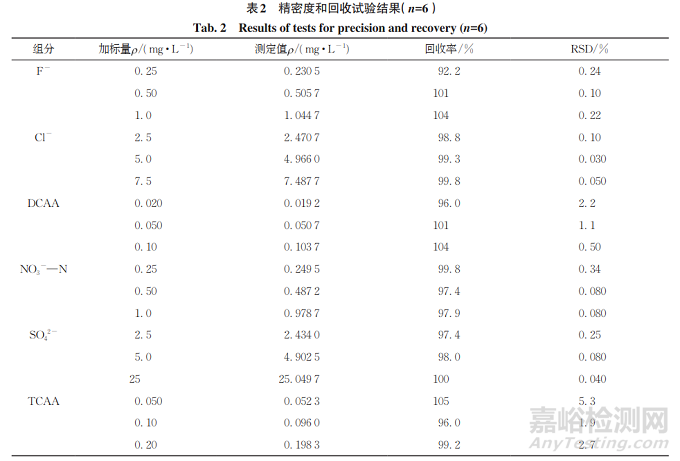
结果显示:6种组分的回收率为92.2%~105%,测定值的RSD为0.030%~5.3%,说明方法的准确度和精密度较好。
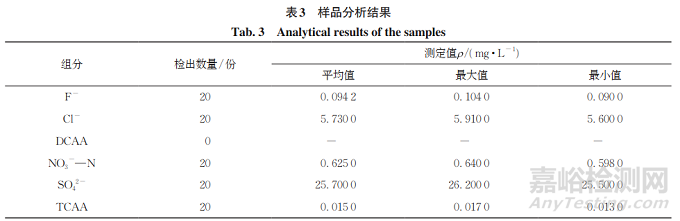
2.5 样品分析
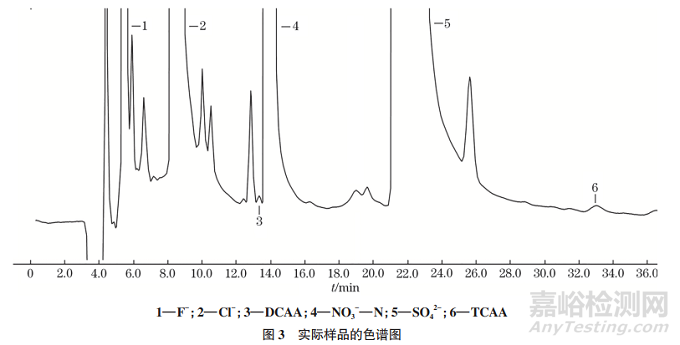
随机抽取成都市武侯区各小区及公共场所的自来水20份,按照试验方法分析,检出结果见表3。其中,一份样品的色谱图见图3。
3试验结论
研究人员提出的离子色谱法可以快速、一次性完成生活饮用水中DCAA、TCAA、F−、Cl−、NO3−—N、SO42−的同时测定,并且不需要复杂的样品前处理,降低了时间成本与人力成本,具有一定应用推广价值。

来源:理化检验化学分册


