今日头条
兴齐儿童近视新药拟纳入优先审评。兴齐眼药改良型新药硫酸阿托品滴眼液(SQ-729)的上市申请获CDE拟纳入优先审评,适应症为用于延缓儿童近视进展。在Ⅲ期研究中,与安慰剂组相比,硫酸阿托品滴眼液组在主要疗效指标上有统计学意义的显著性改善,而且药物安全性良好,患者使用依从性好。目前,国内尚无延缓儿童近视进展的低浓度硫酸阿托品滴眼液获批上市。
国内药讯
1.卫材抗癫痫药物口服混悬液中国获批上市。卫材抗癫痫药物吡仑帕奈(Fycompa)的口服混悬液新制剂获国家药监局批准上市,用于治疗成人和4岁及以上儿童癫痫部分性发作(伴有或不伴有继发全面性发作)的治疗。Fycompa是一款高选择性非竞争性AMPA型受体拮抗剂,其片剂(商品名为卫克泰)已在国内获批用于12岁及以上癫痫部分性发作患者(伴有或不伴有继发性全面性癫痫发作)的辅助治疗;以及用于成人和4岁及以上儿童癫痫部分性发作患者的治疗。
2.拜耳「非奈利酮」在中国获批治疗慢性肾病。国家药监局批准拜耳制药非奈利酮(Kerendia)的拓展适应症,用于2型糖尿病相关的慢性肾脏病早期阶段的治疗。非奈利酮是一种非甾体选择性盐皮质激素受体拮抗剂,此前已在中国获批用于治疗与2型糖尿病相关的慢性肾脏病成人患者,可降低eGFR持续下降、终末期肾病的风险。
3.恒瑞PD-1单抗组合疗法美国报肝癌NDA。恒瑞医药PD-1抑制剂卡瑞利珠单抗已在美国提交新药申请(NDA),联合VEGFR2抑制剂甲磺酸阿帕替尼片用于一线治疗不可切除肝细胞癌(uHCC)患者。在国际III期CARES 310研究(NCT03764293)中,与索拉非尼相比,卡瑞利珠单抗联合阿帕替尼显著延长患者的无进展生存期(中位PFS:5.6个月vs3.7个月,p<0.0001。)以及总生存期(中位OS:22.1个月vs15.2个月,p<0.0001)。今年1月,该组合疗法上述适应症已获批国内上市。
4.北京百泰EGFR单抗报食管癌NDA。百泰生物EGFR单抗尼妥珠单抗的新适应症上市申请获CDE受理,推测申报的适应症为联合放化疗治疗不可切除局部晚期食管癌。公布于ASCO 2022会议上的III期NEXCELL1311研究结果显示,与单纯放化疗相比,尼妥珠单抗联合放化疗治疗使局部晚期食管鳞癌患者实现完全缓解的比例更高(32.5%vs12.2%,P=0.002),达到客观缓解率的比例更高(93.8%vs72%,P<0.001)。
5.博安CEA/CD3双抗获批实体瘤临床。博安生物1类生物药BA1202获国家药监局批准开展用于实体瘤治疗的临床研究。这是一款靶向CEACAM5 (CEA)和CD3的双抗药物,一端与肿瘤细胞上的CEA二价且高亲和力结合,另一端与T细胞上的CD3单价且相对低亲和力结合,同时保留Fc区,通过激活内源性T细胞清除CEA阳性肿瘤细胞,在降低CRS风险的同时可保证优异的药物疗效。目前,全球尚无CEA/CD3双抗获批上市。
6.德琪FIC靶向CD24单抗获批临床。德琪医药潜在“first-in-class”CD24单抗ATG-031获FDA批准开展首次人体I期临床,评估用于晚期实体瘤或B细胞非霍奇金淋巴瘤(B-NHL)患者治疗的安全性和有效性。ATG-031可阻断肿瘤微环境(TME)中的 “别吃我” 信号。在临床前研究中,ATG-031可纳摩尔级别亲和力与CD24特异性结合并阻断CD24与Siglec-10的互动;并可诱导皮摩尔EC50水平的高效吞噬作用,并促进巨噬细胞分泌促炎细胞因子。
7.贝达引进EGFR/c-Met双抗报IND。贝达药业1类生物制品注射用MCLA-129的临床试验申请获CDE受理,拟联合第三代EGFR-TKI产品甲磺酸贝福替尼胶囊开展联合用药临床研究,评估用于具有表皮生长因子受体(EGFR)外显子19缺失或外显子21(L858R)置换突变的局部晚期或转移性非小细胞肺癌(NSCLC)成人患者的治疗潜力。MCLA-129是Merus公司开发的一款拟用于治疗实体瘤的EGFR/c-Met双抗,贝达药业拥有该新药的中国权益。
8.先声引进失眠症新药报IND。先声药业从瑞士Idorsia公司引进的失眠症新药daridorexant的临床试验申请获CDE受理。Daridorexant是一款双重食欲素受体(orexin receptor)拮抗剂,可通过阻断促觉醒神经肽食欲素的结合,抑制过度活跃的不眠状态。该新药已于2022年1月在美国获批上市,商品名为QUVIVIQ。先声药业拥有daridorexant在大中华地区(中国大陆、香港、澳门)开发和商业化的独家权利。
国际药讯
1.雅培脊髓刺激系统获批扩展适应症。雅培脊髓神经刺激(SCS)系统获得FDA批准新适应症,用于治疗手术选择有限的慢性背部疼痛患者。这一新适应症将涵盖雅培在美国的整个SCS设备组合,包括免于充电的Proclaim SCS系列和可充电的Eterna SCS产品。SCS是一种神经调节技术,植入的电极通过调节传输到大脑的疼痛信号,起到减轻疼痛的效果。
2.EGFR-TKI联合化疗肺癌III期临床成功。阿斯利康第三代EGFR抑制剂奥希替尼联合化疗治疗携带EGFR突变的非小细胞肺癌(NSCLC)的III期Flaura2研究结果积极。与奥希替尼单药组相比,奥希替尼联合化疗治疗显著延长患者的无进展生存期(PFS)。目前总生存期(OS)数据尚未成熟。安全性数据和不良事件导致的停药率与每种药物的既往研究数据一致。
3.罗氏BTK抑制剂RMS II期临床成功。罗氏三代BTK抑制剂fenebrutinib治疗复发多发性硬化症(RMS)的II期FENopta研究达到主要终点和关键次要终点。与安慰剂组相比,fenebrutinib组患者第12周时新发T1病灶数量显著减少(P=0.0022);第4/8/12周时新发或扩大T2病灶数量亦显著减少。目前,罗氏正在开展三项fenebrutinib用于MS的III期注册性临床试验,预计这三项研究将于2025年和2026年完成。
4.MyoGene公司融资开发新型DMD基因疗法。MyoGene Bio公司宣布获得非营利组织CureDuchenne风险投资公司旗下CureDuchenne Ventures的投资款项,具体金额暂未对外披露。MyoGene将利用这笔资金推进其针对杜氏肌营养不良症(DMD)的新型AAV基因疗法MyoDys45-55的开发。MyoDys45-55采用CRISPR/Cas9基因编辑方法,旨在永久删除存在Duchenne突变的DNA区域以恢复抗肌萎缩蛋白的表达。据悉,CureDuchenne公司已支持了17个DMD相关项目进入到人体临床试验。
5.安斯泰来联合索尼开发ADC技术平台。安斯泰来宣布与索尼达成一项合作研究协议,将利用索尼独特的聚合物材料“KIRAVIA”开发新型抗体-偶联药物平台。2020年3月,索尼推出一种新型、有机高分子荧光染料KIRAVIA Dyes,KIRAVIA染料聚合物的结构经过独特设计,通过控制骨架上染料分子之间的距离,减弱相邻染料分子之间的猝灭现象从而提升亮度。根据协议,两家公司将使用KIRAVIA骨架作为连接子,共同开发和优化一个新的ADC平台。
6.Cambrex完成沃尔瑟姆的化学设施扩建。全球合同开发和制造组织(CDMO)Cambrex公司宣布,Snapdragon Chemistry已完成了其在马萨诸塞州沃尔瑟姆的5.1万平方英尺(4700多平米)扩建项目的二期工程。此次扩建为Snapdragon的活性药物成分(API)开发和制造设施增加了1.2万平方英尺(1100多平米)的面积。新实验室配备100L和60L搪玻璃钢反应釜、10L塞流式反应器、切向流过滤和纳滤橇、5kW光化学反应器,以及符合GMP标准的LabOS数据采集与监控系统。新套间将于2023年6月投入运营。
医药热点
1.广东省人民医院挂牌南方医科大学附属医院。近日,广东省人民医院官网显示,该院已挂上了“南方医科大学附属广东省人民医院”的牌子,成为南方医科大学非直属附属医院。2022年10月28日,南方医科大学与广东省人民医院签署了深度战略合作协议,此次挂牌便源于双方在去年签署的深度战略合作协议中的一项内容。据悉,广东省人民医院此前曾是华南理工大学的直属附属医院之一。
2.新冠感染次数越多后遗症风险越高。近日,国家感染性疾病临床医学研究中心2023年学术年会在北京召开。关于“长新冠”的争议,中科院院士高福认为,长新冠是一个基本事实,不要回避,不要因为长新冠可能对人类有影响就不敢讲,这不是科学的态度。高福院士还提醒民众,新冠感染次数越多,后遗症风险越高,病人该诊断要诊断,该用药要用药。
3.百济神州将为29个国家免费提供泽布替尼。百济神州与Max Foundation签署协议,将在未来三年内免费向29个中低收入国家的慢性淋巴细胞白血病(CLL)患者提供泽布替尼。泽布替尼(商品名:百悦泽)是一款布鲁顿氏酪氨酸激酶抑制剂(BTKi),已于今年初获FDA批准CLL适应症。此前,Max基金会与诺华、BMS、辉瑞、武田和Incyte就其它癌症药物达成了类似的协议。
评审动态
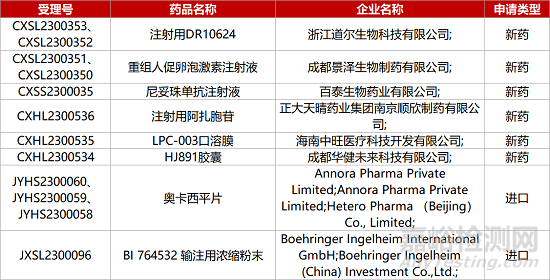
1. CDE新药受理情况(05月18日)
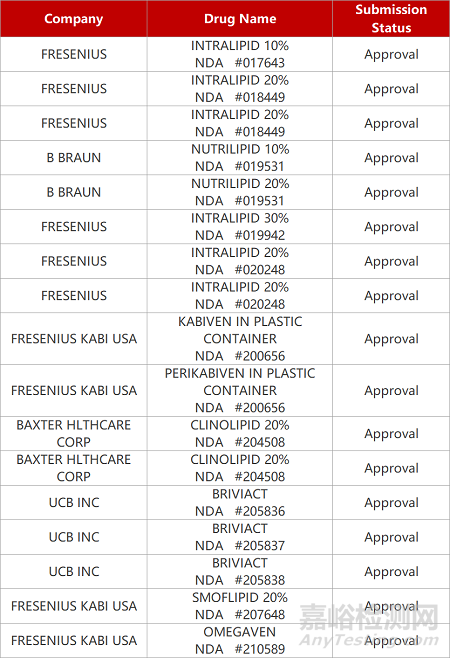
2. FDA新药获批情况(北美05月17日)