今日头条
睿诺急性胰腺炎新药获批Ⅱ期临床。上海睿诺1类化药注射用RN-0001获国家药监局批准开展Ⅱ期临床,评估用于急性胰腺炎(AP)治疗的有效性与安全性。RN-0001具有新颖的作用机制和靶点。该新药此前已获批开展用于“重大手术后急性肾损伤(AKI)”治疗的Ⅱ期临床,该项试验将由四川大学华西医院牵头,在全国多家临床中心开展。
国内药讯
1.石药新冠mRNA疫苗获批紧急使用。石药集团新冠mRNA疫苗SYS6006获国家药监局纳入紧急使用,预防新冠感染引起的疾病(COVID-19)。在10.12.2022-18.1.2023期间开展的临床研究(SYS6006-008)中,以重组蛋白疫苗为对照,SYS6006在序贯加强接种后7-28天期间和接种后14-28天期间,疫苗的保护效力分别达到70.2%和85.3%。这也是中国首个自主研发并获得紧急授权使用的mRNA疫苗。
2.艾美斐小分子GPCR拮抗剂获批临床。艾美斐生物自研创新药IPG11406获FDA批准开展I期临床,评价用于健康成人受试者中的安全性、耐受性和药代动力学特征。IPG11406是一款针对包括炎症性肠病(IBD)在内的自身免疫性疾病开发的小分子GPCR拮抗剂,可阻断该GPCR介导的下游信号通路,抑制多种免疫细胞向病灶部位迁移和增殖,完全清除自身免疫性疾病病灶部位的炎症细胞,降低促炎因子的表达。
3.赫吉亚NASH新药上I期临床。上海赫吉亚自研拟用于治疗非酒精性脂肪性肝炎(NASH)的创新药Kylo-0603在浙江大学医学院附属第一医院正式启动I期临床,拟评估用于中国健康受试者单次和多次给药后的安全与耐受性、药代动力学(PK)特征。Kylo-0603同时具有GalNAc结构以及类似甲状腺激素T3结构,既具有主动的高效肝组织靶向性,又对THR-β具有高的亲和力和选择性,有望成为Best-in-class的治疗药物。
4.信达GLP-1R/GCGR激动剂获批NASH临床。信达生物申报的GLP-1R/GCGR激动剂Mazdutide(IBI362)获国家药监局批准开展用于治疗非酒精性脂肪性肝炎(NASH)的临床研究。在临床前研究中,IBI362已显示出可明显下降NAS评分,包括脂肪变性、气球样变和炎症指标。去年11月,信达生物在国内登记启动IBI362的一项III期DREAMS-1研究,拟在单纯饮食运动控制不佳的2型糖尿病患者中评估IBI362的有效性和安全性。
5.博芮健可入脑TrkB受体激动剂获批临床。上海博芮健制药1类化药BrAD-R13片获国家药监局临床试验默示许可,拟用于治疗轻、中度阿尔茨海默症(AD)。BrAD-R13是一款具有血脑屏障高通透性的TrkB受体激动剂,可通过激活BDNF(脑源性神经营养因子)-TrkB信号通路,起到神经保护和调节突触可塑性等生理作用,从而改善患者在临床上学习与记忆能力衰退和认知功能障碍等症状。
6.九芝堂美科干细胞疗法获批中风临床。九芝堂美科(北京)1类生物药“人骨髓间充质干细胞注射液”获国家药监局批准开展用于缺血性脑卒中的临床研究。2021年1月,九芝堂美科已在首都医科大学附属北京天坛医院发起我国首个使用进口干细胞治疗缺血性卒中的Ⅰ/Ⅱa期临床,评估单次注射Stemedica公司缺血耐受人同种异体骨髓间充质干细胞(it-hMSC)的安全与有效性。该项研究也是我国首个按照药品申报方式开展的干细胞治疗临床试验。
国际药讯
1.度普利尤单抗在欧盟获批用于婴幼儿湿疹。欧盟(EC)批准赛诺菲与再生元联合开发的IL-4/IL-13抗体度普利尤单抗(Dupixent)扩展适应症,用于治疗6个月以上至5岁重度特应性皮炎儿童患者。在Ⅲ期临床中,与安慰剂相比,度普利尤单抗显著提高达到总体疾病严重程度改善75%或以上的患者比例(46%vs7%),以及皮肤症状清除或几乎清除的患者比例(14%vs2%)。而且安全性特征与在6岁以上特应性皮炎儿童中观察到的结果相似。
2.Selecta公司痛风新药两项Ⅲ期临床积极。Selecta Biosciences与Sobi公司开发的每月一次创新组合疗法SEL-212(由聚乙二醇化尿酸酶与减低抗药物抗体(ADA)生成的ImmTOR组成),在治疗慢性难治性痛风患者的两项Ⅲ期临床(DISSOLVE I和DISSOLVE II)达到主要终点。在DISSOLVE I试验中,高剂量SEL-212治疗较安慰剂显著提高患者的缓解率(56%vs4%,p<0.0001);在DISSOLVE II试验中,两组患者的缓解率分别为47%和12%(p=0.0002)。此外药物的总体耐受性良好。
3.吉利德CAR-T治疗R/R LBCL的Ⅲ期临床成功。吉利德旗下Kite公司靶向CD19的CAR-T疗法Yescarta(axicabtagene ciloleucel)用于二线治疗复发/难治性大B细胞淋巴瘤(R/R LBCL)的Ⅲ期临床ZUMA-7最新结果积极。该试验此前已达到无事件生存期(8.3个月v2.0个月)的主要终点。最新数据(即首例患者随机化后5年进行OS分析)显示,与标准治疗相比,Yescarta治疗组显著改善患者的总生存期。详细数据将公布于医学会议上。
4.双机制肥胖症新药II期临床积极。Altimmune公司GLP-1R/胰高血糖素受体双激动剂pemvidutide用于治疗肥胖的II期MOMENTUM研究中期结果积极。治疗24周时,pemvidutide(1.2mg、1.8mg和2.4mg)组受试者平均体重降低幅度分别达到7.3%、9.4%和10.7%,安慰剂组降幅为1.0%(三种剂量组与安慰剂相比p<0.001);次要终点包括受试者腰围(内脏脂肪的一种测量方法)和血脂等指标也明显改善。主要的不良事件为上胃肠道反应,包括恶心和呕吐。
5.基因编辑技术公司Seamless完成种子轮融资。Seamless公司宣布完成1250万美元的种子轮融资,主要用于推进其专有的基于设计重组酶(designer recombinases)的新型基因编辑平台,并扩大公司在欧盟和美国的业务。Seamless的技术平台能够成功针对任何给定的目标序列制作出位点特异性的重组酶,并做出一系列特异性改变,从小DNA片段到大DNA片段都能进行倒置、切除、替换和插入的操作。
6.第一三共终止引进Zymeworks双抗平台协议。Zymeworks子公司Zymeworks BC日前透露,第一三共已终止引进其双特异性抗体技术平台的许可协议。Azymetric技术平台能够将单抗转化为双抗,能够同时结合两个不同的靶标。该技术平台开发的抗体药物可以阻断多个信号通路,将免疫细胞募集到肿瘤,增强受体聚集和降解,并增加肿瘤特异性靶向,具有提高疗效同时降低毒性和耐药性的潜力。此次协议终止后,该公司仍可保留几款抗体的非独家特许使用权。
7.2022年辉瑞CEO年收入3300万美元。近日,辉瑞在股东签署的委托书中披露,其CEO Albert Bourla 2022年薪酬为3300万美元,与2021年的2435万美元相比,涨薪36%。辉瑞2022年财报显示,全年营收达到1003.3亿美元(+23%),是全球首个年收入超千亿美元的制药企业;其中,新冠疫苗Comirnaty和新冠口服药Paxlovid的销售额分别达到378.06亿美元和189.33亿美元,合计567.39亿美元。
医药热点
1.江苏成立院前急救质量控制中心。江苏省医疗质量控制中心管理办公室发布《关于成立江苏省院前急救质量控制中心的通知》,南京市急救中心正式成为江苏省院前急救质量控制中心挂靠单位。未来,该中心将进一步加强江苏省院前急救行业管理,积极推进并逐步建立规范的全省院前急救医疗质量控制体系,不断提高院前急救医疗质量,提升服务质量和突发事件应急医疗救援能力。
2.浙江嘉兴鼓励执业药师多点执业。3月15日,浙江嘉兴市监局正式发布《嘉兴市零售药店执业药师多点执业管理办法(试行)》文件,自4月14日起施行。通知中提及:鼓励执业药师(含执业中药师)利用节假日和业余时间在零售药店(含单体药店、药品零售连锁门店)多点执业,作为零售药店注册执业药师不在岗或人数无法满足审方和药事服务等业务需求时的补充。
3.山东省立医院开展糖尿病一站式诊疗服务。为方便糖尿病患者高效就医,山东第一医科大学附属省立医院(山东省立医院)内分泌与代谢病科开展规范化的“一站式”糖尿病慢性并发症检测及防治。内分泌与代谢病科门诊MMC检查室,配备免散瞳眼底照相机、四肢动脉硬化检测仪、内脏脂肪检测仪、神经传导速度检测仪等设施设备,患者可完成全面快速检测、数据分析、健康宣教等“一站式”诊疗服务。
评审动态
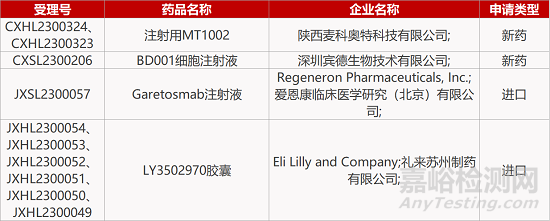
1. CDE新药受理情况(03月22日)
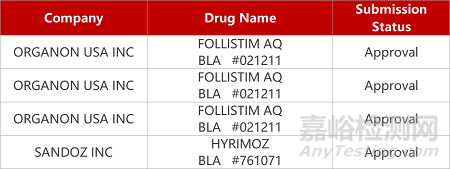
2. FDA新药获批情况(北美03月21日)