您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-12-06 11:02
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
国内药讯
1.罗氏创新CD79b-ADC在华报NDA。罗氏注射用维博妥珠单抗(Polatuzumab vedotin)的上市申请获国家药监局受理。该新药是首个在国内申报上市的CD79b抗体偶联药物(ADC),能够与CD79b蛋白特异性结合并释放化疗药物来破坏B细胞,以降低其对正常细胞的影响。2019年6月,维博妥珠单抗(Polivy)首次获FDA批准上市,联合苯达莫司汀和利妥昔单抗用于治疗复发或难治性弥漫性大B细胞淋巴瘤(DLBCL)。
2.艾美斐MIF抑制剂国内获批临床。艾美斐生物1类新药IPG1094片获国家药监局临床试验默示许可,用于治疗实体瘤和多发性骨髓瘤。IPG1094是一款FIC小分子MI抑制剂,已在临床前研究中显示对多种实体肿瘤,多发性骨髓瘤以及银屑病、红斑狼疮等自身免疫性疾病具有良好治疗作用,同时在渐冻症、阿尔茨海默病方面也具有治疗潜力。该新药目前已在美国获批临床;在澳大利亚开展I期临床。
3.诺华新一代IgE抗体在华报IND。诺华下一代抗免疫球蛋白E (IgE)单抗ligelizumab (QGE031)的临床试验申请获CDE受理。Ligelizumab目前在国外处于III期临床开发阶段,已获FDA授予突破性疗法认定,用于治疗对H1-抗组胺药治疗反应不足的慢性自发性荨麻疹。在一项IIb期(NCT02477332)剂量探索性研究中,与诺华上一代IgE抗体Xolair (奥马珠单抗)组相比,ligelizumab组荨麻疹得到完全缓解人数更多(51%vs26%)。
4.Omeros公司MASP-2抑制剂在华报IND。Omeros公司治疗用生物制品1类新药OMS721(arsoplimab)注射液的临床试验申请获CDE受理。这是国内第二款申报临床的MASP-2抑制剂,康诺亚MASP-2单抗CM338已于上个月获批临床。在美国,Omeros已向FDA递交OMS721用于治疗造血干细胞移植后血栓性微血管病(HSCT-TMA)的BLA申请,FDA已回复一封完整回复函,并要求该公司提供更多的数据来支持监管部门的批准。
5.康辰药业特立帕肽类似药国内报IND。康辰药业3.3类新药特立帕肽注射液的临床试验申请获CDE受理。这是一款由Pfenex公司开发的特立帕肽生物类似药,康辰生物通过与泰凌医药合作获得了Bonsity在中国大陆、中国香港、新加坡、马来西亚和泰国的权益。原研产品礼来的特立帕肽(Forteo)已在2002年11月获批上市,销售峰值达到17.49亿美元,是骨质疏松领域的重磅药物。
国际药讯
1.Keytruda辅助治疗早期黑色素瘤获FDA批准。FDA批准默沙东重磅PD-1抗体Keytruda作为辅助疗法,治疗接受过手术切除治疗的IIB和IIC期黑色素瘤患者(12岁以上)。在一项Ⅲ期临床中,中位随访为14.4个月时,Keytruda与安慰剂相比,将患者疾病复发或死亡的风险降低35%(HR=0.65,95% CI: 0.46, 0.92; p=0.0132)。此前,该药已获批用于III期黑色素瘤患者的辅助治疗。
2.抗焦虑口服新药获FDA快速通道资格。FDA授予Bionomics公司FIC口服疗法BNC210快速通道资格,用于治疗急性社交焦虑障碍(SAD)和其他焦虑相关疾病。此前,FDA已授予BNC210用于治疗创伤后应激障碍(PTSD)和其他创伤相关和应激相关疾病的快速通道资格。BNC210是一款α7烟碱乙酰胆碱受体(α7 nAChR)选择性负变构调制剂 ,具有快速起效、不会出现过度镇静和无药物相互作用等特点,可迅速吸收并在大约1小时内达到最大血药浓度。
3.创新ARi组合治疗特定前列腺癌Ⅲ期临床积极。拜耳与Orion公司开发的口服雄激素受体抑制剂(ARi)Nubeqa(darolutamide)治疗转移性激素敏感性前列腺癌(mHSPC)患者的Ⅲ期临床达到主要终点。在雄激素剥夺治疗联合多西他赛的基础上,Nubeqa显著延长患者的总生存期(OS),将出现癌症转移或死亡的风险降低59%。详细结果将在科学大会上公布。该药物此前已获FDA批准,用于治疗非转移性去势抵抗性前列腺癌。
4.反义寡核苷酸药物治疗癫痫临床积极。Stoke公司反义寡核苷酸(ASO)疗法STK-001治疗遗传性癫痫Dravet综合征的Ⅰ/Ⅱa期临床结果积极。在治疗第29天至第84天期间,STK-001单次给药(10 mg、20 mg、30 mg)或多次给药(20 mg),使患者癫痫发作频率与基线相比有所降低的患者比例达到70.6%(12/17),中位降低幅度范围为17%-37%。临床中未报告与STK-001相关安全性问题。STK-001此前已获FDA授予孤儿药资格。
5.GSK/Vir新冠中和抗体对Omicron毒株有效。葛兰素史克与Vir公司联合开发的中和抗体sotrovimab,在针对新的Omicron SARS-CoV-2突变毒株(B.1.1.529)的关键突变进行伪病毒测试的临床前数据显示出活性作用。两家公司正在进一步确定sotrovimab对所有Omicron突变的中和活性,并预计在2021年底之前提供预印本更新。迄今为止,sotrovimab或许是已被证实对世卫组织所列出的“受关注的病毒变体”均有效。
6.基因疗法AviadoBio公司完成A轮融资。AviadoBio公司完成8000万美元的A轮融资。AviadoBio公司先导AAV9载体基因疗法AVB-PGRN,旨在将一个表达颗粒蛋白前体的正常基因拷贝递送至大脑,以恢复颗粒蛋白前体的正常表达,以用于治疗额颞叶痴呆(FTD)患者。此轮融资将用于推进AVB-PGRN进入临床,并推进其处于临床前阶段的其他产品管线,包括治疗肌萎缩侧索硬化(ALS)的疗法。
7.安斯泰来联手Dyno开发新一代AAV基因疗法。安斯泰来联合Dyno Therapeutics将利用后者CaspidMap人工智能平台开发下一代AAV载体基因疗法,用于治疗骨骼肌和心肌疾病。根据协议,Dyno将设计新型AAV衣壳用于基因治疗,安斯泰来将负责候选基因疗法的临床前、临床以及商业化活动。Dyno将获得1800万美元的预付款,里程碑后付款和合作产品的特许权使用费。Dyno将从每种产品中获得潜在超过2.35亿美元的里程碑和特许权付款,协议总价值超过16亿美元。
医药热点
1.程英升任上海同济医院院长。同济大学附属同济医院日前召开干部大会,同济大学党委常委、组织部部长吴利瑞在会上宣布了同济大学党委的任免决定,任命程英升同志为同济大学附属同济医院院长。任命程黎明同志为同济大学医学与生命学部副主任,不再担任同济医院院长职务。
2.四川公立医院高质量发展方案出台。四川省日前印发《四川省推动公立医院高质量发展实施方案》,计划通过5年时间,积极争取国家公立医院高质量发展试点,探索开展省级试点,力争病例组合指数(CMI)值分别达到2、1.5左右,微创手术占比分别达到30%、25%左右,四级手术占比分别达到60%、40%左右,逐步提高医疗服务收入占医疗收入比例;县医院100%达到医疗服务能力基本标准、力争80%达到推荐标准。
3.2021年国家医保药品目录调整结果出炉。3日,国家医保局公布2021年国家医保药品目录调整结果,共计74种药品新增进入目录,11种药品被调出目录。调整后,国家医保药品目录内药品总数为2860种,将于2022年1月1日执行。此次有94种 (目录外67种,目录内27种)药品通过谈判成功纳入医保目录,总体成功率80.34%。目录外67种药品平均降价61.71%,最高降幅93.97%。其中,70万一针渤健SMA(脊髓性肌肉萎缩症)治疗药物诺西那生钠注射液纳入医保,阿尔茨海默病新药九期一降至296元。
评审动态
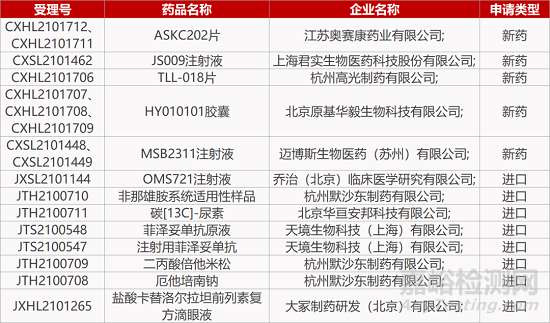
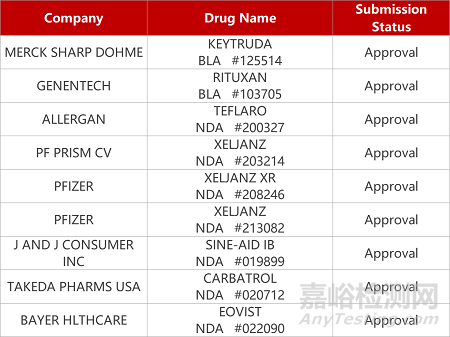

来源:药研发


