您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-11-22 11:20
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
抗肿瘤药物临床研发指导原则发布。CDE日前发布《以临床价值为导向的抗肿瘤药物临床研发指导原则》指出,‘对照药’是体现新药临床价值的基础;强调单臂试验适用于治疗危及生命且缺乏标准治疗的难治疾病或罕见疾病,并在早期探索性研究中初步显示突出疗效的单药治疗;鼓励研发单位开发针对儿童的剂型,尤其是低龄儿童,需考虑其吞咽能力及口味等,并建议研发单位在对其所开发的药物在肝功能/肾功能对PK的影响有所掌握的前提下,进行老年人群用药的临床开发,确保老年人群的安全性。
国内药讯
1.翰森「氟维司群注射液」获批上市。翰森制药氟维司群注射液获国家药监局批准上市。氟维司群是阿斯利康原研的一款雌激素受体(ER)下调剂,2002年4月获FDA批准上市,用于抗雌激素药物(如他莫昔芬)治疗后病情仍趋恶化的绝经后乳腺癌患者的治疗。该原研药2018年销售额达到峰值10.28亿美元;2020年销售额5.8亿美元。翰森制药为该品种国产第2款氟维司群注射液。
2.科伦PD-L1单抗治疗鼻咽癌报产。科伦药业PD-L1抑制剂泰特利单抗(A167)上市申请获CDE受理,拟用于既往接受过二线及以上化疗失败的复发或转移性鼻咽癌。A167是科伦首个进入申报阶段的创新项目。除鼻咽癌适应症外,科伦已与CDE就A167用于经典型霍奇金淋巴瘤(cHL)召开 pre-NDA 沟通交流会议,预计该新药很快会递交第2项适应症上市申请。目前A167也在临床试验中用于治疗三阴乳腺癌。
3.亘喜双靶点CAR-T获FDA孤儿药资格。FDA授予亘喜生物BCMA/CD19双靶点CAR-T产品GC012F孤儿药资格,用于治疗多发性骨髓瘤。公布在ASCO 2021年会上的I期临床长期随访数据显示,GC012F的客观缓解率高达 94.7%,而且最高剂量组全体患者均取得微小残留病灶阴性-严格意义上的完全缓解(MRD-sCR)。亘喜生物计划于明年上半年向FDA提交新药临床试验申请。
4.广州麓鹏乙肝新药上I期临床。广州麓鹏制药拥有全球知识产权的1类新药LP-128完成在健康受试者中开展的I期临床(CTR20212597)首例受试者给药。LP-128是一款口服HBsAg抑制剂,旨在降低乙肝患者HBsAg表达, 减少HBsAg包裹乙肝病毒空壳数量, 从而恢复机体对乙肝病毒免疫力,杀死乙肝病毒。该项研究将由南方医科大学南方医院许重远主任担任主要研究者。
5.维泰瑞隆RIP1抑制剂国内启动临床。维泰瑞隆1类新药SIR1-365登记启动一项Ⅰ期临床。此次为SIR1-365首次在中国启动临床,适应症为感染相关的全身性炎症反应综合征(SIRS)。SIR1-365是一款RIP1抑制剂,已在动物试验中显示出预防或减轻一系列疾病进展的潜力,包括多发性硬化(EAE模型)、阿尔茨海默病、肌萎缩性侧索硬化症、SIRS等。在美国,该新药此前已登记开展一项用于COVID-19重症患者治疗的Ⅰ期临床。
6.因明生物HPK1抑制剂在美获批临床。因明生物自主开发的HPK1小分子抑制剂PRJ1-3024获FDA批准,将在美国开展Ⅰ期临床试验。PRJ1-3024通过靶向HPK1来有效调控几类重要的免疫细胞,激活其协同抗肿瘤效应。该公司同时宣布眼科新药QA102在美国开展的针对干性年龄相关性黄斑变性的Ⅰ期临床试验已完成全部受试者给药,即将正式进入Ⅱ期临床试验阶段。
国际药讯
1.FDA允许成人接种增强针新冠疫苗。FDA扩展Moderna和辉瑞/BioNTech新冠疫苗的紧急使用授权,允许18岁以上的成人在完成Moderna或辉瑞/BioNTech新冠疫苗接种至少6个月后,接种一针新冠增强疫苗。完成强生新冠疫苗接种至少两个月的人群,也可以接种一针mRNA新冠增强疫苗。FDA认为接种一剂增强疫苗的获益超过心肌炎和心包炎的风险。
2.Keytruda治疗早期肾癌获FDA批准。FDA批准默沙东PD-1抑制剂Keytruda作为辅助疗法,用于治疗早期肾细胞癌术后患者。这也是首款获得FDA批准辅助治疗肾细胞癌的免疫疗法。在一项关键性Ⅲ期临床中,与安慰剂相比,Keytruda将这类患者疾病复发或死亡风险降低32%(HR=0.68 [95% CI,0.53-0.87];p=0.0010);使患者死亡风险降低46%。目前这一试验正在继续评估患者的总生存期。
3.软骨发育不全疗法获FDA加速批准。FDA加速批准BioMarin Pharmaceutical公司C型利钠肽(CNP)类似物Voxzogo(vosoritide)上市,用于治疗5岁以上软骨发育不全儿童患者。在一项Ⅲ期临床中,与安慰剂相比,vosoritide治疗的儿童平均每年多长1.57 cm。而且在开放标签研究中,这些患者的生长速率的改善得到维持。Voxzogo也是FDA批准治疗这一疾病的首款疗法。
4.吉利德丁肝创新疗法在美报BLA。吉利德已向FDA提交其首创抗病毒药物bulevirtide的生物制品许可申请(BLA),用于治疗伴有代偿性疾病的慢性丁型肝炎病毒(HDV)感染成人患者。在一项Ⅲ期试验中,2 mg bulevirtide治疗组24周后达到病毒学和生化联合应答的患者比例为36.7%(对照组为0%,p<0.001)。FDA此前已授予bulevitide突破性疗法认定和孤儿药资格,如果获批,它将成为FDA批准的治疗这一疾病的首款疗法。
5.mRNA癌症疫苗获快速通道资格。FDA授予BioNTech公司即用型治疗性mRNA疫苗BNT111快速通道资格,用于在晚期黑色素瘤治疗患者中,编码4种非突变的肿瘤相关抗原(NY-ESO-1、MAGE-A3、酪氨酸酶和TPTE),防止T细胞耗竭,提高晚期黑色素瘤患者的预后。目前,该疫苗正在Ⅱ期临床中评估与PD-1单抗Libtayo联用,治疗不可切除、难治/复发性晚期黑色素瘤患者的疗效和安全性。
6.诺和诺德收购RNAi疗法开发公司。诺和诺德与Dicerna Pharmaceuticals达成一项最终协议,将斥资约33亿美元收购Dicerna,以加快其RNAi药物研发并扩展RNAi技术的应用。Dicerna的技术平台通过对RNAi分子的修饰,能够将疗法有效递送到肝脏、中枢神经系统、肌肉等多个组织。两家公司此前已合作开发30多个临床候选药物,诺和诺德计划明年启动合作项目中获得的首个在研RNAi疗法的临床开发。
医药热点
1.2020年度中国医院排行榜出炉。复旦大学医院管理研究所发布了一年一度的复旦版《2020年中国医院综合排行榜》。位列排行榜前五名的医院分别为中国医学科学院北京协和医院、四川大学华西医院、中国人民解放军总医院、复旦大学附属中山医院和上海交通大学医学院附属瑞金医院。全国共有100家医院进入“复旦版中国医院综合排行榜”。
2.医生开具中药配方颗粒处方前应告知患者。国家卫健委、国家中医药管理局近日联合发布《关于规范医疗机构中药配方颗粒临床使用的通知》。通知要求,医生在开具中药配方颗粒处方前应当告知患者,保障患者的知情权、选择权。此外,医生开具中药处方时,原则上不得混用中药饮片与中药配方颗粒。
3.原料药领域反垄断指南出炉。11月18日上午,国家反垄断局正式挂牌成立。国家反垄断局与国家市场监督管理总局三里河办公区同楼,国家反垄断局与国家市场监管总局牌子分别悬挂于办公大楼两侧。甘霖担任首任国家反垄断局局长。同日,原料药领域反垄断指南出炉,部署预防和制止原料药领域垄断行为。《指南》共六章29条,明确反垄断监管的基本原则、思路和方法,细化垄断行为认定标准。
4. 全球首款注射疫苗机器人问世。加拿大初创公司Cobionix日前宣布研制出全球首款能注射疫苗的机器人Cobi。Cobi由一个带有药瓶储存区的机械臂和一个与患者互动的屏幕组成。人们通过触摸屏在系统中完成登记手续后,Cobi会拿起一个装有药剂的小瓶,并使用其激光雷达传感器识别患者的身体,然后通过压力喷射来注射疫苗。该机器人目前只是一个工作原型,可能需要两年或更长时间才能上市。
评审动态
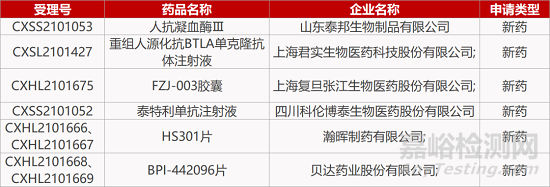
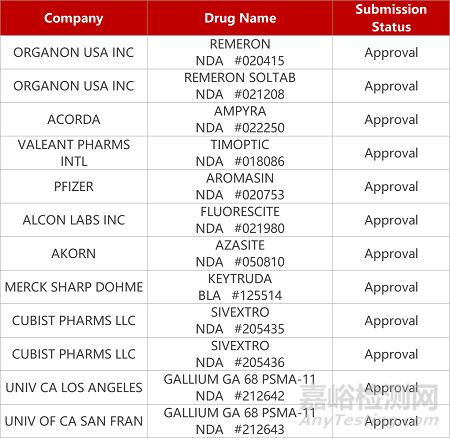

来源:药研发


