您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-07-04 18:33
近日,国家药监局批准了沛嘉医疗科技(苏州)有限公司的创新医疗器械经导管主动脉瓣系统,我们一起了解一下经导管主动脉瓣在临床前研发阶段做了哪些实验。
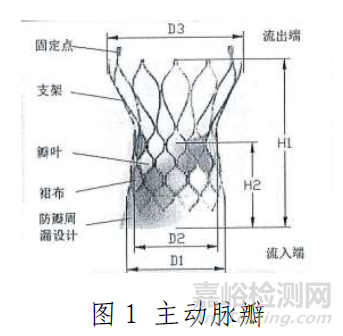
一、经导管主动脉瓣产品结构及组成
三、经导管主动脉瓣作用机理
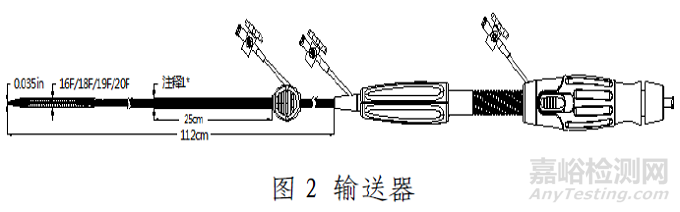
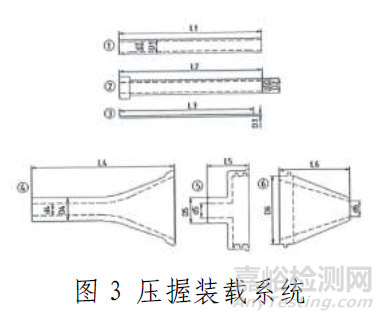
产品采用微创介入治疗方法,使用前通过压缩装载系统将主动脉瓣装载进输送器内;使用时在医学影像设备的监控下,通过建立好的血管通路将输送器推送至预期位置,操作输送器手柄完成瓣膜的释放,通过人工主动脉瓣支架的径向支撑力将患者自身的主动脉瓣膜植入并贴附在主动脉壁上,人工主动脉瓣替代患者的自身主动脉瓣,构建正常的血流通道。
四、经导管主动脉瓣研究与实验项目
(一)技术要求研究项目
2.产品性能评价
产品性能评价包括:主动脉瓣的裙布破裂力、瓣叶拉伸强度、瓣叶破裂力、外观、主动脉瓣基本尺寸、主动脉瓣支架厚度、主动脉瓣瓣叶厚度、径向支撑力、慢性向外力、支架相变点Af、主动脉瓣轴向短缩率、主动脉瓣抗挤压性、支架腐蚀敏感性、支架和瓣叶连接强度、支架和裙布连接强度、瓣叶和裙布连接强度、主动脉瓣脉动流性能、主动脉瓣开合状态、植入物抗位移性能、主动脉瓣静态前向流性、主动脉瓣稳态泄露性能、主动脉瓣耐久性能、支架疲劳性能、主动脉瓣局部抗挤压性、热皱缩温度、孔隙率、渗漏量和长度变化率。输送器的外观、尺寸、断裂力、导引导丝畅通性、连接件(座)、无泄漏、耐腐蚀性、止血性能和水合性。压握装载系统的外观和尺寸。主动脉瓣系统的压握装载性能、系统排空性、系统柔顺性、系统推送力、系统追踪性、系统释放准确性、系统释放时间、系统可回收性、系统回收后主动脉瓣性能、输送器回撤性能、产品磁共振兼容性、射线可探测性、系统释放扭矩、扭转性能和主动脉瓣与输送器连接强度等性能进行了验证。
(二)生物相容性
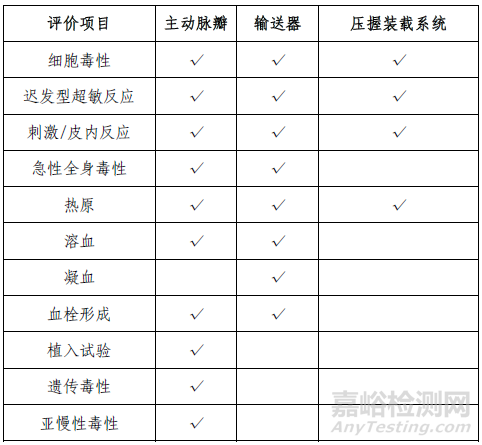
该产品包括主动脉瓣、输送器和压握装载系统三个部分。其中瓣膜为植入器械,与循环血液长期接触;输送器为外部介入器械,与循环血液短期接触;压握装载系统与人体间接接触。申请人按照GB/T 16886 系列标准对所有部件分别进行了生物相容性评价,产品的生物相容性风险可接受,具体评价项目详见表3。
(三)生物安全性
该产品的瓣膜部分采用了牛心包。申请人从原材料选取、原材料获取、原材料和供应商管控、生产过程管控、产品处理工艺方法控制、质量体系保证等方面进行了论述,并参照标准GB/T 16886.20 和动物源性医疗器械注册技术审查指导原则等要求对瓣膜的抗钙化,免疫原和病毒灭活的性能进行了验证,结果符合要求,相关生物安全性风险可控。
(四)灭菌
该产品包括主动脉瓣、输送器和压握装载系统三个部分。其中主动脉瓣部分采用戊二醛液体化学灭菌方法,其余的部件均采用环氧乙烷灭菌,无菌状态提供。申请人提供了灭菌过程确认报告,保证10-6 无菌水平。输送器环氧乙烷残留量不应大于10μg/g,压握装载系统环氧乙烷残留量不应大于4mg/套。输送器和压握装载系统的ECH 残留量不应大于9mg/套。
(五)产品有效期和包装
该产品包括主动脉瓣、输送器和压握装载系统三个部分。产品有效期均为2 年。申请人提供了货架有效期验证报告,包括产品稳定性、包装完整性和运输模拟验证。
(六)动物研究
申请人开展了大动物实验研究以验证产品使用性能及安全性。评价指标包括有效性指标(瓣膜及输送系统的急性性能,瓣膜的短期、中期和长期血液动力学性能等)和安全性指标(包括瓣膜的生物学反应等)。动物实验结果表明,产品达到预期设计要求。

来源:嘉峪检测网


