您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-03-04 09:13
牵张成骨是治疗复杂骨缺损的有效方法,新骨形成及钙化不良是该技术临床应用中亟待解决的问题。本研究将高纯镁棒作为髓内导向器用于大鼠股骨牵张成骨模型,结果表明随着高纯镁棒的逐渐降解,镁离子可以有效地促进新生骨钙化。进一步RNA-seq和生信分析发现该过程可能是通过镁离子调节Ptch蛋白激活Hedgehog-alternative Wnt复合信号通路来实现的。
01、研究内容简介
骨缺损是由于创伤、感染、肿瘤、畸形等造成的常见结局,临床治疗非常困难。牵张成骨技术自上世纪60年代应用于骨科临床,取得了良好的临床效果。牵张成骨技术通过给活体组织持续、稳定的缓慢牵伸力,刺激或激活组织细胞的再生和活跃生长, 其生长方式类似胎儿组织。牵张成骨技术目前应用越来越广泛,但一个共性问题是新骨形成钙化缓慢、薄弱,以至于带支架时间长,再骨折、感染、关节僵硬等并发症增多。这些都导致治疗周期延长,给患者的生活工作带来了极大的不便,增加了经济和精神负担,限制了牵张成骨技术的临床应用。因此,在牵张成骨过程中提高新骨形成和钙化的速度,缩短带架时间是临床亟待解决的问题。
医用可降解镁金属的成骨作用和机制研究是近年来的研究热点。既往研究发现各种形式的镁金属在体内外均有良好的成骨作用。镁有良好的成骨效果,那么能否利用镁来促进牵张成骨新骨形成钙化呢?由于牵张成骨是一种特殊状态下的新骨形成和钙化,镁能否应用于牵张成骨中,对于这种特殊状态的新骨形成钙化是否有促进作用、其机制如何,之前国内外仍是研究空白。课题组在近期研究中发现高纯镁棒可以通过VHL /HIF-1α/ VEGF信号通路促进牵张成骨中新生血管生成达到促进新生骨钙化过程。
尽管在先前的研究中我们发现了高纯镁棒通过激活VHL /HIF-1α/ VEGF信号通路增强了牵张成骨新生骨钙化,但其机制研究局限于血管生成,上游的机制仍不清楚。针对这一问题,课题组在之前的研究的基础上进行了镁对于牵张成骨作用及机制的一系列研究。在本研究中课题组将高纯镁棒作为髓内导向器用于大鼠股骨牵张成骨模型,用不锈钢组和空白组作为对照(Fig.1)。
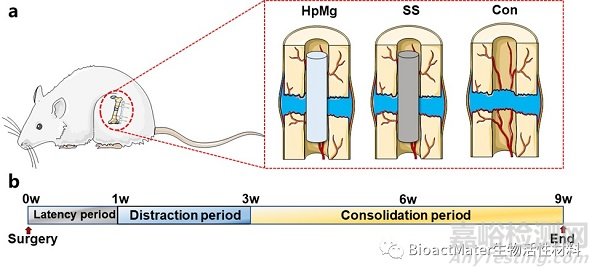
Fig.1. a: The grouping of rat femur DO model. b: Timeline for distraction protocol.
我们对术后第3、6、9周组织进行X线片、micro-CT检测观察,发现高纯镁组显著加快成骨钙化速度(Fig.2)。
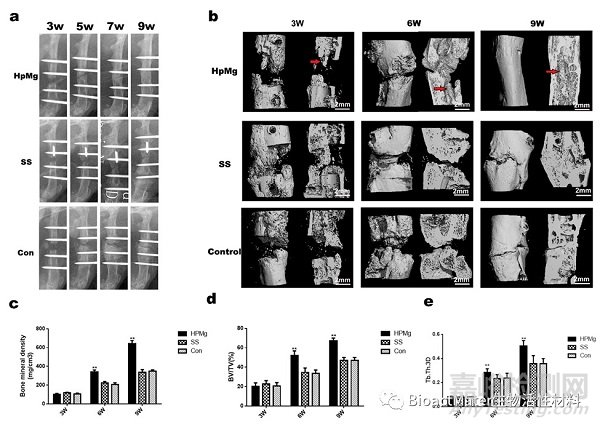
Fig.2. Hp Mg accelerated bone consolidation during distraction osteogenesis in rats. a:X-ray images of the distraction regenerate at 3,5,7 and 9 weeks after distraction. b: Representative 3D micro-CT images of the distraction zone after surgery 3,6 and 9 weeks. c, d, e: Quantitative analysis of micro-CT data showed higher values of BMD, BV/TV and Tb.Th in the Hp Mg group at consolidation phase (**p < 0.01).
相应的组织学观察也显示在术后第9周高纯镁组已基本完成钙化过程,明显优于不锈钢组和空白组(Fig3f,g)。力学检测进一步显示出高纯镁组有更好的力学性能(Fig3d,e)。这些结果都表明,在牵张的同时,随着高纯镁棒的逐渐降解,可以有效地促进新生骨成骨钙化。
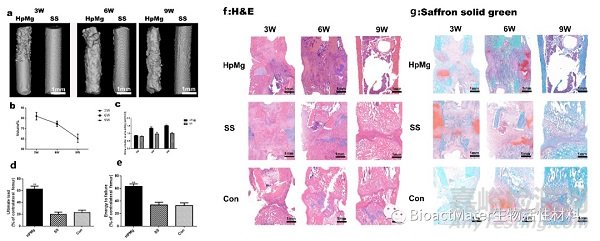
Fig.3. a: In vivo 3D micro-CT images of the Hp Mg and SS pins. b: Volume change of intramedullary Hp Mg pins. c: Bone volume surrounding Hp Mg and SS pins (**p < 0.01). d, e: Mechanical tests (ultimate load and energy to failure) of the distracted femur. The values were normalized to the corresponding contralateral normal femur (**p < 0.01). f:H&E staining Hp Mg group enhanced bone consolidation in comparison with the SS and control group. g: In Saffron solid green, at 6 and 9weeks chondrocytes cartilage were evident in the SS and control groups compared to the Hp Mg group.
镁对于牵张新生骨的形成钙化的促进机制是什么?是否与前期研究的VHL /HIF-1α/ VEGF信号通路有关呢?为此,课题组于钙化中期取新生骨组织进行高通量转录组测序(RNA-seq),与不锈钢组和空白组比较得到差异表达基因,并对差异表达基因进行了KEGG通路富集分析。KEGG通路富集结果显示,Wnt通路在所有通路中排名第二并且在成骨相关通路中富集最明显。VHL /HIF-1α/ VEGF信号通路虽然也有富集,但排名比较靠后(Fig.4)。该研究结果首次揭示了镁促进牵张成骨的主要信号通路与Wnt通路相关。
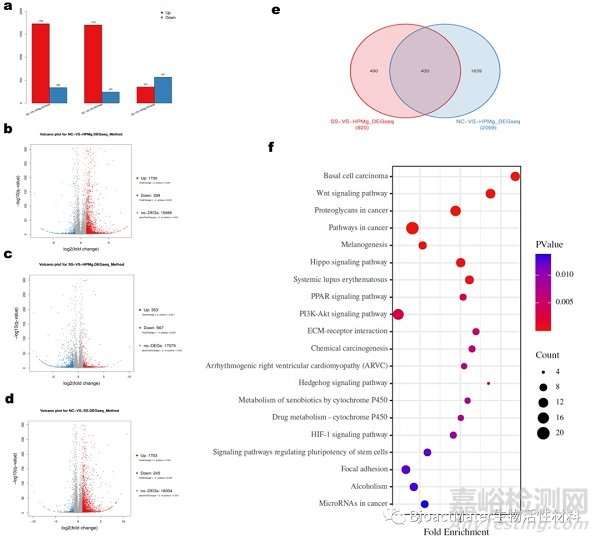
Fig.4. a: Summary of DEGs. Red color represents up-regulated DEGs. Blue color represents down-regulated DEGs. b, c, d: Volcano plot. Red points represent up-regulated DEGs. Blue points represent down-regulated DEGs. Gray points represent non-DEGs. e: Venn diagram of DEGs. f: Bubble chart showing top 20 enriched pathways in the KEGG.
进一步对于Wnt通路关键基因研究中,课题组发现经典Wnt 通路的Wnt 分子及其下游的β-catenin未差异表达,而近期研究发现的Alternative Wnt信号通路完全被激活。2015年Park HW等在Cell上发表的研究显示:Alternative Wnt信号通路通过Wnt5b蛋白刺激膜蛋白Fzd,进一步激活YAP/TAZ并入核促进核内TEAD高表达,从而促进Runx2等成骨基因表达而促进成骨。我们针对Wnt通路关键基因进行了qPCR、WesternBlot和免疫组化验证。结果验证高纯镁通过Alternative Wnt通路,而不是经典Wnt通路,促进牵张成骨钙化。
Wnt5b作为激活Alternative Wnt通路的上游配体,在骨生长及骨折愈合过程中有重要作用,尤其在软骨内成骨中有重要作用。我们前期研究也发现Wnt5b有高表达。因此,针对Wnt5b我们通过生物信息学进一步探索上游基因并与前期RNA-Seq结果比对,发现其上游基因中Gli1和Gli2有高表达(Fig.5a)。Gli1和Gli2都是Hedgehog通路的关键核转录因子。Hedgehog信号通路是一条保守且重要的信号通路,参与体内多种生物代谢过程中。研究显示Hedgehog信号通路参与骨形成,代谢以及骨折愈合等代谢过程,抑制Hedgehog通路会导致骨折不愈合或延迟愈合。当存在Hedgehog蛋白时,Hedgehog蛋白与Patched(Ptch)受体结合,阻断Ptch对Smoothed(Smo)受体的抑制,促使Smo受体发生磷酸化修饰,活化的Smo受体抑制PKA的活性,从而抑制了对Gli蛋白的裂解,使核转录因子Gli家族蛋白完整的在核内发挥作用促进成骨钙化基因表达,其中Gli1 和Gli2在蛋白水平作用相似, 均可以促进Wnt5b表达(Fig.5b)。因此,我们针对Hedgehog通路关键基因进行了qPCR、WesternBlot和免疫组化验证。结果验证高纯镁通过Hedgehog-Alternative Wnt通路促进牵张成骨钙化。
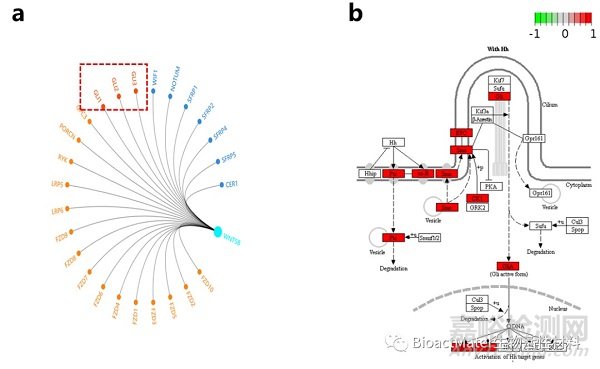
Fig.5.a: Wnt5b gene radar analysis. b: RNA-seq results enrichment map of Hedgehog pathway.
针对这些Hedgehog通路上游基因我们比对了RNA Seq结果并做了进一步的qPCR及Western Blot验证。结果发现膜表面受体Smo,Ptch均有高表达,而三种Hedgehog蛋白基因均未高表达(Fig.5b)。关于膜蛋白Ptch的研究中,Hitzenberger M等通过分子动力学实验发现,Ca2+、Zn2+作为二价金属离子在Hedgehog蛋白调控Ptch过程中发挥了重要作用。因此可以假设同样作为二价金属离子的镁离子通过某种机制取代Hedgehog蛋白的二价金属离子结构与Ptch结合,改变其蛋白构象和功能,减少对Smo的抑制,进一步激活Hedgehog通路。因此,我们以钠离子作为对照通过分子动力学模拟镁离子对Ptch蛋白构象变化。结果显示结果表明,Mg2 +与Ptch蛋白表面的酸性氨基酸残基Glu592,Asp803和Asp804形成配位键,从而稳定了562-595和794-803区的结构。镁离子与其他酸性残基Glu191,Glu188,Glu205,Asp782,Asp361,Asp105和Asp787形成配位键,这在稳定Ptch蛋白结构中也起着重要作用(Fig.6a)。
至此,结合全部前期试验结果,我们提出镁促进牵张成骨新生骨的成骨钙化作用的机制假说。其可能的机制是:镁通过调控膜受体Ptch,减少对膜受体Smo的抑制作用,进而激活Hedgehog通路,而该通路的Gli1和Gli2转录表达Wnt5b激活Alternative Wnt通路,通过YAP/TAZ蛋白转录生成Runx2等成骨相关蛋白表达,从而促进牵张成骨中新生骨的成骨钙化(Fig.6b)。通过上述实验,我们明确镁在牵张成骨过程中促进成骨钙化的具体调控机制,为医用可降解镁金属髓内导向这一创新方法克服临床上牵张成骨关键难点提供理论依据。
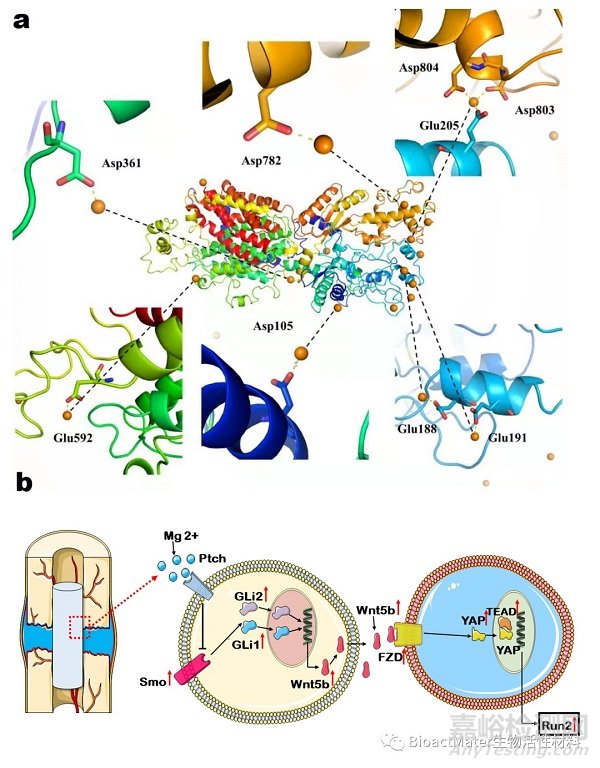
Fig.6. a: Molecular dynamics simulation results. Mg2+ forms a coordination bond with Glu592, Asp803, Asp804, Glu191, Glu188, Glu205, Asp782, Asp361, Asp105, and Asp787. b: Schematic diagram showing diffusion of implant-derived Mg2+ enhances bone consolidation in distraction osteogenesis via regulating Ptch protein activating Hedgehog-alternative Wnt signaling.
02、通讯作者简介
第一作者:木沙·哈木山
上海交通大学附属第六人民医院,骨科,2020级博士研究生,研究方向为镁基材料在骨科应用以及骨关节感染免疫机制。
通讯作者:韩培
上海交通大学附属第六人民医院,骨科,主任医师,博士,硕导。长期从事创伤骨科与修复重建外科的临床工作,作为组长负责骨关节与软组织感染专业组临床工作,作为Co-PI共同负责骨研所骨内植物感染实验平台科研工作。主要研究方向生物医用镁金属材料的医工交叉研究,骨关节感染的临床基础研究。主持国家、省部级课题5项,先后以第一作者/共同第一作者/通讯作者在Biomaterials、Acta Biomaterialia等杂志发表SCI论文近20篇。研究获得上海市科技进步一等奖和华夏医学科技进步一等奖。
沈灏
上海交通大学附属第六人民医院,骨科,主任医师,博士,博导,上海交通大学附属第六人民医院骨科副主任,上海市四肢显微研究所骨关节内植物感染实验平台负责人。长期从事关节外科的临床和研究工作。主要从事关节置换和骨科感染的临床和基础研究,骨科内植物感染的发病机制和抗菌生物材料的研发和转化研究。主持国家级及省部级课题5项,完成2次成果鉴定,多次获得国家级及省部级医学科技奖励。先后以第一作者/共同第一作者/通讯作者在ACS Nano、Acta Biomaterialia、The Journal of infection等杂志发表SCI论文近50余篇,主编和参编专著8部。
张小农
上海交通大学材料科学与工程学院博士生导师,主持和参加国家重点研发专项、国家“863”高技术计划、国家自然科学基金、上海市纳米专项基金等科研项目30余项,发表学术论文150多篇(其中2篇论文入选ESI高被引论文),参编著作3部,授权发明专利20多项,获得国家自然科学二等奖 、上海市科技进步一等奖和二等奖各一次。
03、资助信息
该研究得到了国家自然科学基金(81974325,81702183)和上海市科委基金(18ZR1428700, 19441903000)等项目的支持。
04、原文信息
Musha Hamushan #, Weijie Cai , Yubo Zhang, Zun Ren, Jiafei Du, Shaoxiang Zhang, Changli Zhao, Pengfei Cheng, Xiaonong Zhang*, Hao Shen*, Pei Han *
High-purity magnesium pin enhances bone consolidation in distraction osteogenesis via regulating Ptch protein activating Hedgehog-alternative Wnt signaling.
Bioactive Materials 2020;6(6):1563-1574

来源:BioactMater生物活性材料


