您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2019-11-08 09:12
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
「本文共:16条资讯,阅读时长约:3分钟 」
今日头条
百奥泰阿达木单抗获批上市。百奥泰阿达木单抗注射液(商品名:格乐立)获国家药监局批准上市,适应症为强直性脊柱炎、类风湿关节炎和银屑病等自身免疫性疾病。阿达木单抗是抗肿瘤坏死因子(TNF)生物制剂,该药原研药(修美乐)由艾伯维研制,目前已在全球90多个国家/地区上市,获批适应症包括类风湿关节炎、强直性脊柱炎、银屑病等14个。2010年,修美乐已获批进口中国。目前国内药企除了百奥泰之外,海正药业、信达生物、复宏汉霖已提交了该品种的上市申请。2018年修美乐的全球销售额约为204.85亿美元。
国内药讯
1.齐鲁2款重磅仿制药获批。齐鲁制药注射用紫杉醇(白蛋白结合型)和他达拉非片获国家药监局批准上市,这两款药均视同通过仿制药一致性评价。白蛋白紫杉醇原研产品(Abraxane)由Abraxis BioScience开发,目前已获批的适应症包括乳腺癌、肺癌和胰腺癌。Abraxane于2008年6月获批进口中国。齐鲁是继石药、恒瑞之后国内第3家获得该品种仿制药上市资格的企业。他达拉非是礼来开发的一款选择性、可逆性磷酸二酯酶5(PDE5)抑制剂,用于治疗男性勃起障碍(ED)。该药原研药2004年11月已获批进口中国。齐鲁是继长春海悦、正大天晴之后第3家获得该品种仿制药上市资格的国内企业。
2.以岭药业盐酸环丙沙星片通过一致性评价。以岭药业盐酸环丙沙星片通过一致性评价并获《药品补充申请批件》。盐酸环丙沙星片为抗感染类药物,用于治疗或预防确诊或高度怀疑的敏感菌感染。该药原研药由拜耳研发,1987年1月在德国获批上市,商品名为Ciprobay。目前国内共有108个盐酸环丙沙星片生产批文,以岭药业是该品种首家通过一致性评价的企业。
3.景峰医药吉西他滨一致性评价申请获受理。景峰医药旗下海南锦瑞注射用盐酸吉西他滨的一致性评价补充申请获国家药监局受理。注射用盐酸吉西他滨主要适用于治疗局部晚期/转移的非小细胞肺癌或胰腺癌,也可与紫杉醇联合,用于治疗经辅助/新辅助化疗后复发、不能切除的、局部复发/转移性乳腺癌。根据IMS数据显示,吉西他滨2017年和2018年的全球销售额分别为4.95亿美元和4.73亿美元,中国销售额分别为1.80亿美元和1.84亿美元。
4.基石药业将更新CS1001-201研究试验数据。基石药业将在2019年美国血液学会(ASH)大会上,更新其II期临床CS1001-201研究的试验数据。CS1001-201试验评估CS1001单药治疗复发或难治性结外自然杀伤细胞/T细胞淋巴瘤的疗效。初步结果显示,在22例可评估患者中,经研究者评估的客观缓解率为40.9%。7例(31.8%)患者达完全缓解且缓解可持续。2例患者达部分缓解,另有1例患者在假性进展后达到部分缓解。缓解持续时间(DoR)范围为0.03+到8.61+个月,中位缓解持续时间尚未达到。至数据截止时间,IRRC评估尚未进行。详细更新数据将在2019 ASH大会期间呈现。
5.广生堂1类创新药GST-HG141获批临床。广生堂研发的乙肝核心蛋白抑制剂GST-HG141获国家药监局临床批件,拟开发适应症为慢性乙型肝炎。目前,乙肝治疗药物主要有干扰素和核苷(酸)类似物两类,均无法有效清除乙肝病毒实现以停药为目的的功能性治愈。全球范围内尚无批准任何药物或方案用于乙肝治愈。GST-HG141是全新靶点的新型抗乙肝病毒1类新药,该项目是广生堂乙肝功能性治愈计划的最重要组成药物之一,目前全球尚无该靶点药物获批上市。
6.复星医药ORIN1001片临床申请获受理。复星医药旗下在研靶向药ORIN1001片临床试验申请获国家药监局受理。ORIN1001片为复星集团自主研发的具有新酶型靶点、新作用机制和新化学结构类型的首创(First-in-Class)小分子药物,用于晚期实体瘤治疗,其首个探索的适应症为复发性、难治性、转移性乳腺癌。目前该新药用于晚期实体瘤治疗于美国处于I期临床阶段,其用于复发性、难治性、转移性乳腺癌(包括三阴乳腺癌)已获FDA授予快速通道资格。全球范围内尚无与该新药同类型产品获批上市。
国际药讯
1.赛诺菲/再生元PD-1抑制剂Ⅲ期临床数据积极。再生元与赛诺菲共同开发的PD-1抑制剂Libtayo(cemiplimab),在用于单药一线治疗PD-L1表达水平≥50%的晚期非小细胞肺癌(NSCLC)患者的Ⅲ期临床中获积极结果。中期分析显示,与单独化疗相比,接受Libtayo治疗的患者达到42%的ORR,与正在成为某些肺癌患者标准护理疗法的Keytruda在以前Ⅲ期试验中达到的ORR(39%)非常相近,化疗组中的这一数据为22%。Libtayo在美国、欧盟、加拿大和巴西已获批用于治疗转移性皮肤鳞状细胞癌(CSCC)或不能接受治愈性手术或放疗的局部晚期CSCC患者。
2.吉利德两款HIV新药Ⅲ期扩展期研究获积极结果。吉利德宣布,其作为暴露前预防(PrEP)疗法降低男性和变性女性HIV感染风险的Descovy,以及用于治疗初次感染HIV患者的Biktarvy,分别在Ⅲ期临床(DISCOVER、1489和1490)的扩展期研究中,进一步证实了它们的长期有效性和安全性。DISCOVER试验96周的结果延续了Descovy与已获批的PrEP疗法Truvada此前取得的非劣效性结果,Descovy组HIV感染几率平均为每年0.16/100人,而Truvada组为每年0.30/100人。同时,Descovy在骨密度和肾功能方面也显示出长期的安全性。其详细数据以及144周Ⅲ期试验(1489和1490)的研究结果均在第17届欧洲艾滋病会议(EACS)上公布。
3.武田登革热疫苗Ⅲ期临床成功。武田登革热疫苗TAK-003在大规模Ⅲ期临床Tides中获积极结果。2万名年龄在4至16岁的受试者接受TAK-003或安慰剂的治疗,研究人员追踪了疫苗组61例登革热病例,以及安慰剂组149例患者的试验结果,其发布在《新英格兰医学杂志》上的试验结果显示,接受两种剂量TAK-003的患者中,疫苗的有效率达到80.2%。而且TAK-003对不同血清型的登革热的疗效各不相同:对1型登革热的有效率为73.7%;对2型登革热的有效率为97.7%;对3型登革热的有效率为62.6%等。此外TAK-003预防登革热感染的有效率达到74.9%。
4.Constellation公司BET抑制剂Ⅱ期临床数据积极。Constellation 公司选择性BET抑制剂CPI-0610在治疗骨髓纤维化患者的Ⅱ期临床MANIFEST中获积极结果。在此前对ruxolitinib产生耐药或不耐受的患者的第1/2队列中,患者接受CPI-0610,或CPI-0610+ruxolitinib的治疗。截至2019年6月27日,患者的脾脏体积缩小,血红蛋白含量有所增加,骨髓纤维化综合评分和疾病症状也均得到改善。在此前未接受过JAK抑制剂治疗的患者的第3队列中。患者接受CPI-0610+ruxolitinib的治疗。数据显示,4例可评估患者的脾脏体积至少缩小35%,疾病症状综合评分降低50%,达主要疗效终点。详细结果将于美国血液学会年会上公布。
5.渤健获得三星Bioepis两款眼科生物仿制药权益。渤健与三星Bioepis达成一项交易,获得后者两种眼科生物仿制药(SB11、SB15)在美国、加拿大等全球主要市场商业化的独家权利。SB11原研药为罗氏/诺华的雷珠单抗,SB15原研药为再生元的阿柏西普,两者均为抗血管内皮生长因子疗法,治疗包括新生血管(湿性)年龄相关性黄斑变性、视网膜静脉阻塞后黄斑水肿、糖尿病性黄斑水肿(DME)和DME伴有糖尿病性视网膜病变。根据协议,三星Bioepis将获1亿美元的预付款、可高达2.1亿美元的额外开发、监管和基于销售的里程碑付款;三星Bioepis将负责开发,生产提供这两种产品。
6.MD安德森癌症中心与Artios Pharma达成合作协议。德克萨斯大学MD安德森癌症中心联合Artios Pharma和ShangPharma Innovation宣布:Artios获得MD Anderson和ShangPharma共同开发的小分子ATR抑制剂的授权许可。根据协议,Artios拥有全球范围内独家研发、生产和商业化该ATR抑制剂的权利。Artios计划于2020年下半年递交候选化合物的新药研究申请。ATR是DNA双链断裂修复和复制应激中的重要信号蛋白。通过抑制ATR,可以通过称为合成致死性的概念选择性杀死具有ATM缺陷的肿瘤。目前已在多种肿瘤类型中鉴定出高水平的ATM突变和蛋白质损失。
医药热点
1.北大肿瘤医院I期临床病区新病房启用。北京大学肿瘤医院I期临床病区新病房正式启用。目前,I期临床病区有专职医生6人,研究护士团队18人,专职实验室分析人员4人。全体医护人员均接受过相关培训。这也是全国仅有的设立专职医护团队的临床试验中心。据介绍,北京大学肿瘤医院I期临床病区是在2014年成立的,原来只有三张固定病床。新病区创立后,固定床位扩展到15张。根据国家药监局药品评审中心网站登记数据,该医院2016年到2018年承接的I期临床试验项目数居于全国第一位。
2.全国首例网络个人大病求助纠纷案一审宣判:全额返还筹款。11月6日,全国首例因网络个人大病求助引发的纠纷在北京朝阳法院一审宣判,法院认定筹款发起人莫先生隐瞒名下财产和其他社会救助,违反约定用途将筹集款项挪作他用,构成违约,一审判令莫先生全额返还筹款153136元并支付相应利息。法院同时向民政部、北京水滴互保科技有限公司发送司法建议,建议推进相关立法、加强行业自律,建立网络筹集资金分账管理及公示制度、第三方托管监督制度、医疗机构资金双向流转机制等,切实加强爱心筹款的资金监督管理和使用。
3.学生体质健康将与中考挂钩。教育部在11月5日的新闻通气会上透露,学生参加体育活动、体质健康状况和运动技能等级,或将纳入学生综合素质评价体系。教育部正在探索基于初中学业水平考试成绩结合综合素质评价的招录模式。据介绍,我国青少年形态发育水平继续提高,肺活量指标稳步上升,力量和耐力素质指标稳中向好。2018年,全国学生体质达标测试合格率为91.91%,优良率为30.57%。2016年~2018年,全国学生体质健康状况总体呈现逐步提升趋势,不及格率由12.0%下降至11.3%,良好率由21.9%上升至24.1%,优秀率由4.6%上升至6.2%。
股市资讯
.
【恒瑞医药】引进德国Novaliq公司用于治疗干眼症的药物CyclASol™(0.1%环孢素A制剂)和NOV03(全氟己基辛烷),恒瑞将获得这两个产品在中国的临床开发、生产和市场销售的独家权利。
【九强生物】第三期限制性股票激励计划第一个解除限售期的解除限售条件已成就,2名激励对象可解除限售的限制性股票数量为50.44万股(总股本0.1005%)。其中,实际解除限售并可上市流通股份数量为26.80万股(总股本0.0534%)。
【贝达药业】(1)提名丁列明、YI SHI、万江、JIABING WANG、余治华、LI MAO为第三届董事会非独立董事候选人,提名JIANGNAN CAI(蔡江南)、汪炜、赵骏为第三届董事会独立董事候选人。(2)提名张洋南、吴颢为公司第三届监事会非职工代表监事候选人。
审评动向
1. CDE最新受理情况(11月07日)
2. FDA最新获批情况(北美11月06日)
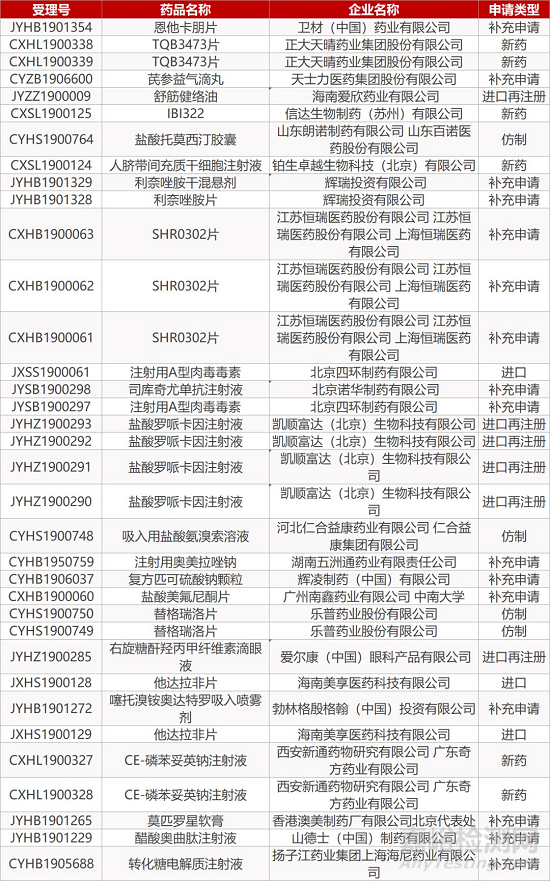
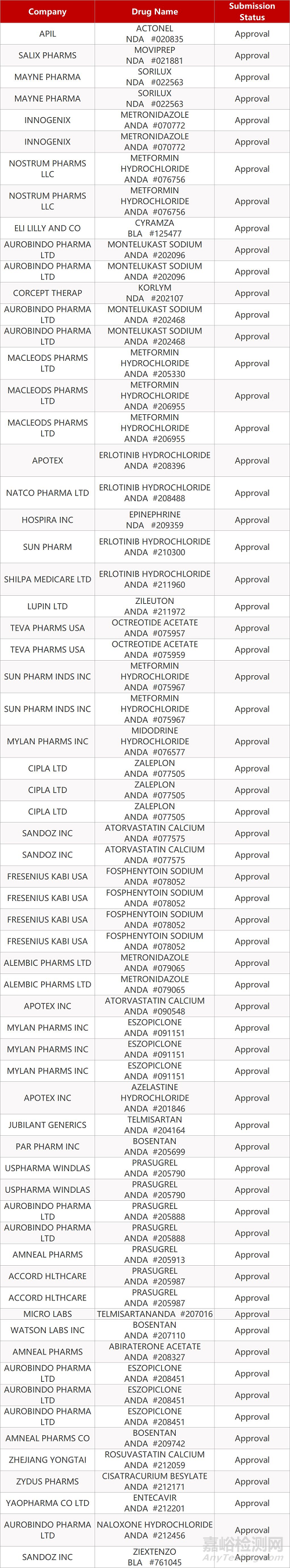

来源:药研发


