您当前的位置:检测资讯 > 法规标准
嘉峪检测网 2017-04-19 16:05
兽药残留(animal drug residues)是指给动物使用药物后蓄积或贮存在细胞、组织或器官内的药物原形、代谢产物和药物杂质。近10年来,水产品中兽药残留问题引起了社会的广泛关注,也经历了贸易壁垒的多发期,直接影响着中国水产行业的转型和升级。在水产品养殖过程中,非法使用违禁药物、不遵守休药期、生物体代谢差异和不合理用药等都有可能导致兽药残留超标。
兽药残留分析的检测手段多样,酶联免疫试剂盒、胶体金免疫试纸条和荧光试纸条等快速检测产品能够实现高通量、快速筛选,其灵敏度、准确性和时效性正在不断优化和革新;气相色谱仪、液相色谱仪、气相色谱-质谱仪、液相色谱-串联质谱仪和高分辨质谱等仪器是实验室常用的分析设备,具有定量准确、准确度更高等优点,特别是具有高灵敏度、高分辨率的质谱仪,是进行阳性样品确证分析的首选。
目前,兽药残留测定是进行水产品质量安全监控的主要手段,氯霉素、孔雀石绿和硝基呋喃等禁用药物是药物残留监控的重点,为了确保水产品的质量安全,氟甲砜霉素、甲砜霉素、磺胺类和喹诺酮类等限用药物也早已纳入监控工作。但是由于各个实验室间的检验能力良莠不齐,有时会对检验数据的可靠性存在质疑,影响了监控工作的权威性,因此监管部门将能力验证作为检验实验室能力水平的一个主要的方式。
能力验证(proficiency testing)是通过实验室间比对,按照预先制定的准则来判定实验室能力的活动。能力验证是实验室认可机构加入和维持国际相互承认协议(mutual recognition agreement, MRA)的必要条件之一,也是实验室进行自我评价的手段[2]。中国农产品能力验证考核始于2003年,虽然起步较晚,但是实验室能力验证的方法标准均参考国外权威机构的标准制定,10多年来技术能力取得了长足的进步。能力验证在检测实验室的覆盖率逐年增加,监管部门通过组织能力验证,可以了解实验室是否有能力胜任所从事的监控工作;实验室通过参加能力验证,了解自身能力,将其作为内部质量控制的补充措施,满足持续改进的要求。
在实际检测工作中,同一个检测项目可以从多个检测方法标准中选择,这些技术标准主要在前处理方法和仪器设备的选择上存在差异,需要根据检测的目的和要求进行选择。为了解决水产品药物残留检测中由于标准方法差异和操作不熟练出现检验结果不准确的问题,本文综述了水产品质量安全监控工作中关注较多的兽药残留测定检测技术标准,对各种检测方法的差异、适用性和灵敏度等进行了介绍,并详细说明了标准操作中应该注意的问题和解决办法等,最后提出做好能力验证工作的建议,旨在为提高实验室的水产品兽药残留检测能力和能力验证整体水平提供借鉴。
1 水产品兽药残留标准检测方法概述
1.1 硝基呋喃类代谢物
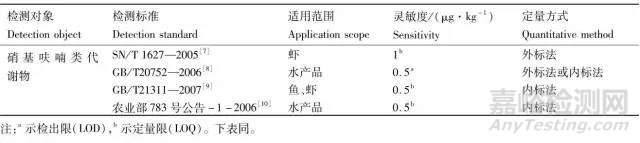
硝基呋喃类药物是一类化学合成的广谱抗菌药物,常见的有呋喃唑酮(furazolidone,FZD)、呋喃西林(nitrofurazone,NFZ)、呋喃妥因(nitrofurantion,NFT)和呋喃它酮(furaltadone,FTD),曾广泛用于畜禽、水产等动物传染病的预防与治疗。硝基呋喃类药物原药及其代谢产物具有一定的毒性,有致畸、致突变和致癌的危险[3]。出于安全性考虑,自1993年开始,欧盟、美国等发达国家和地区先后颁布了禁止使用该类兽药的禁令[4-5]。中国于2002年颁布的农业部第193号公告《食品动物禁用的兽药及其它化合物清单》,明确禁止使用硝基呋喃类广谱抗菌药物[6]。但是由于硝基呋喃类药物价格低廉、疗效好,在水产养殖中仍存在违禁使用的现象,在近几年开展的水产品风险隐患排查工作中屡有检出。硝基呋喃类药物在生物体内代谢迅速,很难检测到原药,因此标准方法都是对其代谢产物进行测定,表1中列出了当前适用于水产品中硝基呋喃代谢物残留测定的方法标准,均采用液相色谱-串联质谱法(LC-MS/MS)进行测定,其中农业部783号公告-1-2006是中国水产品质量安全监控的推荐方法,该方法的适用范围广、定量准确、灵敏度高,是常用的检测方法。
表1 水产品中硝基呋喃代谢物残留测定方法标准
Tab.1 Detection standard of nitrofuran metabolic residues in aquatic products
1.2 孔雀石绿
孔雀石绿(malachite green, MG)作为一种三苯甲烷类染料,曾广泛用作水产养殖业中的驱虫剂和杀菌剂,以防治鱼类水霉病、鳃霉病、及小瓜虫病等,是一类抗菌效力较强的药用染料。然而,MG不仅在生物体内有明显蓄积现象,且迅速被代谢成隐色孔雀石绿(leucomalachite green, LMG)。在鱼体内和环境中残留时间长,具有潜在的“三致”作用[11],因此包括中国在内的许多国家都禁止其在水产养殖中使用。但是由于MG抗菌效果较好,价格低廉且无有效替代药物等原因,在近几年的监控工作中发现MG仍在个别水产品种的养殖中违规使用。表2是水产品中MG残留测定常用的方法标准,GB/T 19857—2005 (第一法)和GB/T 20361—2006的检测结果相近,差异不显著,可根据实验室情况自行选择。但是与液相色谱法(LC)相比,LC-MS/MS前处理操作相对简单,定性方式更准确,是进行阳性样品确证的必要方法,也是农业部水产品质量安全监控的首选方法。
表2 水产品中孔雀石绿残留标准测定方法
Tab.2 Detection standard of malachile green in aquatic products
1.3 氯霉素
氯霉素(chloramphenicol,CAP)是1947年首次从委内瑞拉链丝菌的培养液中提取而得到的抗生素[14],具有广谱抗菌作用,对多数G+、G-菌均有效,在水产养殖中能有效防治烂鳃、赤皮病。CAP对人类的毒性较大,可抑制骨髓造血机能、造成过敏反应,引起不可逆的再生性障碍贫血等[15]。美国、日本、韩国和欧盟等国家和地区均已禁止在食用性动物中使用氯霉素,并规定在动物源性食品中不得检出。中国农业部在2002年12月第235号公告《动物性食品中兽药最高残留限量》中规定CAP为禁用药物,在动物性食品中不得检出[6]。目前,CAP是中国水产品质量安全监管的对象之一,其抑菌效果优于其替代药物,近年来在大宗水产品中的检出率不高,但是带入途径复杂,仍是目前监控的重点。
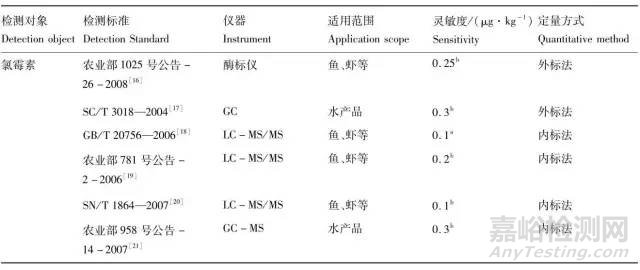
水产品中CAP残留量的测定方法很多,包括酶标法、气相色谱法(GC)、气相色谱-质谱联用法(GC-MS)和LC-MS/MS等(表3)。其中酶标法用于CAP的快速筛查测定,气相色谱法可以用于CAP的准确定量测定, LC-MS/MS和GC-MS法均可以作为CAP残留的确证方法,在对阳性样品的测定中,可以互为补充。
表3 水产品中氯霉素残留标准测定方法
Tab.3 Detection Standard of chloramphonicol in aquatic products
1.4 磺胺类
磺胺类药物(sulfonamides, SAs)是对氨基苯磺酰胺结构的一类药物的总称,主要用于预防和治疗细菌感染性疾病。在水产养殖中主要用于治疗鱼、虾、蟹、鳖等动物的细菌性疾病,防治鲤的赤鳍病,香鱼、虹鳟等的弧菌病等。由于SAs在生物体内的作用时间和代谢时间较长,蓄积浓度超过一定值会对人体健康造成危害,导致很多细菌对SAs产生抗药性[1]。因此,许多国家都对SAs的使用限量进行了规定,欧盟规定肉类食品中磺胺类药物的最高残留限量(MRL)为:单一SAs药物≤25 μg/kg,SAs总量≤100 μg/kg;日本肯定列表规定动物源性食品中单一SAs 0.01~0.1 mg/kg,其中水产品为0.1 mg/kg;国际食品法典委员会与中国农业部235号公告中均规定动物组织中SAs药物的MRL为100 μg/kg。
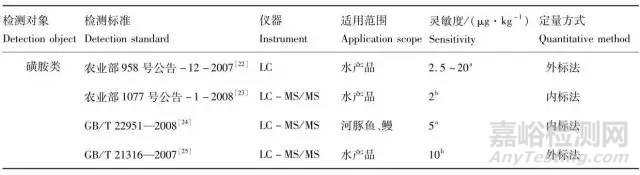
表4是水产品中磺胺类药物残留测定的方法标准,其中农业部958号公告-12-2007和农业部1077号公告-1-2008是常用的检测方法,农业部958号公告-12-2007前处理繁琐,回收率稍低,灵敏度基本能够满足限量要求;农业部1077号公告-1-2008方法简便快捷,灵敏度高,可以用于磺胺类药物的阳性确证。
2 方法操作要领和关键点
2.1 硝基呋喃类代谢物
2.1.1 标液配制
1)标准储备液配制时,应查看证书上的分子式和纯度,氨基脲(semicarbazize,SEM)和1-氨基乙内酰脲(1-aminohydantoin,AHD)的分子结构中通常带有盐酸盐,应根据分子量和纯度进行折算,配制时可借助超声波助溶。
表4 水产品中磺胺类残留标准测定方法
Tab.4 Detection standard of SAs in aquatic products
2)标准储备液低温放置后,稀释时应恢复至室温,观察是否有结晶析出,如有结晶析出,需重新摇匀溶解后再稀释。
3)硝基呋喃类代谢物的标准曲线需要衍生化,因此要与测试样品同时进行前处理。
2.1.2 提取过程
1)待测样品开始提取时加入盐酸调节pH约为1,因为不同样品基质酸碱度有差异,故要测pH。
2)衍生化过程振荡时间16 h并非严格控制,实验证明振荡12 h以上就能保证衍生化完全。
3)衍生化后调节pH至7.0~7.5(pH试纸测试),常规样品不需要再调节,如果难以调节,可考虑加入50 μL NaOH溶液(1 mol/L)。
2.1.3 净化过程
1)对于乙酸乙酯反萃取过程中发生乳化的样品,可将离心转速提高至6 000 r/ min以上,或者增加离心时间,可明显改善乳化层。
2)对于定容后仍旧浑浊的样品,可以采用正己烷去脂,14 000r/min离心10 min以上,脂肪漂浮在上层,取下层清液,过0.22 μm滤膜后进样。
3)对于基质干扰大的样品,如果采用SPE法净化,可以参考GB/T 20752—2006,使用Oasis HLB 固相萃取柱。使用前依次用5 mL甲醇、10 mL水活化,将待净化液转移至固相萃取柱中,用10 mL水洗涤,抽至近干后,用5 mL乙酸乙酯洗脱,并于40 ℃下氮气吹干,残留物用1.0 mL流动相溶解。
2.1.4 色谱条件
采用C18色谱柱进行测试,推荐进样量为10 μL。流动相中的有机相推荐使用甲醇,因为其灵敏度和分离效果更好。不同厂家的仪器对水相的选择有差别,通常采用2 mmol/L醋酸铵或者0.1%甲酸。
2.1.5 特殊样品的处理
1)对于残留量超出线性范围的样品,可以采取以下方式:一是减少称样量,根据估算结果,确定是否可以通过减少称样量实现目的;二是加大内标的量,并在定容时稀释到相应浓度。
2)SEM是呋喃西林药物的特征性代谢产物,但是它作为内源性物质在甲壳类产品中普遍存在,因此在对这类样品进行测试时,应考查该药物的带入途径。
2.2 孔雀石绿
2.2.1 标液配制
1)孔雀石绿标准品的分子结构中可能带有草酸盐,配制标准贮备液时应根据分子量和纯度进行折算。
2)由于孔雀石绿不稳定,标准储备液保存可采用少量分装,-18℃避光保存的方式。
3)标准曲线现用现配,标准曲线浓度最高点≤100 ng/mL,避免检测器饱和并防止污染仪器和色谱柱。
2.2.2 提取过程
对于标准方法GB/T 20361—2006,采用二氯甲烷进行反萃取时,如果分层不明显,可能二氯甲烷发生倒相,此时应该加入适量的超纯水或二氯甲烷,以使二氯甲烷相处于下层。
2.2.3 定容过程
采用标准方法GB/T 19857—2005测定时,定容过程应充分溶解残留物,可超声30 s。如果定容后样品溶液较浑浊,可将溶液移入2 mL离心管中,进行14 000 r/min高速离心,进一步去除大分子杂质。
2.2.4 色谱条件
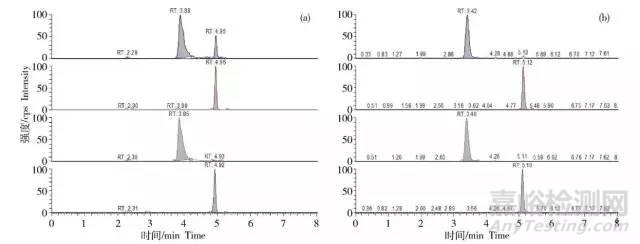
流动相中水相的pH对色谱峰形影响较大(图1),pH调为4.5后峰形明显改善,调节方式为在500 mL乙酸铵溶液中加入60 μL甲酸即可。
图1 流动相pH对孔雀石绿(1 ng·mL-1)色谱峰形的影响
(a)未调节pH的水相;(b)pH调为4.5的水相。
Fig.1 Effects of mobile phase pH on chromatographic peak profiles of MG (1 ng·mL-1)
(a)The pH value of aqueous phase was not adjusted;(b)The pH value of aqueous phase was adjusted to 4.5.
2.3 氯霉素
2.3.1 气相色谱法
SC/T 3018—2004为水产品中氯霉素残留量测定的气相色谱法,方法前处理步骤繁琐,操作中要注意以下几点:
1)样品均质提取应充分,并减少刀头上样品的附着,避免样品交叉污染。
2)净化时振荡混合过程要剧烈、充分,每次不少于2 min,尽量减少提取液转移过程中的损失。
3)衍生化反应前要注意防潮,所用器皿中不能有水,衍生化反应后,恢复室温,再进行氮吹,吹干过程很短,以刚好吹干为准。
2.3.2 液相色谱-串联质谱法
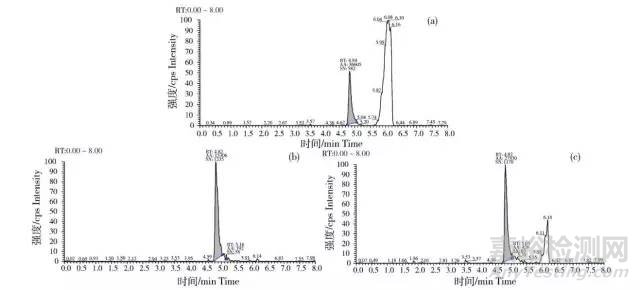
GB/T 20756—2006、SN/T 1864—2007和农业部781号公告-2-2006均为水产品中氯霉素残留测定的LC-MS/MS法,这3个方法的测定原理相似,前处理都比较简单,均可用于氯霉素残留的确证分析。但是净化过程存在区别,GB/T 20756—2006中正己烷液液萃取脱脂净化方式的干扰较大,SN/T 1864—2007的净化效果更好(图2)。
图2 3种标准方法的净化效果比较
(a)GB/T 20756—2006;(b)SN/T 1864—2007;(c)农业部781号公告-2-2006。
Fig.2 Comparison on purification effects of the three standard methods
(a)GB/T 20756—2006; (b)SN/T 1864—2007; (c)Announcement of the Ministry of Agriculture No.781-2-2006.
对于色谱条件的选择,当样品中干扰杂质对氯霉素的离子化或对色谱峰背景干扰时,推荐采用梯度洗脱的方式。
2.4 磺胺类
2.4.1 液相色谱法
农业部958号公告-12-2007为液相色谱法,包括紫外检测法(UVD)和荧光检测法(FLD)两个方法。紫外法和荧光法的准确度和灵敏度都能满足检测要求,但是紫外法的基质干扰较大,目标峰难以有效分离,而荧光法的干扰小,灵敏度更高。采用紫外检测法时要注意以下事项:1)浓缩过程应注意避光和严格控制温度,同时也要避免因过快的浓缩降低回收率,才能确保药物残留在溶液中的稳定性。2)浓缩后溶解残渣时,要保证溶剂的用量,如果不能完全溶解时可以适当增加乙酸溶液的用量,有效溶解梨形瓶中的SAs。3)SPE净化时,如果上样溶液中含有正己烷,会导致回收率下降,如果采用自动固相萃取仪,将上样速度设为3 mL/min时回收率最高。
2.4.2 液相色谱-串联质谱法
农业部1077号公告-1-2008是水产品中磺胺类多残留测定的液相色谱-串联质谱法,方法简单、快速。在具体操作过程中需要注意以下两个方面。
1)部分磺胺类标准品的溶解度不好,在进行标准溶液配制时,可以加入200~400 μL甲酸助溶,还可以降低标准贮备液的配制浓度。此外标准使用液应定期配制,否则对峰形有影响。标准曲线配制时应该采用流动相进行稀释,用纯甲醇稀释的标准溶液在色谱柱上无保留。
2)提取过程中,应将无水硫酸钠与样品充分搅匀后,再加入提取液,防止样品结块,提高提取效率。对于复杂基质的样品,正己烷去脂后,可以采用低温高速离心的方法。
3 对做好水产品兽药残留检测技术能力验证工作的建议
根据能力验证活动的要求,选择正确的检测方法标准,掌握检测方法的操作要领和关键点,减少方法对检测结果的影响是确保顺利通过能力验证工作的关键。在此基础上,还建议采取做好准备工作,提高检测能力,保证质量控制措施到位,以及对检测数据进行正确的修约等如下保障措施,减少不满意结果的产生。
3.1 提前练习
按规定的标准操作程序或作业指导书进行操作,熟练掌握方法的前处理过程,并能重现方法的灵敏度和准确度。
3.2 标准溶液核查
根据标准要求重新配置标准贮备液或购置有证标准溶液,并与在用标准溶液进行核对,保证标准溶液的有效性。
3.3 考核样品的处理
检查编号是否准确,包装是否完整、无破损,按照通知要求进行保存。严禁用微波等加热方式对样品解冻,应在室温下自然解冻后再进行前处理。样品前处理过程中,应尽量避光操作。
3.4 做好质量控制
质量控制中应包括空白实验(包括试剂空白和对应的基质空白)和控制样品(检出限加标、3~10倍检出限加标),与考核样品同时测定。空白实验可确保空白值在控制限内,避免测试过程中的污染和空白基质中的干扰。控制样品的有效性可确保测试结果的灵敏度和准确度。
3.5 检测结果的判断
在进行检测结果计算时,首先应考察校准曲线是否满足要求,其次是平行样的测定结果是否在相对偏差范围内,然后是质控样品的准确度和灵敏度是否符合标准要求,还要进行不确定度的计算。对于偏差较大的数据,可以采用统计学方法进行测算,如平均值的置信区间等。
4 小结
通过对水产品兽药残留测定中常用的检测标准进行梳理,强化检测方法中的操作要领和关键点,使检测人员的实验操作技能得到提升,有利于提高水产品兽药残留检测水平和能力验证的通过率,保证检测质量。随着水产品能力验证工作的规范性和公正性的不断加强,实验室的检测能力将会得到快速提高,水产品质量安全监管水平也会不断提升,有利于保障中国的水产品质量安全。


来源:AnyTesting


