您当前的位置:检测资讯 > 行业研究
嘉峪检测网 2025-08-05 19:04
1. 全球人工晶体市场分析
1.1 市场规模与增长趋势
全球人工晶体(Intraocular Lens, IOL)市场在近年来表现出稳健的增长态势,市场规模已达到数十亿美元级别。根据多家市场研究机构的数据,2023年全球市场规模存在细微差异,这主要源于不同的统计口径和估算模型。Zion Market Research的报告显示,2023年全球人工晶体市场价值为43.3亿美元。与此同时,Fortune Business Insights的评估则略高,为45.2亿美元。其他机构的估算值也集中在相似区间,如Reports and Insights报告为41.6亿美元 ,Market Research Future为44.6亿美元。进入2024年,市场规模继续扩大,Polaris Market Research的数据显示,2024年市场价值达到47.8亿美元,并预计在2025年增长至50.0亿美元。这些数据共同描绘出一个庞大且持续扩张的市场图景,其增长基础坚实,主要由全球人口老龄化加剧和白内障手术需求的持续增加所驱动。
全球人工晶体市场预计将继续保持强劲的增长势头。各市场分析机构对未来几年的复合年增长率(CAGR)和市场规模的预测虽有不同,但总体趋势高度一致,均指向显著的增长。Zion Market Research预测,到2032年市场规模将达到65.6亿美元,期间的复合年增长率为4.74%。Fortune Business Insights则预测市场规模将从2024年的48.2亿美元增长到2032年的82.6亿美元。Mordor Intelligence的预测更为乐观,认为到2030年市场规模将达到95亿美元,复合年增长率为6.64%。Research and Markets的预测也显示,到2030年市场规模将达到70.6亿美元,复合年增长率为7.4%。综合来看,市场普遍预期到2030年前后,全球人工晶体市场规模将突破70亿至90亿美元大关,显示出巨大的市场潜力和发展空间。
1.2 区域市场格局
北美地区,特别是美国,长期以来一直是全球人工晶体市场的领导者,并预计在未来几年继续保持其主导地位。这一领先地位主要归因于几个关键因素。该地区拥有高度发达的医疗保健体系和高水平的消费者健康意识,使得患者能够及时获得先进的眼科治疗。美国拥有庞大的老年人口基数,他们是白内障手术的主要目标群体。有利的医疗保险报销政策,如Medicare对白内障手术的覆盖,极大地降低了患者的经济负担,促进了手术的普及。高手术量和对高端、创新型人工晶体(如多焦点和EDOF镜片)的高接受度,共同推动了北美市场的持续增长。
欧洲市场同样是全球人工晶体行业的重要组成部分,其特点是老龄化人口结构和对高质量医疗保健的持续关注。根据欧盟统计局的数据,2024年欧洲65岁及以上人口占比达到21.6%,这为白内障手术创造了稳定的需求。与北美类似,欧洲市场对高端人工晶体的需求正在上升,尤其是在德国、法国、英国等发达国家。患者越来越倾向于选择能够提供全程视力和减少对眼镜依赖的先进产品。欧洲在眼科研究和创新方面也处于领先地位,许多知名的人工晶体制造商(如Carl Zeiss Meditec)均源自欧洲,这进一步促进了该地区市场的技术升级和产品迭代。
亚太地区被认为是全球人工晶体市场增长最快的区域,其巨大的市场潜力主要由中国和印度等人口大国驱动。该地区拥有庞大的老年人口基数,且白内障的患病率较高,但过去由于经济和医疗条件的限制,许多患者未能得到及时治疗。随着经济的快速发展和医疗基础设施的不断完善,白内障手术的可及性大幅提高,释放出巨大的市场需求。中国的人工晶体市场预计到2030年将达到2.453亿美元,复合年增长率为6%。日本作为发达国家,其人工晶体市场也相当成熟,预计将继续引领亚太地区的收入。
拉丁美洲、中东及非洲(LAMEA)地区的人工晶体市场虽然目前规模相对较小,但展现出巨大的增长潜力。这些地区的市场增长主要受到政府和非营利组织推动的防盲治盲项目的支持,这些项目旨在提高白内障手术的可及性和可负担性。随着当地经济的发展和医疗水平的提高,对人工晶体的需求正在稳步增长。特别是在一些新兴经济体,对高性价比的标准单焦点人工晶体的需求尤为旺盛。同时,随着生活水平的提高,对先进人工晶体的需求也开始显现,为市场参与者提供了新的增长机遇。
1.3 竞争格局与主要参与者
全球人工晶体市场呈现出高度集中的竞争格局,少数几家大型跨国公司占据了市场的主导地位。这些公司凭借其强大的研发能力、广泛的产品组合、成熟的全球分销网络和品牌影响力,构筑了较高的市场壁垒。
市场的主要领导者包括Alcon Inc.、Johnson & Johnson Vision、Carl Zeiss Meditec AG、Bausch + Lomb和Hoya Corporation。这些公司不仅在传统的单焦点人工晶体领域占据优势,更在代表未来发展方向的高端产品领域(如多焦点、EDOF、Toric等)展开激烈竞争。它们通过持续的研发投入、战略性收购和新产品发布来巩固和扩大市场份额。Alcon凭借其AcrySof系列产品在全球市场占据领先地位。Johnson & Johnson Vision则以其TECNIS系列产品和在屈光性白内障手术领域的创新而闻名。Carl Zeiss Meditec AG以其卓越的光学技术和高端产品在欧美市场拥有强大的影响力。
Alcon Inc.是全球眼科保健领域的领导者,也是人工晶体市场的绝对霸主。公司总部位于瑞士日内瓦,拥有约25,000名员工。其2024年的总收入达到94亿美元,其中人工晶体业务约占32%,显示出其在公司战略中的核心地位。Alcon的旗舰产品线是AcrySof系列人工晶体,该系列产品以其卓越的生物相容性和光学性能而闻名。公司在三焦点(trifocal)和散光矫正型(toric)人工晶体技术方面处于行业领先地位,其产品组合覆盖了从标准单焦点到最复杂的高端功能性人工晶体。Alcon在全球各大主要市场,包括北美、欧洲和亚太地区,都拥有强大的市场渗透率和品牌忠诚度,其持续的研发投入和广泛的教育培训项目进一步巩固了其市场领导地位。
Johnson & Johnson Vision(强生视力健)是全球人工晶体市场的另一巨头,总部位于美国佛罗里达州杰克逊维尔。作为强生公司的子公司,它拥有强大的研发实力和全球资源。其2024年视力保健部门的收入约为52亿美元。J&J Vision以其TECNIS系列人工晶体而著称,特别是TECNIS Synergy和Eyhance等产品,专注于解决老视(presbyopia)问题和提供延展的景深视觉。公司在屈光性白内障手术领域投入巨大,致力于通过技术创新帮助患者实现术后“脱镜”。J&J Vision还非常重视全球外科医生的培训和教育,通过其专业的培训项目,推广先进的手术技术和人工晶体应用知识,从而推动其产品的市场接受度。
Carl Zeiss Meditec AG是全球领先的眼科医疗技术公司,总部位于德国耶拿。作为光学巨头蔡司集团的成员,公司在光学设计和精密制造方面拥有无与伦比的优势。其2024年的收入达到26亿欧元。Carl Zeiss Meditec的人工晶体产品线,如AT LISA tri(三焦点)和CT ASPHINA(非球面)系列,以其卓越的光学质量和视觉性能在高端市场享有盛誉。公司在欧洲市场表现尤为强劲,并正在积极拓展亚洲市场。除了人工晶体,Carl Zeiss Meditec还提供包括手术显微镜、OCT(光学相干断层扫描)和生物测量仪在内的完整眼科手术解决方案,这种“一站式”的产品策略使其能够为眼科医生提供集成的手术平台,从而增强了客户粘性。
Hoya Corporation是一家总部位于日本的多元化跨国公司,其医疗保健部门在人工晶体领域占据重要地位。公司2024年医疗保健部门的收入约为59亿美元,其中眼科业务约占30%。Hoya Surgical Optics以其Vivinex和iSert人工晶体平台在亚洲太平洋地区市场占据主导地位。公司以其高品质的疏水性丙烯酸酯人工晶体和在预装式人工晶体递送系统方面的创新而闻名。预装式系统通过简化手术流程、提高手术效率和安全性,受到了外科医生的广泛欢迎。Hoya通过持续的技术创新和对区域市场的深入理解,在全球人工晶体市场中保持了强大的竞争力。
Bausch + Lomb是一家拥有悠久历史的眼科保健公司,总部位于美国新泽西州。公司2024年的收入为45亿美元。其人工晶体产品线包括Akreos和enVista等系列。Bausch + Lomb在发展中国家的市场拓展方面表现突出,通过推出高性价比的产品和可负担性项目,致力于解决全球范围内的白内障致盲问题。公司也在积极布局高端市场,其在2023年完成了对AcuFocus公司的收购,获得了其创新的IC-8 Apthera小孔径延展景深(EDOF) 人工晶体技术,该产品已于2022年获得FDA批准。这一举措显示了Bausch + Lomb向高端功能性人工晶体市场进军的战略意图。
2. 人工晶体技术分析
2.1 核心材料科学
人工晶体的材料选择是决定其光学性能、生物相容性、手术操作便利性以及长期安全性的关键因素。目前,市场上的主流材料是丙烯酸酯,根据其表面特性的不同,可分为疏水性和亲水性两大类。硅胶和聚甲基丙烯酸甲酯(PMMA)等传统材料仍在特定场景下使用。
疏水性丙烯酸酯(Hydrophobic Acrylic)
疏水性丙烯酸酯是目前全球应用最广泛的人工晶体材料,尤其是在欧美市场。这种材料的特点是含水量极低(通常在0.5%至1%之间),表面具有较强的疏水性。其最大的优势在于能够有效抑制后囊膜混浊(Posterior Capsular Opacification, PCO) 的发生。PCO是白内障手术后最常见的并发症之一,会导致视力再次下降。疏水性丙烯酸酯材料制成的晶体通常具有锐利的方形边缘设计,这有助于形成物理屏障,阻止晶状体上皮细胞的迁移和增殖,从而显著降低PCO的发生率。疏水性材料在光学性能上表现出色,能够提供高质量的视觉体验。其缺点是材料相对较硬,折叠和植入时需要更大的力量,且更容易在表面产生 “闪辉”(glistening) 现象,即材料内部形成微小液滴,可能会轻微影响视觉质量。
亲水性丙烯酸酯(Hydrophilic Acrylic)
亲水性丙烯酸酯是另一种重要的材料,其含水量较高,通常在18%至38%之间。这种高含水量赋予了材料更好的柔韧性和生物相容性,使其在植入时更容易折叠和展开,对手术器械的顺应性更好,操作更为便捷。亲水性材料制成的晶体表面更光滑,不易产生闪辉。早期的亲水性丙烯酸酯晶体曾被报道存在钙化(calcification) 和混浊(opacification) 的风险,这引发了对其长期安全性的担忧。尽管现代技术已经通过改进材料配方和制造工艺在很大程度上解决了这些问题,但关于其PCO发生率高于疏水性材料的争论依然存在。多项研究表明,由于亲水性材料的表面特性,其抑制PCO的效果不如疏水性材料,导致术后需要进行Nd:YAG激光后囊膜切开术的比例更高。
2.1.3 其他材料
在丙烯酸酯材料成为主流之前,硅胶和PMMA是人工晶体的主要材料。
硅胶(Silicone) 硅胶材料具有良好的柔韧性和生物稳定性,是最早被广泛使用的可折叠人工晶体材料。它的优点是光学性能良好,且可以通过更小的手术切口植入。硅胶材料的缺点是容易与硅油(一种用于复杂视网膜手术的填充物)发生粘连,因此对于可能需要未来进行视网膜手术的患者不适用。其抑制PCO的效果也不如疏水性丙烯酸酯。
聚甲基丙烯酸甲酯(PMMA) PMMA是一种硬性、不可折叠的塑料材料,是历史上第一种被成功植入眼内的人工晶体材料。由于其不可折叠的特性,植入PMMA晶体需要较大的手术切口(通常大于5.5毫米),这会增加手术创伤和术后散光的风险。随着微切口超声乳化技术的发展和可折叠晶体的普及,PMMA晶体的使用已大幅减少,目前主要在一些资源有限或特殊情况下使用。
2.1.4 材料对比 生物相容性、光学性能与临床结果
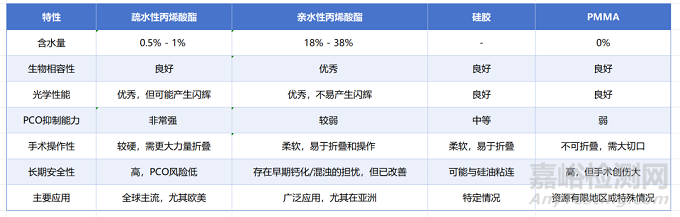
综合来看,不同的人工晶体材料在各项性能上各有优劣。
临床选择哪种材料,通常取决于外科医生的偏好、患者的具体情况以及经济因素。对于追求最佳长期视觉效果和最低PCO风险的患者,疏水性丙烯酸酯是首选。而对于需要精细操作或特定手术技巧的医生,亲水性丙烯酸酯的易操作性可能更具吸引力。

2.2 光学设计与产品类型
人工晶体的光学设计直接决定了患者术后的视觉质量和功能。随着技术的进步,人工晶体已经从单一功能的单焦点设计,发展到能够满足不同距离视觉需求、矫正散光等多种复杂功能的精密光学器件。
单焦点人工晶体(Monofocal IOLs)
单焦点人工晶体是最传统、最基本的人工晶体类型。其光学设计只有一个焦点,意味着它只能为患者提供一个固定距离的清晰视力,通常是远距离。患者在接受单焦点人工晶体植入后,如果需要看清中距离(如电脑屏幕)或近距离(如阅读书籍)的物体,仍然需要佩戴相应的眼镜。尽管功能单一,但单焦点人工晶体具有设计简单、价格经济、术后视觉干扰(如眩光、光晕)最少等优点,因此在全球范围内,尤其是在发展中国家,仍然是应用最广泛的类型。通过“单眼视”(Monovision) 技术,即一只眼植入看远的单焦点晶体,另一只眼植入看近的单焦点晶体,也可以在一定程度上帮助患者摆脱眼镜,但这需要患者大脑进行适应,并非所有人都适用。
多焦点人工晶体(Multifocal IOLs)
多焦点人工晶体旨在解决单焦点晶体无法同时满足远、中、近视力需求的痛点。其光学表面设计有多个同心圆或衍射环,能够将进入眼内的光线分配到不同的焦点上,从而使患者能够同时看清不同距离的物体。根据焦点数量的不同,可分为双焦点(bifocal) 和三焦点(trifocal) 人工晶体。多焦点人工晶体的最大优势在于能够显著降低患者对眼镜的依赖,实现“脱镜”生活。其缺点也较为明显。由于光线被分散到多个焦点,每个焦点的光线能量都会有所降低,可能导致对比敏感度下降。部分患者术后可能会出现眩光、光晕等视觉干扰现象,尤其是在夜间驾驶时。尽管如此,随着技术的不断改进,新一代多焦点人工晶体的视觉质量和患者满意度正在不断提高,使其成为追求高质量生活患者的首选。
散光矫正型人工晶体(Toric IOLs)
散光是一种常见的屈光不正,由于角膜或晶状体的曲率不规则导致。对于同时患有白内障和散光的患者,如果植入普通的人工晶体,术后仍然需要佩戴散光眼镜来矫正散光。散光矫正型(Toric)人工晶体则通过在晶体表面设计特殊的柱镜度数,在摘除白内障的同时矫正角膜散光。Toric人工晶体可以与其他光学设计相结合,如单焦点Toric、多焦点Toric或EDOF Toric,从而在为患者提供清晰视力的同时,解决散光问题。植入Toric人工晶体需要精确的手术规划,包括术前精确测量散光的轴位和度数,并在手术中将晶体旋转到预定的轴位上。其定位的准确性直接影响散光矫正的效果。Toric人工晶体的出现,极大地提高了白内障合并散光患者的术后视觉质量和生活质量。
延展景深型人工晶体(EDOF IOLs)
延展景深型(Extended Depth of Focus, EDOF)人工晶体是近年来发展起来的一种新型功能性人工晶体,它试图在单焦点和多焦点晶体之间找到一个平衡点。与多焦点晶体创建多个离散的焦点不同,EDOF晶体通过特殊的光学设计(如小孔径技术或衍射技术),将焦点“拉长”,形成一个连续的、扩展的清晰视觉范围。这种设计通常能够提供出色的远距离和良好的中距离视力,同时保留部分近距离视力。EDOF晶体的主要优势在于,它在提供宽广视觉范围的同时,显著减少了传统多焦点晶体常见的眩光和光晕等视觉干扰现象,并且对比敏感度更高,神经适应性更好。因此,EDOF晶体特别适合那些对视觉质量要求高,但又担心多焦点晶体副作用的患者。目前市场上的代表性产品包括Tecnis Symfony等。
可调节人工晶体(Accommodating IOLs)
可调节人工晶体是模拟人眼自然晶状体调节功能的一种理想化设计。其设计理念是,当眼睛需要看近处物体时,睫状肌收缩,通过悬韧带的作用,使人工晶体的形状或位置发生改变,从而增加其屈光力,实现变焦。理论上,这种设计可以提供从远到近的全程连续视力,且不会产生多焦点晶体那样的视觉干扰。目前市场上的可调节人工晶体的实际调节能力有限,其效果尚不能完全达到理想的生理状态。尽管如此,随着材料科学和生物力学研究的深入,可调节人工晶体仍然是未来人工晶体发展的重要方向之一,有望为患者带来更自然、更完美的视觉体验。
2.3 制造工艺与递送系统
精密制造与质量控制
人工晶体的制造是一个对精度要求极高的过程,通常在洁净室环境中进行,以防止微粒污染。制造过程通常从高质量的医用级聚合物材料(如丙烯酸酯或硅胶)开始。首先,通过精密的数控车床或铣床,根据预先设计好的光学模型,对材料进行加工,形成晶体的基本形状,包括光学区和襻。这个过程需要极高的精度,因为光学表面的任何微小瑕疵都可能影响最终的视觉质量。Rayner采用精密的制造工艺,结合专有的边缘设计,以确保其IOL的光学和机械性能。加工完成后,晶体需要经过多道抛光工序,以获得光滑、透明的光学表面。随后,根据设计要求,可能还需要进行表面处理,如创建非球面轮廓或衍射环。对于需要过滤蓝光或紫外线的晶体,还需要在材料中添加特定的色素(chromophore)。EyeKon Medical公司在其Natural Yellow™系列IOL中,使用了与年轻人眼晶状体相同的天然色素(3-羟基犬尿氨酸),以提供自然的紫外线和紫光过滤效果。在整个制造过程中,质量控制是至关重要的。每个晶体都需要经过严格的检测,包括光学性能测试(如屈光度、像差)、尺寸测量和表面质量检查,以确保其符合设计规格和监管要求。EyeKon Medical公司采用其专有的“CLEAR VIEW”分子测试程序,以识别和去除在亲水性丙烯酸酯晶体中可能存在的未完全聚合的微量物质,确保产品的最高质量。
预装式人工晶体(Preloaded IOLs)系统
预装式人工晶体(Preloaded IOLs)系统是近年来白内障手术领域的一项重要进步。传统的IOL植入过程需要手术助手或医生在手术台上手动将晶体装载到植入器中,这个过程不仅耗时,而且存在晶体在装载过程中受损、污染或错误装载的风险。预装式系统将IOL预先由制造商装载在一次性的、经过无菌处理的植入器内,医生在手术时只需打开包装,即可直接进行植入操作。这大大简化了手术流程,缩短了手术时间,并降低了手术风险。各大IOL制造商都推出了自己的预装式系统,并与自家的IOL产品相匹配。Alcon的Clareon® AutonoMe®系统就是为其Clareon®系列IOL设计的预装式递送系统,它提供了直观、易于控制的植入体验,有助于实现精确的IOL植入。同样,Bausch + Lomb也提供多种预装式IOL和植入器组合,如INJIOO™植入器,适用于其部分型号的IOL,推荐切口尺寸为2.2-2.6毫米,可实现单手操作。预装式系统的设计也在不断优化,旨在实现更小的植入切口和更平稳的晶体展开。Rayner公司宣布其新推出的RayOne Galaxy™ IOL将在整个产品线中提供完全预装的版本,并立即提供散光矫正型号。预装式系统的普及,不仅提升了手术的效率和安全性,也体现了人工晶体技术向更便捷、更标准化方向发展的趋势。
植入技术与手术切口发展趋势
随着人工晶体材料和设计的进步,植入技术和手术切口也在不断演变。手术切口正朝着更小的方向发展,从最初的5.5毫米以上,发展到如今的2.2-2.8毫米甚至更小。微切口白内障手术(MICS) 已成为主流,其优点在于创伤小、恢复快、术后散光小。为了实现微切口植入,人工晶体必须具有优异的可折叠性和记忆性,能够在通过狭小的注射器后,在眼内迅速、平稳地展开。手术技术本身也在不断创新,如飞秒激光辅助白内障手术(FLACS) 的应用,可以实现更精准的撕囊、劈核和切口制作,进一步提高了手术的安全性和可预测性,也为高端功能性人工晶体的植入创造了更好的条件。
3. 当前技术与新兴创新
3.1 现有主流技术优化
多焦点与EDOF技术的融合与改进
当前,多焦点和延展景深(EDOF)技术是功能性人工晶体领域的两大主流方向,各大厂商正致力于将两者的优势进行融合,并不断优化其性能。Johnson & Johnson的TECNIS Synergy™晶体,被称为“三焦点EDOF”晶体,它结合了EDOF技术提供的连续、高质量的远中视力,以及一个额外的近焦点,从而实现了更完整的全程视力覆盖,同时最大限度地减少了传统三焦点晶体可能带来的视觉干扰。Alcon公司也在不断升级其产品线,2025年推出的Clareon® PanOptix® Pro三焦点晶体,通过全新的ENLIGHTEN® NXT光学技术,将光能利用率提升至94%,在提供三个清晰焦点的同时,保证了极高的视觉质量和对比敏感度。这些改进的核心目标是在增加焦点、扩大景深的同时,尽可能地保留光能、减少光学副作用,为患者提供更自然、更舒适的视觉体验。
散光矫正技术的精准化发展
散光矫正型(Toric)人工晶体的精准度是影响术后视觉质量的关键。为了提高矫正的精准性,制造商在多个方面进行了技术优化。首先是晶体设计的改进,例如Johnson & Johnson的TECNIS Toric II®平台,采用了方形、磨砂处理的襻设计,极大地增强了晶体在囊袋内的旋转稳定性,确保柱镜轴位在术后长期保持精准。其次是计算公式的优化,结合人工智能和大数据,开发出更精准的Toric晶体度数计算软件,能够更准确地预测术后残余散光。Bausch + Lomb公司还推出了 “Low-Cyl” 技术,将可治疗的散光范围扩大至角膜平面低至1.0D,使得更多低度散光患者也能从Toric晶体中获益。这些发展使得散光矫正变得更加个性化和精准化。
材料表面处理与生物相容性提升
人工晶体的长期安全性和视觉稳定性与其材料的生物相容性密切相关。制造商通过先进的表面处理技术,不断提升材料的性能。Alcon的Clareon®材料,通过其独特的表面工程技术,在保持疏水内核稳定性的同时,增加了表面的亲水性,从而减少了蛋白质和细胞的粘附,降低了术后炎症反应和后发障(PCO)的风险。对材料本身的改良也在不断进行,如开发具有更高纯度的硅胶材料,以减少炎症细胞的粘附,使其更适合于眼内环境复杂的患者。这些材料和表面处理技术的进步,旨在让人工晶体与眼内环境实现更和谐的共存,确保患者获得长期、稳定、清晰的视觉。
3.2 革命性新兴技术
在现有主流技术不断优化的同时,人工晶体领域也涌现出一些具有革命性潜力的新兴技术。这些技术旨在从根本上改变人工晶体的功能,从静态的、固定的光学器件,转变为动态的、可调的、甚至智能化的视觉解决方案。这些创新不仅有望解决当前技术无法完全克服的挑战,如术后屈光不正的残余误差、调节能力的丧失等,还可能开启个性化视觉矫正的新时代。其中,光可调式人工晶体(LALs)和植入式胶原聚合物镜片(ICLs)是两项备受关注的前沿技术。
光可调式人工晶体(Light Adjustable Lenses, LALs)
光可调式人工晶体(LAL)是人工晶体技术领域的一项革命性突破,它首次实现了在白内障手术后对人工晶体的屈光力进行非侵入性的精确调整。这项技术的核心在于LAL由一种特殊的光敏性硅胶材料制成,其中均匀分布着被称为“大分子单体”(macromers)的光敏分子。当患者完成手术后,如果其屈光状态未达到理想效果(存在残余的近视、远视或散光),医生可以使用一种特殊的紫外线(UV)光照射设备,对LAL进行“雕刻”。其工作原理基于光化学和扩散原理。当特定波长(365纳米)的UV光精确地照射到晶体的某个区域时,该区域的大分子单体被激活并聚合成聚合物。这导致被照射区域的单体浓度降低,形成一个浓度梯度。在随后的12小时内,周围未被照射区域的大分子单体会扩散到被照射区域,直至浓度达到平衡。这个扩散过程会导致晶体的曲率发生高度可预测的改变,从而精确调整其屈光力。通过控制光照的区域、形状和剂量,医生可以同时对球镜和柱镜度数进行调整。患者可以在术后体验调整后的视力,并根据个人生活习惯和偏好,与医生沟通进行多次微调,直到获得最满意的视觉效果。一旦达到理想状态,医生会对整个晶体进行一次最终的“锁定”光照处理,使所有剩余的大分子单体完全聚合,从而永久固定晶体的形状和度数,防止其再次发生任何改变。LAL技术由美国加州大学旧金山分校的Danial Schwartz博士和加州理工学院的Robert Grubbs教授于1997年共同研发,并于2017年11月获得美国FDA批准用于人类。其主要适应症是患有白内障且角膜散光至少为0.75D的患者。该技术也存在一些禁忌症,例如患有黄斑病变、有疱疹性眼病史、正在服用增加光敏性药物(如四环素、胺碘酮等)的患者均不适合使用。LAL技术的出现,极大地提高了白内障手术屈光矫正的精准度和患者满意度,代表了个性化医疗在眼科领域的重大进步。
植入式胶原聚合物镜片(Implantable Collamer Lenses, ICLs)
植入式胶原聚合物镜片(ICLs)代表了一种与传统白内障手术中使用的IOL截然不同的技术路径。ICL并非用于替换已经混浊的自然晶状体,而是作为一种“加法”型屈光矫正工具,被植入到眼内,位于虹膜之后、自然晶状体之前,因此也被称为有晶体眼后房型人工晶体(Phakic Posterior Chamber Intraocular Lens)。这项技术主要面向那些希望摆脱眼镜或隐形眼镜,但又不适合或不愿意接受角膜激光手术(如LASIK)的高度近视或散光患者。ICL手术保留了患者自身的调节能力,因此可以同时矫正屈光不正和老花眼。STAAR Surgical公司是ICL技术的全球领导者和主要推动者。其最新的EVO/EVO+ Visian ICL系列产品由一种名为Collamer®的专利材料制成。Collamer®是一种由羟乙基甲基丙烯酸酯(HEMA)和猪源胶原蛋白组成的生物相容性聚合物。这种材料具有极高的生物相容性,能够与眼内环境和谐共存,并且其表面带负电荷,可以抑制蛋白质和细胞的沉积。EVO ICL的一个革命性设计是其中心带有一个直径为0.36毫米的中央孔(Central Port) ,这个设计允许房水能够自然地从前房流向晶状体前表面,从而维持了正常的房水循环,避免了早期ICL产品需要术前进行周边虹膜切开术(PI)以预防瞳孔阻滞性青光眼的必要。这一改进极大地简化了手术流程,并降低了相关并发症的风险。EVO ICL的光学直径根据屈光度不同而变化,范围从4.9毫米到6.1毫米,可以通过一个3.5毫米或更小的角膜切口折叠植入。其临床应用已得到多项长期临床研究的支持,证明了其在矫正中高度近视和散光方面的安全性和有效性。ICL技术为屈光不正的矫正提供了一个独特的、可逆的、且视觉质量优异的解决方案,是人工晶体技术领域一项重要的创新。
智能化与个性化定制趋势
随着人工智能(AI)、大数据和先进制造技术的发展,人工晶体的选择和定制正朝着更智能化、更个性化的方向发展。未来的趋势是利用AI算法,综合分析患者的角膜地形图、眼轴长度、前房深度、年龄、生活习惯等海量数据,为每一位患者推荐最适合的人工晶体类型和度数。3D打印等先进制造技术也为完全个性化的人工晶体定制提供了可能。理论上,可以根据患者眼内的精确解剖结构,打印出完全贴合的、具有独特光学特性的晶体,从而实现前所未有的视觉矫正效果。Rayner公司在2024年推出的全球首款AI设计的螺旋形人工晶体RayOne Galaxy,就是这一趋势的早期体现。
3.3 未来技术展望
纳米技术在材料科学中的应用
纳米技术被认为是推动下一代人工晶体发展的关键驱动力之一。通过在材料科学中引入纳米技术,科学家们有望开发出具有革命性性能的新型人工晶体材料。利用纳米技术可以精确控制材料的表面结构和化学性质,从而极大地提高其生物相容性,减少术后炎症反应和细胞粘附。纳米材料还可以被用来改善人工晶体的光学性能,通过设计具有特定纳米结构的表面,可以减少眩光和光晕,提高对比敏感度。未来,纳米技术甚至可能用于开发具有“智能”响应能力的材料,能够根据环境光线强度自动调节透光率的“光致变色”人工晶体,或者能够响应眼内生化信号的材料,为实现真正的动态视觉调节奠定基础。
人工智能辅助的晶体选择与手术规划
人工智能(AI)和机器学习技术正在深刻地改变医疗行业,眼科领域也不例外。未来,AI将在人工晶体的个性化选择和精确手术规划中扮演越来越重要的角色。通过分析海量的患者数据,包括眼部生物测量参数(如眼轴长度、角膜曲率、前房深度等)、角膜地形图、波前像差数据,甚至患者的生活方式和用眼习惯,AI算法可以构建出复杂的预测模型。这些模型能够比传统公式更准确地预测术后屈光状态,并为每位患者推荐最适合其独特眼部条件和视觉需求的人工晶体类型和度数。AI辅助的决策支持系统可以帮助医生做出更科学、更个性化的选择,从而最大限度地提高患者术后的视觉质量和满意度,减少二次手术的风险。这种数据驱动的个性化医疗模式,将是未来屈光性白内障手术发展的必然趋势。
可调节焦距与动态视觉解决方案
实现真正意义上的动态变焦,即完全模拟年轻人自然晶状体的调节功能,是人工晶体技术发展的终极目标。目前市场上的可调节晶体技术尚不完善,未来的研究方向将集中在开发具有更大调节幅度、更快响应速度和更自然调节过程的晶体。这可能涉及到全新的设计理念,如利用液晶、电活性聚合物等智能材料,通过微电机或微流体系统驱动晶体形状的改变。或者,通过仿生学设计,开发出能够利用眼内睫状肌收缩来实现变焦的晶体。一旦这项技术取得突破,将彻底解决老花眼问题,为患者提供从远到近无缝、连续的动态视觉,这将是眼科领域的一场突破。

来源:医械知识产权


