今日头条
信达IGF-1R抗体甲状腺眼病III期研究积极。信达生物IGF-1R抗体注射液IBI311治疗甲状腺眼病(TED)患者的中国III期研究(RESTORE-1)达到主要终点。与安慰剂相比,IBI311治疗第24周时患者研究眼的眼球突出应答率(研究眼相对于基线突眼度回退≥2mm,且不伴有对侧眼突眼度增加≥2mm的受试者比例)显著更高(85.8%vs3.8%,95%CI:69.8%-93.9%,P<0.0001)。该公司计划尽快向NMPA递交其新药上市申请(NDA)。
国内药讯
1.智翔金泰IL-17A单抗银屑病Ⅲ期临床成功。智翔金泰自研IL-17A抗体赛立奇单抗(GR1501)治疗中、重度斑块状银屑病的Ⅲ期临床达到主要终点和次要终点。第12周时,与安慰剂相比,GR1501治疗达到银屑病皮损面积和严重程度指数较基线至少改善75%(PASI 75)的患者比例显著更高(90.7%vs8.6%);两组皮损清除/几乎清除(PGA0/1)的患者比例分别为74.4%和3.6%。详细结果已发布于期刊British Journal of Dermatology上。
2.迈威铁稳态调节单抗获FDA孤儿药资格。迈威生物自主研发的TMPRSS6单抗9MW3011(MWTX-003/DISC-3405)获FDA授予孤儿药资格,用于治疗真性红细胞增多症。9MW3011可通过与靶点特异性结合,上调肝细胞表达铁调素(Hepcidin)的水平,抑制铁的吸收和释放,以调节体内的铁稳态。该新药目前正在中美同步临床开发,拟开发用于包括β-地中海贫血、真性红细胞增多症等与铁稳态相关的疾病。
3.AZ创新酶替代疗法中国获批临床。阿斯利康1类生物制品ALXN1850注射液(efzimfotase alfa)获国家药监局临床许可,拟开发作为酶替代疗法用于治疗低磷酸酯酶症(HPP)。ALXN1850具有较长的半衰期。该新药目前正在国际Ⅲ期临床中分别针对此前未接受过asfotase alfa治疗的青少年和成人HPP患者、先前接受过asfotase alfa治疗以及未接受过治疗的儿童HPP患者(2~12岁)评估治疗效果。
4.凯思凯迪TRβ激动剂获批NASH临床。凯思凯迪靶向甲状腺受体β(TRβ)的小分子激动剂CS060304获FDA批准开展Ⅰ期临床研究,拟评估用于非酒精性脂肪性肝炎(NASH)适应症的安全性与有效性。临床前研究显示,CS060304在NASH小鼠模型中可显著改善NAS评分和纤维化,具有起效剂量低、药效显著且耐受性良好的特点。该公司计划在中、美同步推进CS060304的临床开发。
5.唯源立康HSV外用基因疗法获批临床。北京唯源立康1类生物药WG1025获国家药监局临床许可,其适应症为营养不良型大疱性表皮松解症(DEB)。WG1025是国内首款可重复使用的外用基因疗法,含有两个拷贝全长COL7A1基因的复制缺陷型HSV-1载体,可以在皮肤细胞持续表达功能性VII型胶原蛋白并促进创口愈合。在研究者发起、针对DEB治疗的IIT研究中,WG1025给药后创口完全愈合时间为5-10天,且药物总体耐受性良好。
6.百奥赛图与吉利德达成多靶点抗体合作。百奥赛图宣布与吉利德达成抗体评估和选择协议,授权吉利德在三年提名期内使用百奥赛图针对广泛的药物靶点建立的全人抗体库进行相关靶点的抗体评估,合作开发治疗性特定抗体。根据协议,百奥赛图将会获得一笔付款;且针对每个被提名的靶点被选定的抗体,百奥赛图将有权获得选择权行权费,开发、监管和销售里程碑付款,及个位数净销售额分成。
国际药讯
1.奥希替尼治疗III期肺癌结果积极。阿斯利康第三代EGFR抑制剂奥希替尼(Tagrisso)治疗不可切除、EGFRm突变、III期非小细胞肺癌(NSCLC)经治患者的III期研究LAURA结果积极。与安慰剂相比,Tagrisso在这类难治、脑转移患者中的无进展生存期(PFS)的统计具有显著性改善;患者的总生存期(OS)数据也显示改善趋势。该项研究的总生存期(OS)关键次要终点仍在持续评估中。
2.大冢APRIL单抗获IgA肾病突破性疗法认定。大冢制药与Visterra公司开发的细胞因子A增殖诱导配体(APRIL)单抗sibeprenlimab(VIS649)获FDA突破性疗法认定(BTD),用于治疗免疫球蛋白A(IgA)肾病。在Ⅱ期临床中,与安慰剂相比,sibeprenlimab(2mg、4mg和8mg)治疗12个月时患者的蛋白尿水平显著减少,两组患者24小时尿蛋白/肌酐比值(UPCR)的几何平均比值降幅分别为47.2%、58.8%、62.0%和20.0%。
3.赛诺菲渐冻症药物Ⅱ期临床未达主要终点。Denali公司与赛诺菲开发的潜在“first-in-class”小分子RIPK1抑制剂SAR443820(DNL788)在治疗肌萎缩性侧索硬化症(ALS,渐冻症)的Ⅱ期Himalaya试验中未能达到显著改善修订版ALS功能评定量表(ALSFRS-R)评分的主要终点。该新药具有中枢神经系统(CNS)高渗透性,主要用于调节eIF2B的活性,以提高神经元存活率。目前,SAR443820也正在Ⅱ期试验中评估治疗多发性硬化症(MS)的潜力。
4.首款外用DEB基因疗法临床积极。Krystal Biotech公司基因疗法Vyjuvek的眼药水配方,在用于遗传性营养不良性大疱性表皮松解症(DEB)患者改善眼球表面受累(因病致盲)的临床试验结果积极。受试者在三个月内接受19次Vyjuvek治疗,患者角膜上皮完全愈合;眼压和视网膜完整性恢复正常,并表现出更好的视力。Vyjuvek是FDA针对DEB批准的首款基因疗法,也是首款可重复给药的基因疗法。
5.“减肥神药”或可治阿片类药物成瘾。诺和诺德GLP-1类药物利拉鲁肽用于对抗阿片类药物成瘾的小型随机对照试验结果积极。数据显示,使用利拉鲁肽的患者对阿片类药物的渴望减少30%,即使是在最低的利拉鲁肽剂量下,这种效果也很明显。相关研究结果已公布于美国科学促进会(AAAS)议上。目前GLP-1RA精神疾病益处研究仍处于早期阶段。
医药热点
1.中国生物制药再剥离非核心业务。2月6日,中国生物制药发布公告,该公司同附属公司与两位买方及正大青岛签订协议,中国生物制药将出售正大青岛67%股权给两位买方,交易总对价约为人民币18.2亿元。正大青岛主要从事骨质疏松症药物及海洋药物的研究开发、生产及销售。完成出售事项后,集团将继续持有正大青岛26%权益。
2.海南深化医改十大创新举措公布。2月19日,2023年海南省深化医改十大创新举措向社会公布。2023年海南省深化医改十大创新举措是:打造三条“医疗主干道”,推进优质医疗资源逐级下沉取得新成效;全面推广“2﹢3”健康服务包,防治严重影响全省居民健康的5种疾病;以综合改革推进公立医院高质量发展;推动数字疗法从“政策高地”走向“应用高地”,推动医疗卫生服务提质增效降费;打造区域危急重症救治体系,建成“15分钟医疗急救圈”等。
3.2024医药反腐强势来袭。2月18日,中纪委官方发布题为《牢牢扛起重点领域监督职责保障护航高质量发展》的头条文章指出:深化中央企业“靠企吃企”问题专项整治,是中央纪委国家监委指导国务院国资委推进的重点工作。文中点名,中国通用技术集团纪检监察组围绕药品、器械、耗材试剂“带金销售”等5个方面的34个“靠医吃医”“靠药吃药”问题推进整治。这是医药首次和金融、基建工程等腐败高发领域并称列举,意味着医药领域反腐工作已被提升到前所未有的高度。
评审动态
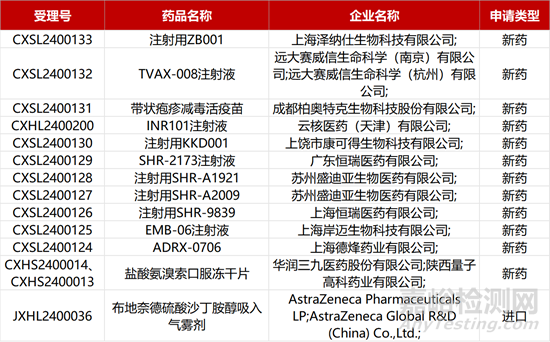
1. CDE新药受理情况(02月09日)
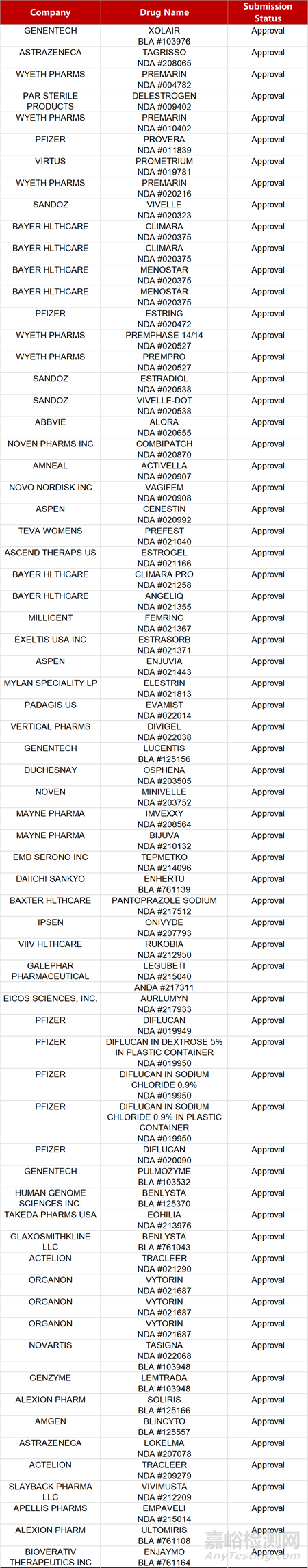
2. FDA新药获批情况(北美02月16日)