医疗器械可用性工程的重要性
制造商在生产新一代产品时,由于经常遭遇这样的难题:应舍弃前代产品的哪些控件和按钮?因此,不少企业便索性全部保留,用繁多的标签和功能键进行组织。这种做法使得设备看似并非医疗器械,而更像是工程师专用的设备。
如果制造商拥有最好的功能组件,但其操作员未能正确使用,那功能组件反而成为负担。
由此,良好的可用性过程就显得尤为重要,可用于防止上述情况并降低使用相关的风险。
产品开发时,应遵守IEC 60601-1-6、IEC 62366-1等关键性标准,FDA人为因素和可用性工程指南等,这些必需的文件与设计控制是一致的。
本期将着重引用IEC 62366-1作解读,该标准同时满足欧盟、FDA和不少国家及地区要求。
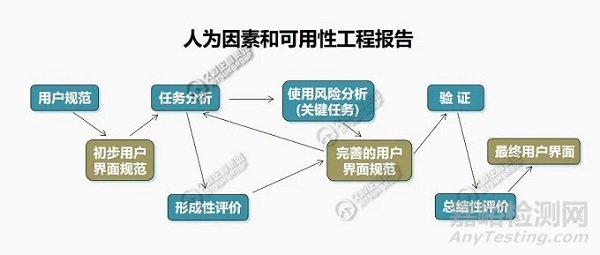
可用性工程的主要步骤
注意:随着产品可用性在开发过程中日益完善,这些步骤之间经常会发生迭代。
可用性工程步骤→创建用户规范
1. 概念
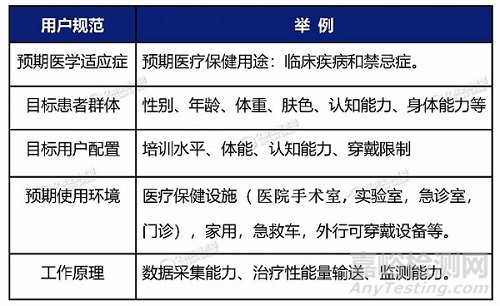
用户规范为关键规范,较大程度决定产品可用性评估方式,内容应包括:预期医学适应症、目标患者群体、目标用户配置、预期使用环境和工作原理。
IEC 62366-1、FDA人为因素和可用性工程指南(HF&UE)均规定“用户规范的最低要求”(见下表)
2. 用户需求
在"用户需求"文档中加入用户规范,是较好的做法。但经常出现的问题是:企业不具备该文档,或企业将其作为产品需求和营销需求的融合而编写。
"用户需求"应当使用用户术语、可测试(即:能够被验证)。"用户需求"虽然较少,但通常会催生大量的产品需求。
用户需求与产品需求的举例说明:
·用户需求:该产品只能在医院实验室使用。
·产品需求:
A.器械应在20-35℃之间运行
B.器械应在10%至95%相对湿度非冷凝的范围之间运行
C.器械应在570毫米汞柱至760毫米汞柱之间运行
D.器械应满足IPX 2流体进入要求
其他:照明、电磁兼容性、泄漏等。
3. 用户配置
对用户界面进行形成性和总结性评估时,重点在于:使用充足的用户配置和患者群体样本进行评估。审核部门将关注前述内容,并且如果因为该研究未充分涵盖用户规范,则总结性评估不得不面临重新来过的重大挫折。
用户配置影响权限的示例:
服务/维护用户:无法访问患者记录,但可访问计算机文件、诊断(服务菜单)等。
研究用户:匿名化数据文件,无法访问操作系统、诊断(服务菜单)等。
临床用户:可访问先前记录的患者信息文件,但无法访问系统文件、服务菜单或更新软件的能力等。
紧急用户:能够快速运行一个案例,但不能审查以前保存的文件或审查已归档的案例。
管理员用户:能够分配密码,无法访问操作系统、诊断等。
举例说明:
开发一种具有多个用户配置的仪器。服务用户无法访问患者数据,而研究用户可以访问患者数据,但导出时必须匿名(仅允许显示年龄和性别)。不同的权限被定义,然后用户界面也基于各种权限排列而开展设计。
可用性工程步骤→用户界面规范
用户界面User Interface是用户所接触产品的所有方面。60601-1则提出:用户界面是可访问的部分。软件的图形用户界面GUI特征非常显著,但可能不容易联想到:服务访问面板、传输手柄、连接器位置和连接器类型。
用户界面的作用:便于在预期使用环境中,实现各种用户配置的预期用途。一个被良好定义的用户规范提供简练的GUI实现方法,可显示登录用户轻松执行任务所需内容。拥有明显且简单的控制并明确提示下一步操作,对某些利基产品而言至关重要。
用户界面规范的示例包括:视角、无菌窗帘或手套操作的适应性,手持和/或移动设备的重心等,包装和使用说明书的布局/可读性也被认为是UI一部分。所有这些规范都需要可确认和验证。
可用性工程步骤→任务分析
任务分析是对给定用例的用户任务的逐步分解。
■ 由于用户的不同类型,因此以下情况可能使用案例进行分析:
A. 初始安装;
B. 更新和维修;
C. 设备配置;
D. 设备操作;
E. 数据审查;
F. 存 档。
■ 给定的用例定义了用户/参与者(来自用户规范)、使用场景的触发器以及目标的结束。
■ 建议对前提条件进行说明,例如:设备已安装和配置,或在下游用例中的设备已连接电源、初始设置和连接均已完成等。
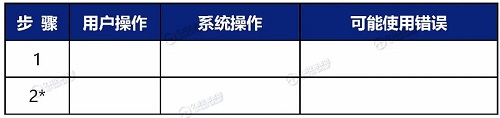
■ 执行分步分析,说明用户操作、系统操作(响应)和可能的错误。
表格:使用流程–任务分析(*代表关键任务):
用户任务属于关键任务,如果被错误执行或根本不执行,可能对患者或用户造成严重伤害。如果设备无关键任务文档,则应当说明其基本原理。所有关键任务都将在人为因素验证测试期间进行评价。
理想情况下,在设计中应尽可能减少关键任务的数量,但许多情况下,用户技能是涉及设备诊断和/或治疗过程的重要组成。
可用性工程步骤→形成性评价
即:制造商识别潜在用户(根据用户规范)并征求其对用户界面的反馈。
形成性评价计划应说明:所用的评价方法、正评价的用户界面的部分、执行各UI评价的可用性工程过程。
■ 模型设备、故事板、原型,都是让用户在最终产品出现前亲身体验用户界面如何工作的方法。
■ 测试使用流程,尤其是关键任务,记录结果并用于用户界面的修订或改进。
■ 更新UI规范和UI\使用流程\使用风险分析。
■ 计划迭代并记录评审和反馈。用户手册是其中重要部分,需评价其有效性。通常,用户手册被用作培训一部分,并在UI实际评价前有decay period(目的是评价说明书在培训/教育用户方面的有效性),将被呈现于总结性评价,但在形成性评价阶段开始时该内容同样也具备价值。
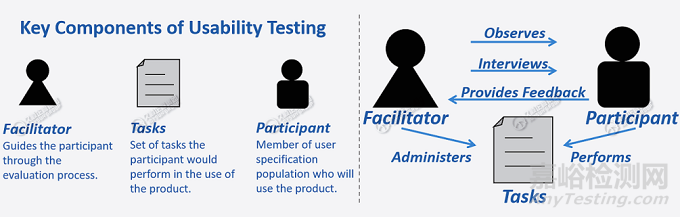
图:可用性测试的关键组成:
形成性评价和总结性评价都可通过类似方式开展,尽管总结性评价使用最终定型设备和IFU。
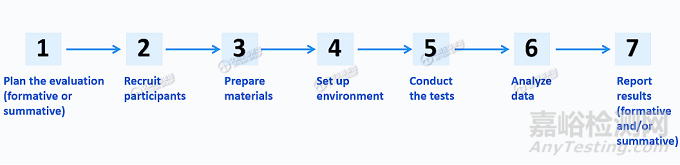
图:可用性测试7步骤(形成性和/或总结性)
可用性工程步骤→总结性评价
总结性评价发生于最终用户界面实施例。对每个与危害相关的使用场景,总结性评价的UI评价方案应明确所用的评价方法、评价UI的所属部分,以及适用情况下确定安全信息是否可感知、可理解、支持正确使用的标准。
总结性评价真正值得关注的是:用户规范所要求的产品预期用途的可用性验证。其必须评价关键任务,并对总体风险可接受性提供信息。