您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2025-07-28 19:24
摘要:目的 运用多种微生物鉴定技术建立制药企业无菌制剂高风险生产区环境微生物鉴定信息库。方法 连续4个季度对中间体、制药用水、洁净空间、人员设备表面等收集微生物,采用VITEK生化鉴定、MALDI-TOF MS蛋白鉴定和16SrRNA/ITS基因鉴定技术进行鉴定,结合微生物形态学和来源信息进行分析,建立相应的微生物鉴定信息库。结果 共收集获得89株细菌和5株真菌的鉴定结果,开展相关形态学分析:在收集的94株菌中,革兰氏阳性球菌和革兰氏阳性芽孢杆菌共占比60.6%,是洁净区常见污染菌;B级环境收集到46株微生物,葡萄球菌是主要优势菌属,占比45.7%,其次是芽孢杆菌(17.4%)、微球菌(6.5%)和酵母菌(4.3%),B级还分离到1株洋葱伯克霍尔德菌;制药用水收集到29株微生物,主要为革兰氏阴性菌(58.6%)。结论 本研究建立了融合生化、蛋白、基因鉴定结果的微生物鉴定信息库并开展相关分析,为制药企业开展风险控制,加强对不可接受微生物的管理,开展微生物数据偏差调查和溯源分析提供依据;企业还可利用鉴定结果建立环境微生物地图,有针对性地控制并消除微生物污染,提高无菌保障水平,确保药品质量安全。
关键词:VITEK;MALDI-TOFMS;16SrRNA/ITS;微生物鉴定
药品微生物污染是影响药品质量、引发临床药害事件的主要因素之一[1]。药品生产区域范围大,物料流转线路长,产品接触微生物概率高,药品在生产过程中易受微生物污染,导致产品微生物指标不合格,轻者产品召回、企业利益和声誉受损,重者则严重危害患者的身体健康。国内的“欣弗事件”和“刺五加事件”就是无菌药品因受微生物污染而对公众健康造成了严重危害和无法挽回的损失。微生物污染也是目前美国FDA药品召回的主要原因之一,2015—2017 年,美国FDA 公布的药品召回事件中,由微生物污染风险引起的召回事件占50%[2]。如何在药品生产的各个环节严格把控微生物污染风险已成为保障药品安全性的重要研究内容。实现药品微生物的有效控制,需要实施有效的污染控制策略,即建立覆盖药品全生命周期的微生物污染监控方案和微生物快速鉴定方法,构建完善的制药环境微生物鉴定信息库,便于开展微生物污染调查与溯源分析,进而通过改善生产工艺,增加中间控制措施,改进清洁或消毒方法,加强人员管理等方式,靶向控制并消除微生物污染,更好地保障药品的安全,这也是监管部门和生产企业努力的方向。
药企对微生物的检测由最初主要依赖人工的传统检测方法,包括观察菌落形态、革兰氏染色镜检、生化鉴定及血清学分型等,后来进展到自动化仪器检测方法,包括VITEK 生化鉴定和基质辅助激光解析电离飞行时间质谱(MALDI-TOF MS)蛋白鉴定,再到近年来逐渐普及的基因序列鉴定等方法。相较传统方法的操作繁琐,耗时长,敏感度低且特异性较差,基因序列鉴定以其快速、准确、灵敏的优势被广泛应用于微生物鉴定及溯源领域,为药企建立微生物数据库提供了技术支撑。
本研究运用VITEK 生化鉴定、MALDI-TOF MS 蛋白鉴定和16S rRNA/ITS 基因测序鉴定3 种技术帮扶药企进行快速鉴定并开展污染分析,进而探讨微生物鉴定结果如何助力完善药企微生物风险控制和质量保障体系。
1材料与方法
1.1 仪器、培养基和试剂
BX53 生物显微镜( 日本奥林巴斯);Color Gram 12 染色仪、VITEK 2 COMPACT 微生物鉴定系统(生物梅里埃);Microflex LT/SH smart 微生物鉴定质谱仪(德国布鲁克);ABI 3500 测序仪(美国赛默飞)。
HCCA portioned(德国布鲁克,批号:602012 2059);TSA 培养基(批号:1100645)、R2A 培养基(批号:1108435)均购自广东环凯公司。
1.2 微生物的收集
连续4 个季度对辖区内某企业无菌制剂高风险生产区中的A/B 级(每次采集)、C/D 级和水系统(取关键点位采集)采集微生物,通过微生物限度检测法(中间体和制药用水)、沉降菌法、浮游菌法、接触碟法(人员和设备表面)进行样本采集及检测,结果显示,A 级环境控制良好,未分离到微生物,B 级共分离到46 株,C 级关键区域(如称量室、配液室)18 株,D 级关键区域(洗瓶室)1 株,水系统关键取样点(总送水点和总回水点)29 株菌。将收集的菌种进行分离、纯化、鉴定,同时用磁珠保存管置−70 ℃保存。
1.3 VITEK 生化鉴定
VITEK 2 Compact 全自动微生物鉴定及药敏分析系统是通过微生物的微量生化反应产生不同的浊度,再由光学仪器判读,从而快速鉴定微生物。对分离纯化获得的菌株进行菌落形态学观察、革兰氏染色,然后根据镜检结果选择相应鉴定卡,按照VITEK 2 Compact 操作程序进行生化鉴定。
1.4 MALDI-TOF MS 蛋白鉴定
MALDI-TOF MS 通过检测微生物的蛋白质指图谱来鉴定微生物。本研究采用甲酸提取法对 菌株进行前处理,再取1 μL 上清液点样于靶板,添加1 μL HCCA 基质,晾干,最后用Microflex LT/SH smart 微生物鉴定质谱仪分析鉴定。
1.5 16S rRNA/ITS 基因鉴定
16S rRNA/ITS 基因鉴定以特征核酸序列作为目标检测物来鉴定微生物。细菌采用16S rRNA 基因(正向引物16SV1F 和反向引物16SV3R),丝状真菌采用ITS 区域序列(正向引物ITS5 和反向引物ITS4),酵母采用D2 区域序列(正向引物D2_NL1和反向引物D2_NL4),进行扩增、测序,测序结果拼接核对后,与经验证的专业数据库进行全局比对,基于相似度获得菌种的鉴定信息。
2结果与分析
2.1环境微生物的鉴定结果
对无菌制剂高风险生产区进行12 个月的持续采样收集微生物,通过VITEK 生化鉴定、MALDI-TOF MS 蛋白鉴定和16S rRNA/ITS 基因测序鉴定技术进行鉴定,共获得89 株细菌和5 株真菌的鉴定结果,再结合样本采集信息,初步构建了融合生化、蛋白、基因鉴定结果的环境微生物鉴定信息库,见表1。由表1 可见,VITEK 生化鉴定和16S rRNA/ITS 基因测序鉴定成功率均为
表1 无菌制剂高风险生产区环境微生物鉴定信息库
Tab. 1 Environmental microbial identification information database for high risk production areas of sterile formulations
|
采样日期 |
采集来源 |
测序鉴定结果 |
质谱鉴定结果 |
VITEK 2 鉴定结果 |
|
2021.12.08 |
c |
Chitinophaga varians |
Unidentified |
Sphingomonas paucimobilis |
|
|
|
多变噬几丁质菌 |
无法鉴定 |
少动鞘氨醇单胞菌 |
|
2021.12.09 |
a |
Pseudomonas juntendi |
Pseudomonas monteilii |
Pseudomonas putida |
|
|
|
顺天堂大学假单胞菌 |
蒙太利假单胞菌 |
恶臭假单胞菌 |
|
2021.12.09 |
a |
Comamonas testosteroni |
Comamonas testosteroni |
Comamonas testosteroni |
|
|
|
睾丸酮丛毛单胞菌 |
睾丸酮丛毛单胞菌 |
睾丸酮丛毛单胞菌 |
|
2021.12.09 |
a |
Pseudomonas juntendi |
Pseudomonas monteilii |
Pseudomonas putida |
|
|
|
顺天堂大学假单胞菌 |
蒙太利假单胞菌 |
恶臭假单胞菌 |
|
2021.12.09 |
a |
Stenotrophomonas indicatrix |
Stenotrophomonas maltophilia |
Stenotrophomonas maltophilia |
|
|
|
指示器寡养单胞菌 |
嗜麦芽窄食单胞菌 |
嗜麦芽窄食单胞菌 |
|
2021.12.09 |
a |
Comamonas testosteroni |
Comamonas testosteroni |
Comamonas testosteroni |
|
|
|
睾丸酮丛毛单胞菌 |
睾丸酮丛毛单胞菌 |
睾丸酮丛毛单胞菌 |
|
2021.12.12 |
e |
Staphylococcus epidermidis |
Staphylococcus epidermidis |
Staphylococcus epidermidis |
|
|
|
表皮葡萄球菌 |
表皮葡萄球菌 |
表皮葡萄球菌 |
|
2021.12.14 |
b |
Comamonas testosteroni |
Comamonas testosteroni |
Comamonas testosteroni |
|
|
|
睾丸酮丛毛单胞菌 |
睾丸酮丛毛单胞菌 |
睾丸酮丛毛单胞菌 |
|
|
b |
Comamonas testosteroni |
Comamonas testosteroni |
Comamonas testosteroni |
|
|
|
睾丸酮丛毛单胞菌 |
睾丸酮丛毛单胞菌 |
睾丸酮丛毛单胞菌 |
|
2021.12.20 |
b |
Staphylococcus saprophyticus |
Staphylococcus saprophyticus |
Sta hylococcus saprophyticus |
|
|
|
腐生葡萄球菌 |
腐生葡萄球菌 |
腐生葡萄球菌 |
|
2021.12.20 |
b |
Haematomicrobium sanguinnis |
Unidentified |
Microbacterium spp. |
|
|
|
未译名 |
无法鉴定 |
微 |
|
2021.12.28 |
a |
Stenotrophomonas indicatrix |
Stenotrophomonas maltilia |
Stenotrophomonas maltophilia |
|
|
|
指示器寡养单胞菌 |
嗜麦芽窄食单胞菌 |
嗜麦芽窄食单胞菌 |
|
2021.12.28 |
a |
Brevundimonas vesicularis |
Brevundimonas vesicularis |
Sphingomonas paucimobilis |
|
|
|
泡囊短波单胞菌 |
泡囊短波单胞菌 |
少动鞘氨醇单胞菌 |
|
2021.12.28 |
a |
Brevibacterium casei |
Brevi acum casei |
Brevibacterium casei |
|
|
|
乳酪短杆菌 |
乳酪短杆菌 |
乳酪短杆菌 |
|
2021.12.28 |
a |
Tsukamurella pulmonis 肺冢村氏菌 |
Tsukam ella paurometabola 稍变(少代谢)冢村氏菌 |
Alicyclobacillus acidoterrestris /acidocaldarius |
|
|
|
|
|
酸土/酸热脂环酸芽孢杆菌 |
|
2021.12.28 |
a |
Sphingomonas pseudosanguinis |
Sphingomonas pseudosanguinis |
Sphingomonas paucimobilis |
|
|
|
假(伪)血鞘氨醇单胞菌 |
假(伪)血鞘氨醇单胞菌 |
少动鞘氨醇单胞菌 |
|
2022.01.05 |
c |
Staphylococcus sap ophyticus |
Unidentified |
Staphylococcus saprophyticus |
|
|
|
腐生葡萄球菌 |
无法鉴定 |
腐生葡萄球菌 |
|
2022.01.06 |
c |
Metaba llus idriensis |
Lactobacillus paraplantarum |
Clavibacter michiganensis |
|
|
|
传染病研究所副芽孢杆菌 |
类植物乳杆菌 |
密歇根棍状杆菌 |
|
2022.01 |
|
Staphylococcus hominis |
Staphylococcus hominis |
Kocuria rhizophila |
|
|
|
人葡萄球菌 |
人葡萄球菌 |
嗜根库克菌 |
|
2022.01 |
d |
Staphylococcus hominis 人葡萄球菌 |
Staphylococcus hominis 人葡萄球菌 |
Staphylococcus hominis ssp. hominis 人葡萄球菌人亚种 |
|
2022.01.12 |
d |
Micrococcus antarcticus |
Micrococcus sp. |
Micrococcus luteus/lylae |
|
|
|
南极微球菌 |
微球菌属 |
藤黄/里拉微球菌 |
|
2022.01.13 |
g |
Paenibacillus glucanolyticus |
Paenibacillus glucanolyticus |
Cronobacter sakazakii group |
|
|
|
解葡糖类芽孢杆菌 |
解葡糖类芽孢杆菌 |
阪崎克洛诺杆菌群 |
|
2022.01.13 |
g |
Paenibacillus glucanolyticus |
Paenibacillus glucanolyticus |
Paenibacillus amylolyticus |
|
|
|
解葡糖类芽孢杆菌 |
解葡糖类芽孢杆菌 |
解淀粉类芽孢杆菌 |
|
2022.01.14 |
g |
Paenibacillus glucanolyticus |
Paenibacillus glucanolyticus |
Paenibacillus amylolyticus |
|
|
|
解葡糖类芽孢杆菌 |
解葡糖类芽孢杆菌 |
解淀粉类芽孢杆菌 |
|
2022.01.14 |
g |
Paenibacillus glucanolyticus |
Paenibacillus glucanolyticus |
Paenibacillus amylolyticus |
|
|
|
解葡糖类芽孢杆菌 |
解葡糖类芽孢杆菌 |
解淀粉类芽孢杆菌 |
|
2022.01.26 |
e |
Staphylococcus warneri |
Staphylococcus warneri |
Staphylococcus warneri |
|
|
|
沃氏葡萄球菌 |
沃氏葡萄球菌 |
沃氏葡萄球菌 |
|
2022.01.26 |
e |
Staphylococcus ureilyticus 解脲葡萄球菌 |
Unidentified 无法鉴定 |
Staphylococcus cohnii ssp.urealyticus |
|
|
|
|
|
科氏葡萄球菌解脲亚种 |
|
2022.01.27 |
e |
Staphylococcus borealis |
Staphylococcus haemolyticus |
Staphylococcus haemolyticus |
|
|
|
挪威北部葡萄球菌 |
溶血葡萄球菌 |
溶血葡萄球菌 |
|
2022.01.27 |
e |
Staphylococcus saprophyticus |
Staphylococcus saprophyticus |
Staphylococcus saprophyticus |
|
|
|
腐生葡萄球菌 |
腐生葡萄球菌 |
腐生葡萄球菌 |
|
2022.01.27 |
e |
Micrococcus luteus |
Unidentified |
Micrococcus luteus/lylae |
|
|
|
藤黄微球菌 |
无法鉴定 |
藤黄/里拉微球菌 |
|
2022.01.29 |
e |
Staphylococcus capitis |
Staphylococcus capitis |
Staphylococcus capitis |
|
|
|
头状葡萄球菌 |
头状葡萄球菌 |
头状葡萄球菌 |
续表1
|
采样日期 |
采集来源 |
测序鉴定结果 |
质谱鉴定结果 |
VITEK 2 鉴定结果 |
|
2022.01.29 |
e |
Micrococcus luteus |
Micrococcus luteus |
Micrococcus luteus/lylae |
|
|
|
藤黄微球菌 |
藤黄微球菌 |
藤黄/里拉微球菌 |
|
2022.02.07 |
b |
Meyerozyma guilliermondii |
Candida guilliermondii |
Candida guilliermondii |
|
|
|
季也蒙迈耶氏酵母 |
季也蒙假丝酵母 |
季也蒙假丝酵母 |
|
2022.02.07 |
b |
Meyerozyma guilliermondii |
Candida guilliermondii |
Candida guilliermondii |
|
|
|
季也蒙迈耶氏酵母 |
季也蒙假丝酵母 |
季也蒙假丝酵母 |
|
2022.02.08 |
a |
Paenibacillus typhae |
Unidentified |
Cronobacter sakazakii group |
|
|
|
香蒲类芽孢杆菌 |
无法鉴定 |
坂崎克洛诺杆菌属 |
|
2022.02.08 |
a |
Paenibacillus xylanexedens |
Paenibacillus amylolyticus |
Sphingomonas paucimobilis |
|
|
|
解木聚糖类芽孢杆菌 |
解淀粉类芽孢杆菌 |
少动鞘氨醇单胞菌 |
|
2022.02.08 |
a |
Pantoea dispersa |
Pantoea dispersa |
Pantoea spp. |
|
|
|
分散泛菌 |
分散泛菌 |
泛菌属 |
|
2022.02.09 |
g |
Bacillus stratosphericus |
Bacillus pumilus |
Bacillus pumilus |
|
|
|
同温层芽孢杆菌 |
短小芽孢杆菌 |
短小芽孢杆菌 |
|
2022.02.09 |
e |
Staphylococcus lugdunensis |
Staphylococcus lugdunensis |
Staphylococcus lugdunensis |
|
|
|
路邓葡萄球菌 |
路邓葡萄球菌 |
路邓葡萄球菌 |
|
|
e |
Micrococcus luteus |
Micrococcus luteus |
Micrococcus luteus/lylae |
|
|
|
藤黄微球菌 |
藤黄微球菌 |
藤黄/里拉微球菌 |
|
2022.02.09 |
c |
Staphylococcus warneri |
Staphylococcus warneri |
Staphylococcus warneri |
|
|
|
沃氏葡萄球菌 |
沃氏葡萄球菌 |
沃氏葡萄球菌 |
|
2022.02.10 |
g |
Bacillus cereus |
Bacillus cereus |
Bacillus cereus/Bacillus thuringiensis |
|
|
|
蜡样芽孢杆菌 |
蜡样芽孢杆菌 |
acillus mycoides 蜡样/金/蕈状芽孢杆菌 |
|
2022.02.17 |
g |
Bacillus infantis |
Bacillus infantis |
Bacillus clausii |
|
|
|
婴儿芽孢杆菌 |
婴儿芽孢杆菌 |
克劳斯芽孢杆菌 |
|
2022.02.17 |
c |
Staphylococcus cohnii |
Staphylococcus cohnii |
Staphylococcus cohnii ssp. cohnii |
|
|
|
科氏葡萄球菌 |
科氏葡萄球菌 |
科氏葡萄球菌科氏亚种 |
|
2022.02.19 |
c |
Staphylococcus cohnii |
Staphylococohnii |
Staphylococcus cohnii ssp. urealyticus |
|
|
|
科氏葡萄球菌 |
科氏葡萄 |
科氏葡萄球菌解脲亚种 |
|
2022.02.19 |
c |
Staphylococcus borealis |
Unidentifie |
Staphylococcus saprophyticus |
|
|
|
挪威北部葡萄球菌 |
无法鉴定 |
腐生葡萄球菌 |
|
2022.02.28 |
d |
Alkalihalobacillus okhensis |
us wakoensis |
Sphingomonas paucimobilis |
|
|
|
奥卡港嗜碱盐芽孢杆菌 |
和光芽孢杆菌 |
少动鞘氨醇单胞菌 |
|
2022.03.04 |
b |
Metaba llus idriensis |
Unidentified |
Sphingomonas paucimobilis |
|
|
|
传染病研究所副芽孢杆菌 |
无法鉴定 |
少动鞘氨醇单胞菌 |
|
2022.03.08 |
b |
Bacillus lichenif mis |
Bacillus licheniformis |
Bacillus licheniformis |
|
|
|
地衣芽孢杆菌 |
地衣芽孢杆菌 |
地衣芽孢杆菌 |
|
2022.03.08 |
e |
Moraxella loensis |
Moraxella osloensis |
Moraxella group |
|
|
|
斯陆莫拉菌 |
奥斯陆莫拉菌 |
莫拉菌群 |
|
2022.03.14 |
c |
Sphingomonas aquatilis |
Sphingomonas aquatilis |
Sphingomonas paucimobilis |
|
|
|
水生鞘氨醇单胞菌 |
水生鞘氨醇单胞菌 |
少动鞘氨醇单胞菌 |
|
2022.03 22 |
g |
Bacillus thuringiensis 苏云金芽孢杆菌 |
Bacillus cereus 蜡样芽孢杆菌 |
Bacillus cereus/Bacillus thuringiensis /Bacillus mycoides 蜡样/苏云金/蕈状芽孢杆菌 |
|
2022.03.31 |
e |
Rhodotorula mucilaginosa 胶红酵母 |
Rhodotorula mucilaginosa 胶红酵母 |
Rhodotorula glutinis/Rhodotorula mucilaginosa |
|
|
|
|
|
粘红酵母/胶红酵母 |
|
2022.04.01 |
e |
Staphylococcus haemolyticus |
Staphylococcus haemolyticus |
Staphylococcus haemolyticus |
|
|
|
溶血葡萄球菌 |
溶血葡萄球菌 |
溶血葡萄球菌 |
|
2022.04.02 |
e |
Staphylococcus petrasii subsp.petrasii |
Staphylococcus petrasii |
Staphylococcus warneri |
|
|
|
未译名 |
佩氏葡萄球菌 |
沃氏葡萄球菌 |
|
2022.04.02 |
a |
Brevibacterium celere |
Unidentified |
Brevibacterium casei |
|
|
|
速生短杆菌 |
无法鉴定 |
乳酪短杆菌 |
|
2022.04.05 |
a |
Tsukamurella pulmonis 肺冢村氏菌 |
Tsukamurella paurometabola 稍变(少代谢)冢村氏菌 |
Alicyclobacillus acidoterrestris/ acidocaldarius |
|
|
|
|
|
酸土/酸热脂环酸芽孢杆菌 |
|
2022.04.07 |
g |
Bacillus pumilus |
Bacillus pumilus |
Bacillus pumilus |
|
|
|
短小芽孢杆菌 |
短小芽孢杆菌 |
短小芽孢杆菌 |
|
2022.04.10 |
c |
Staphylococcus cohnii |
Staphylococcus cohnii |
Enterococcus faecium |
|
|
|
科氏葡萄球菌 |
科氏葡萄球菌 |
屎肠球菌 |
|
2022.04.11 |
a |
Brevibacterium celere |
Brevibacterium sanguinis |
Brevibacterium casei |
|
|
|
速生短杆菌 |
血短杆菌 |
乳酪短杆菌 |
|
2022.04.13 |
a |
Sphingomonas parapaucimobilis |
Sphingomonas parapaucimobilis |
Sphingomonas paucimobilis |
|
|
|
类少动鞘氨醇单胞菌 |
类少动鞘氨醇单胞菌 |
少动鞘氨醇单胞菌 |
|
2022.04.13 |
b |
Chryseobacterium indologenes |
Chryseobacterium indologenes |
Chryseobacterium indologenes |
|
|
|
产吲哚金黄杆菌 |
产吲哚金黄杆菌 |
产吲哚金黄杆菌 |
|
采样日期 |
采集来源 |
测序鉴定结果 |
质谱鉴定结果 |
VITEK 2 鉴定结果 |
|
2022.04.19 |
c |
Pseudomonas zhaodongensis |
Pseudomonas xanthomarina |
Pseudomonas stutzeri |
|
|
|
肇东假单胞菌 |
黄色海假单胞菌 |
斯氏假单胞菌 |
|
2022.04.25 |
c |
Meyerozyma guilliermondii |
Candida guilliermondii |
Candida famata |
|
|
|
季也蒙迈耶氏酵母 |
季也蒙假丝酵母 |
无名假丝酵母 |
|
2022.05.01 |
d |
Micrococcus cohnii |
Micrococcus cohnii |
Alloiococcus otitis |
|
|
|
科氏微球菌 |
科氏微球菌 |
耳炎差异球菌 |
|
2022.05.01 |
c |
Burkholderia cepacia |
Burkholderia cepacia |
Burkholderia cepacia group |
|
|
|
洋葱伯克霍尔德氏菌 |
洋葱伯克霍尔德氏菌 |
洋葱伯克霍尔德菌群 |
|
2022.05.23 |
c |
Dietzia kunjamensis |
Dietzia maris |
Dietzia spp. |
|
|
|
印度冻原迪茨氏菌 |
海迪茨氏菌 |
迪茨菌属 |
|
2022.05.24 |
g |
Meyerozyma guilliermondii |
Candida guilliermondii |
Candida guilliermondii |
|
|
|
季也蒙迈耶氏酵母 |
季也蒙假丝酵母 |
季也蒙假丝酵母 |
|
2022.05.25 |
g |
Peribacillus simplex |
Bacillus simplex |
Bacillus simplex |
|
|
|
简单近芽孢杆菌 |
简单芽孢杆菌 |
简单芽孢杆菌 |
|
2022.05.25 |
c |
Paenibacillus campinasensis |
Paenibacillus lactis |
Sphingomonas paucimobilis |
|
|
|
坎皮纳斯市类芽孢杆菌 |
乳类芽孢杆菌 |
少动鞘氨醇单胞菌 |
|
2022.06.06 |
c |
Luteibacter anthropi |
Unidentified |
Aeromonas salmonicida |
|
|
|
人类藤黄色杆菌 |
无法鉴定 |
杀鲑气单胞菌 |
|
|
c |
Microbacterium paraoxydans |
Microbacterium paraoxydans |
Sphingomonas paucimobilis |
|
|
|
副氧化微杆菌 |
副氧化微杆菌 |
少动鞘氨醇单胞菌 |
|
2022.06.14 |
e |
Brevibacterium celere |
Brevibacterium celere |
Brevibacterium casei |
|
|
|
速生短杆菌 |
速生短杆菌 |
乳酪短杆菌 |
|
2022.08.09 |
d |
Staphylococcus pettenkoferi |
Staphylococcus pettenkoferi |
Staphylo ccus capitis |
|
|
|
皮氏葡萄球菌 |
皮氏葡萄球菌 |
头状葡萄球菌 |
|
2022.08.14 |
c |
Bacillus badius |
Bacillus badius |
Geobactoebii |
|
|
|
栗褐芽孢杆菌 |
栗褐芽孢杆菌 |
堆肥土杆 |
|
2022.08.25 |
c |
Paenibacillus provencensis |
Paenibacillus provencensi |
Sphingom nas paucimobilis |
|
|
|
普罗旺斯类芽孢杆菌 |
普罗旺斯类芽孢杆菌 |
少动鞘氨醇单胞菌 |
|
2022.09.23 |
d |
Kytococcus schroeteri 斯氏皮肤球菌 |
Kytococcus sc oeteri 斯氏皮肤 |
Dermacoccus nishinomiyaensis/ Kytococcus sedentarius 西宫皮球菌/坐皮肤球菌 |
|
2022.10.25 |
g |
Cytobacillus oceanisediminis |
Bacillus firmus |
Bacillus firmus |
|
|
|
大洋沉积物纤维芽孢杆菌 |
强芽孢杆菌 |
坚强芽孢杆菌 |
|
2022.10.25 |
e |
Naganishia diffluens |
Crypto ccus diffluens |
Cryptococcus albidus |
|
|
|
流散长西氏酵母 |
散隐球菌 |
浅白隐球菌 |
|
2022.10.28 |
b |
Sphingomonas panaciterrae |
Unidentified |
Brevundimonas diminuta/vesicularis |
|
|
|
鱼池鞘氨醇单胞菌 |
无法鉴定 |
缺陷/泡囊短波单胞菌 |
|
2022.11.01 |
b |
Ponticoccus gilvus |
Unidentified |
Micrococcus luteus/lylae |
|
|
|
海滑行球菌属 |
无法鉴定 |
藤黄/里拉微球菌 |
|
2022.11.02 |
c |
Oceanobacillus kimchii |
Oceanobacillus kimchii |
Pasteurella canis |
|
|
|
泡菜大洋芽孢杆菌 |
泡菜大洋芽孢杆菌 |
犬巴斯德菌 |
|
2022.11.08 |
b |
iestia aryabhattai |
Bacillus megaterium |
Bacillus megaterium |
|
|
|
阿氏普里斯特氏菌 |
巨大芽孢杆菌 |
巨大芽孢杆菌 |
|
2022.11.14 |
f |
Staphylococcus capitis |
Unidentified |
Staphylococcus capitis |
|
|
|
头状葡萄球菌 |
无法鉴定 |
头状葡萄球菌 |
|
2022.11.28 |
d |
Brevundimonas naejangsanensis |
Brevundimonas diminuta |
Brevundimonas diminuta/vesicularis |
|
|
|
内藏山短波单胞菌 |
缺陷短波单胞菌 |
缺陷/泡囊短波单胞菌 |
|
2022.12.22 |
f |
Staphylococcus ureilyticus |
Unidentified |
Staphylococcus cohnii ssp. cohnii |
|
|
|
解脲葡萄球菌 |
无法鉴定 |
科氏葡萄球菌科氏亚种 |
|
2022.12.22 |
f |
Staphylococcus ureilyticus |
Unidentified |
Staphylococcus carnosus ssp.carnosus |
|
|
|
解脲葡萄球菌 |
无法鉴定 |
肉葡萄球菌肉球亚种 |
|
2022.12.22 |
f |
Streptococcus agalactiae |
Streptococcus agalactiae |
Streptococcus agalactiae |
|
|
|
无乳链球菌 |
无乳链球菌 |
无乳链球菌 |
|
2022.12.28 |
f |
Staphylococcus epidermidis |
Unidentified |
Staphylococcus epidermidis |
|
|
|
表皮葡萄球菌 |
无法鉴定 |
表皮葡萄球菌 |
|
2022.12.29 |
f |
Staphylococcus cohnii |
Unidentified |
Staphylococcus cohnii ssp. cohnii |
|
|
|
科氏葡萄球菌 |
无法鉴定 |
科氏葡萄球菌科氏亚种 |
|
2023.01.13 |
c |
Staphylococcus borealis |
Unidentified |
Staphylococcus hominis ssp. hominis |
|
|
|
挪威北部葡萄球菌 |
无法鉴定 |
人葡萄球菌人亚种 |
|
2023.01.16 |
f |
Cytobacillus kochii |
Bacillus kochii |
Brevibacillus choshinensis |
|
|
|
科赫氏纤维芽孢杆菌 |
科赫氏芽孢杆菌 |
铫子短小芽孢杆菌 |
|
2023.01.16 |
f |
Janibacter limosus 泥两面神菌 |
Janibacter indicus 印度两面神菌 |
Alicyclobacillus acidoterrestris/ acidocaldarius 酸土/酸热脂环酸芽孢杆菌 |
|
2023.01.16 |
f |
Cytobacillus gottheilii |
Unidentified |
Brevibacillus choshinensis |
|
|
|
戈特海尔氏纤维芽孢杆菌 |
无法鉴定 |
铫子短小芽孢杆菌 |
注:a-纯化水;b-注射用水;c-沉降菌;d-浮游菌;e-人员表面微生物;f-设备表面微生物;g-注射剂中间体。
Note: a-purifiedwater;b-waterforinjection;c-sedimentationmicroorganism;d-planktonicmicroorganism;e-microorganismonthesurfaceofpersonnel; f-microorganism on the surface of the equipment; g-injection intermediate.
100.0%(94/94),质谱鉴定成功率为79.8%(75/94)。基于属水平统计,质谱与测序鉴定结果一致的占比为68.1%;VITEK 与测序鉴定结果一致的占比为64.9%;企业可根据自己的需求选择合适的鉴定方法,如多种技术鉴定结果有冲突,建议以测序鉴定结果为准。
无菌制剂高风险生产区环境微生物鉴定信息库仍需要不断完善,这是一个动态持续的过程。企业可根据鉴定结果开展相关分析,有针对性地控制并消除微生物污染,降低微生物负荷,提高无菌保障水平,为企业后续开展风险评估、溯源分析、污染调查提供技术支持,保障药品质量安全。
2.2无菌制剂高风险生产区微生物形态学分析
通过形态学上统计分析可发现,革兰氏阳性球菌占35.1%、革兰氏阳性芽孢杆菌占25.5%、革兰氏阴性杆菌占25.5%、革兰氏阳性杆菌占7.4%、酵母占6.4%。革兰氏阳性球菌和革兰氏阳性芽孢杆菌共占比60.6%,是洁净区常见污染菌类型。此企业环境微生物检出最多的是革兰氏阳性球菌,表明人员仍是洁净区最大的污染源,这与报道的制药企业日常微生物监控数据基本一致[3]。建议企业加强人员管理,提升所有员工的污染控制意识,最大程度降低由人员引起的微生物污染风险。同时要重视对芽孢杆菌的有效杀灭,该类菌的特点是细胞壁厚,孢子耐热、抗氧化能力极强,是一类难以杀灭的微生物,国际上也将该类菌列为产品中不可接受微生物[4]。企业日常使用38%甲醛熏蒸等进行空间消毒,表明上述消毒方式未能完全消灭芽孢杆菌,因此需选用更强效的杀孢子剂。
2.3无菌制剂高风险生产区B 级环境微生物分析
A/B 级是无菌生产的核心区,对该区域监测到的微生物都要明确鉴定并采取控制措施。无菌制剂高风险生产区A 级未监测到微生物;B 级环境共检出环境污染菌46 株,其中从人员表面分离的有18 株、设备表面7 株、沉降菌18 株、浮游菌3株。分析发现,葡萄球菌是主要污染菌,占比45.7%,芽孢杆菌占比17.4%,微球菌占比6.5%,酵母菌占比4.3%,伯克菌、短波单胞菌、链球菌、莫拉菌、鞘氨醇单胞菌分别占比2.2%,其他占比15.2%。葡萄球菌主要采集于人员表面,并以气锁室(出)、灌装三更车间尤为明显,此区域是人员更衣活动的主要场所,因此车间日常应注意控制洁净区人员数量、加强更衣规范、减少人员的不必要活动。芽孢杆菌采集于沉降菌和设备表面,以灭菌后暂存室层流和轧盖室尤为明显,此区域与A级生产区紧密相连,需引起高度重视,说明车间日常应提高空间消毒频率,设备表面消毒应选用适宜的杀孢子剂。
在粉碎混合包装室用沉降菌法分离到1 株致病微生物—— 洋葱伯克霍尔德菌(Burkholderia cepacia,BC),其隶属于洋葱伯克霍尔德菌复合群(Burkholderia cepacia Complex,BCC)。BCC作为不可接受微生物[5],能通过代谢调节、细胞形态改变,长期存活于土壤和水中,对细菌抑制剂和抗菌药物有强大的耐受力,可在多种药物中生长和增殖[6-7]。该位置分离到BCC 的可能原因为空间环境控制不当,BCC 通过物料携带或工具的传递进入洁净区。因此出入人员应严格遵守更衣和物品传递程序,同时企业应制定科学合理的清洁消毒程序,尽量减少由人员和环境控制不当导致的污染。
2.4无菌制剂高风险生产区制药用水微生物分析
水系统微生物的风险控制是药品全生命周 期质量管理的重要一环。在制药用水关键取样点共检出污染菌29 株,其中纯化水分离的有18 株,注射用水11 株。分析发现,水系统中污染微生物主要为革兰氏阴性菌(从毛单胞菌、假单胞菌、鞘氨醇单胞菌和短波单胞菌等),占污染微生物总数的58.6%,符合制药用水系统中微生物绝大多数为革兰氏阴性菌的报道[8],见图1。革兰氏阴性菌在水系统中易形成生物膜,生物膜的检测和去除十分困难,从而成为微生物污染的持续来源。此外,在制药用水检测到葡萄球菌,推测是来自人员取样和检测过程的不当操作,因此需要对检测人员加强培训,严格执行无菌操作,避免污染。
3讨论
3.1企业加强对不可接受微生物的控制
企业通过建立环境微生物数据库,确定对应自身生产环境的不可接受微生物列表,才能更有效地采取针对性手段,避免其最终污染产品。根据表1 可知企业检测到致病菌BCC 以及种类多样且高频出现的芽孢杆菌属等,对于出现的此类不可接受微生物,在今后环境监控过程中要格外注意采样点,对每年环境检测数据进行风险评估,针对高风险点可增加采样频次。从此次数据来看,人员、中间体为高风险区域,可增加采样频次,而一些经常被忽视的连接区域,比如原料混合包装室、轧盖区,也应引起重点关注。真菌,尤其是霉菌是洁净区更不可接受微生物。真菌可以通过孢子繁殖,一旦污染很容易发生扩散,还能形成生物膜,难以杀灭,药企必须加强这方面的防控。缺乏对真菌污染的有效识别是目前制药行业的一个令人担忧的现状。准确的丝状真菌鉴定技术通常使用18S rRNA/ITS 基因测序,也可选择微生物质谱结合丝状真菌数据库来快速鉴定。
为预防不可接受微生物污染,药企更要在源头上进行控制,需制定有效的消毒灭菌手段,如提高空间消毒频率,加强设备清洁,注意去除死角、不易清洁部位的尘埃,交替使用杀孢子剂等;还要制定更为合理的洁净区人员管理程序及环境检测程序,比如企业在制定环境检测程序时,霉菌采集可选择适宜霉菌生长的沙氏琼脂培养基,采样时应严格按照无菌操作,避免增加人员污染。在人员采样方面,最好1人采样1人复核,双人操作使数据更加可靠。
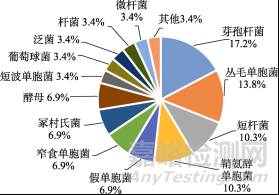
图1 无菌制剂高风险生产区水系统优势菌检出率
Fig. 1Detection rate of dominant bacteria in the water system of high-risk production areas for sterile preparations
3.2指导企业菌种鉴定手段的选择
生化鉴定、蛋白鉴定和基因鉴定这3 种技术均有其适用领域及优缺点,菌种鉴定手段的合理选择对于药品质量控制来说至关重要。在实际应用中,药企环境污染菌的鉴定可根据自身条件、鉴定目的、不同区域风险等级,综合3 种鉴定方法的特点,选择1~3 种不同的鉴定技术,组合成多相鉴定的整套方案[9],以满足控制菌检查、环境监控、溯源分析、风险评估等需要,提高药品微生物控制水平,更好地保障药品质量。比如,对该企业来说,采集到的菌株来源如为洁净区低到中等风险区域,日常污染菌鉴定采用VITEK 生化鉴定结合MALDI-TOF MS 蛋白鉴定技术,基本可满足将菌种鉴定到属水平,部分甚至能鉴定到种水平;对洁净区风险较高的区域,比如B 级环境下的A 级层流、注射剂中间体等,采集的菌株可采用上述任一方法结合基因鉴定技术,基本可将菌株鉴定到种水平,达到分析要求。
3.3微生物数据偏差(microbiological data deviation,MDD)调查
微生物实验室出现不合规范的结果通常称为MDD。MDD 调查分为2 个阶段,第1 阶段仅限于实验室内,焦点集中于确定试验是否无效,第2阶段是全面的调查,目的是确定产品不合格的根本原因。制药环境微生物鉴定信息库包括菌株来源、采样时间、鉴定结果等相关信息,可为第2阶段的调查提供技术支撑,尤其可为微生物污染的精准溯源奠定基础。例如,企业如果在某次产品微生物限度检验中检出BCC,建议企业偏差调查过程按下列步骤进行:首先进行实验室调查回,查看有无微生物分析的明显错误以及阴阳性对照出现问题等情况,排除试验因素后,再开展全面调查(含生产调查),包括人、机、料、法、环等环节,涵盖近期实验、生产环境的监测数据、水系统的检测数据、空调系统的运行、压差、设备和人员的消毒等以及和历史环境微生物鉴定信息库的比对情况(本次研究中在粉碎混合包装室用沉降法检出1 株BCC),同时增加检出批次以及前后各3 批终产品(包括原辅料)的多次检测,实验、生产环境增加环境监测频次(包括沉降、浮游、表面采样、悬浮粒子),查看是否再次检出BCC,从而判断是偶发性原因还是真实污染;最后是开展微生物鉴定和溯源分析,比对同种菌的鉴定信息,包括VITEK、微生物质谱、16S rRNA 测序鉴定结果的一致性,有条件的实验室还可以进行全基因组测序,进一步比对其同源性,根据试验及比对结果开展溯源调查,精准定位污染区域,确定偏差原因,作出调查结论并进行批处置(销毁或者符合工艺流程的再灭菌等)和对应的环境消杀、工艺改进等措施。
由于微生物试验的固有特性导致MDD 调查难度大,基于制药环境微生物鉴定结果分析的MDD调查方案的完善还需要多方面努力,包括长期持续收集环境微生物数据、快速精准地鉴定等。
3.4建立企业环境微生物地图
微生物地图是微生物监测数据和鉴定结果的可视化呈现,具体是指通过对药品生产过程监控收集的污染微生物进行鉴定,从鉴定信息和采样来源等方面进行分析,获取药品生产区域污染微生物的分布和迁移规律[10]。其应用于微生物污染防控中的效果取决于环境监测计划中微生物采样点的分布,采样方式、采样频率的设置和鉴定策略的选取。采样点的选取,应评估各取样点的代表性,从最有可能导致产品污染的位置取样,从而有效反映取样环境的洁净度;采样方式为通过微生物限度检测法(中间体和制药用水等)、沉降菌法和浮游菌法(空间环境)、接触碟法(人员和设备表面等)进行样本采集及检测;采样频率应根据环境的洁净度等级、生产频率、产品特性来决定。对收集的微生物选择合适的方法进行鉴定,可将鉴定结果在生产车间平面图上对应的区域标记出来,并用不同颜色表示不同微生物种类,不断补充丰富,形成完善的环境微生物地图,从而反映洁净区微生物群落分布和转变规律;通过密切关注重点区域微生物变化特点,在趋势变化或发生异常时,可及时发现污染微生物及来源、推断特定微生物可能的扩散路径,并开展溯源分析和污染调查,进而降低终产品微生物污染风险。例如,本次研究在中间体中收集到1 株季也蒙迈耶氏酵母,此酵母之前在注射用水中检出过2 次,3 株酵母根据鉴定信息进行同源性分析来源于同一株菌,中间体是在C 级背景下的配液室进行配制的,该房间使用最多的溶剂就是注射用水,根据微生物地图推测该酵母可能是通过注射用水携带进入配液室并存活在该房间,进而污染该批次的中间体。
微生物地图建成后,企业还可根据不同区域的微生物种群分布情况,选取不同的消毒方式进行有效消杀,增加染菌区域和人员手部的消毒频次,提高无菌保障水平;也可从中挑选优势菌及危害大的致病菌作为环境代表菌,以验证消毒剂的消毒效果,这可以作为日常消毒是否有效的重要评价指标之一;培养基模拟灌装试验,除按照中国药典要求加入促生长能力试验使用的标准菌株外,也可考虑加入环境微生物地图中显示的优
势菌。因此,建立环境微生物地图是药企管理环境污染菌的趋势。
4小结
本研究采用多种微生物鉴定技术,建立了制药企业高风险生产区域的环境微生物鉴定信息数据库,并结合微生物形态学和来源信息进行分析,旨在帮助药企在发现不良趋势和异常时,能及时采取有效措施,防止污染事件发生。随着研究的不断深入,数据库将会更加全面和完善,可为企业开展偏差调查、污染溯源以及日常微生物监控提供技术支持,并为监管部门实现高效监管和风险防控提供新思路。
REFERENCES
[1]HOU K L, HUANG L, FENG Y F. Retrospective analysis of drug qualitary related medication misadventure in China[J]. Chin J Hosp Pharm( 中国医院药学杂志), 2020, 40(6): 640-643.
[2]WU Y W, WANG Y, CHE t al. Review and analysis of international m bial contamination-related drug recalls from 2013 to 2019[J]. Chin J M Appl P arm(中国现代应用药学),
2021, 38(15): 1870-1877.
Q H, WANG Y. Identification and population analysis of m croorganisms in sterile drug manufacturing environment[J]. Chin Pharm Aff(中国药事), 2019, 33(12): 1411-1418.
[1]ZHENGXL,WANGZN, WANG ZJ, etal. Establishmentoftheenvironmentallymicrobiallibraryinthedrugsterilitytesting laboratory[J]. Chin J Mod Appl Pharm(中国现代应用药学), 2015, 32(7): 847-850.
[5]USP-NF. <60>Microbiological examination of nonsterile products tests for burkholderia cepacia complex[S]. 2019.
[6]GAN Y Q, NONG J, HUANG H, et al. Rationality evaluation of prescription of bacteriostatic agent and analysis of contaminated bacteria of methadone hydrochloride oral solution[J]. Chin J Pharm Anal(药物分析杂志), 2020, 40(12): 2193-2200.
[7]YANG X F, CAI R. Study on the detection method of Burkholderia cepacia in Pudilan Xiaoyan oral liquid and purified water[J]. Chin Med Mod Distance Educ China(中国中医药现代远程教育), 2022, 20(1): 143-145.
[8]ZHENG X L, WANG Y H, CAO W, et al. Establishment andanalysisofmicrobiallibraryinpharmaceuticalwatersystemofhigh-riskinjectionmanufacturer[J]. ChinJModApplPharm(中国现代应用药学), 2021, 38(9): 1065-1068.
[9]LI H, YU M, LIU L K, et al. Research progress on the
application of modern microorganism identification technology in pharmaceutical quality control[J]. Chin J Pharm(中国医药工业杂志), 2021, 52(3): 312-319.
[10]SONG M H, LI Q Q, QIN F, et al. Establishment and data analysis of a contaminated microorganisms library for sterile pharmaceutical production processes[J]. Chin J Pharm Anal(药物分析杂志), 2019, 39(11): 1954-1960.

来源:Internet


