今日头条
海思科糖尿病小分子新药获批临床。海思科1类化药HSK34890片获国家药监局临床试验默示许可,拟开展用于治疗“2型糖尿病”的临床试验。HSK34890通过以葡萄糖浓度依赖的方式增强胰岛素分泌,改善糖耐量,抑制胰高血糖素分泌,并能够延缓胃排空,抑制食欲及摄食,从而达到降低血糖的作用。临床前研究显示,HSK34890在体外具有良好的药理活性,有望为2型糖尿病患者提供一种新的治疗选择。
国内药讯
1.科伦博泰TROP2-ADC乳癌III期临床积极。科伦博泰创新TROP2-ADC"注射用SKB264"(MK-2870)治疗既往经二线及以上标准治疗的不可切除、局部晚期、复发或转移性三阴性乳腺癌的III期临床达到主要终点。经独立评审委员(IRC)评估,与对照标准化疗相比,SKB264治疗显著提高患者的无进展生存期(PFS)。科伦博泰计划近期与CDE沟通关于SKB264递交上市申请的事宜。
2.苏州华道CD19靶向CAR-T获批临床。华道生物针对CD19抗原开发的CAR-T疗法“HD CD19 CAR-T细胞”获国家药监局临床试验默示许可,临床适应症为用于难治或复发的B细胞急性淋巴细胞白血病成人患者的治疗。该CAR-T疗法使用慢病毒转导自体T细胞,使T细胞表达特异性结合CD19抗原的CAR结构,从而达到治疗CD19阳性肿瘤的效果。目前,华道生物正在中国、美国、澳大利亚等多个国家同步开展该新药的临床试验。
3.北京质肽GLP-1R激动剂获批AD临床。北京质肽生物1类生物制品ZT002注射液第三项适应症获国家药监局临床试验默示许可,拟开发用于治疗阿尔茨海默病。ZT002是一款新型GLP-1R激动剂,拥有较长的半衰期,有望实现每月仅需注射1次,提高患者的依从性。此前,该产品用于糖尿病和减重的适应症均已获得国家药监局的临床批件。
4.上海原启GPRC5D靶向CAR-T获批临床。原启生物靶向GPRC5D嵌合抗原受体自体T细胞注射液(OriCAR-017)获国家药监局临床试验默示许可,拟开发用于治疗复发难治多发性骨髓瘤(MM)。OriCAR-017用于治疗复发/难治MM患者已在研究者发起的Ⅰ期临床中显示治疗潜力。最新数据显示,中位随访时间为280天,总体缓解率(ORR)达到100%,严格意义的完全缓解(sCR)达到80%。在美国,该新药已获得FDA授予孤儿药资格。
5.凯思凯迪融资1.4亿推进FXR激动剂开发。凯思凯迪宣布完成1.4亿元融资,以用于加速推进其新型FXR激动剂CS0159在中美两国同步开展Ⅱ期临床,评估用于治疗非酒精性脂肪性肝炎(NASH),以及治疗原发性硬化性胆管炎(PSC)的潜力。此前,CS0159已获得FDA快速通道资格、孤儿药资格。此轮融资也将用于该公司3个创新药物分子的IND申报与Ⅰ期临床的推进。
国际药讯
1.Blueprint公司RET抑制剂获FDA完全批准。Blueprint Medicines与基因泰克开发的RET抑制剂Gavreto(pralsetinib)获FDA由加速批准转变为完全批准,用于治疗RET融合阳性的非小细胞肺癌。临床数据显示,pralsetinib在既往接受过含铂化疗的患者中达到63%的总缓解率(ORR),中位DOR为38.8个月;在初治患者中,ORR为78%,中位DOR为13.4个月。
2.阿柏西普高剂量制剂长期疗效积极。再生元8mg剂量水平的aflibercept用于治疗湿性年龄相关性黄斑变性(wAMD)患者的关键PULSAR研究96周随访结果积极。此前,该试验已达到主要终点,与每8周给药一次的阿柏西普2mg相比,每12周或每16周一次的阿柏西普8mg在改善最佳矫正视力(BCVA)评分方面显示非劣性。最新数据显示,绝大多数接受8mg aflibercept治疗的wAMD患者能够保持或进一步延长给药间隔。
3.ALX Oncology终止CD47抑制剂两项临床。ALX Oncology公司CD47抑制剂(SIRPα融合蛋白)Evorpacept(ALX-148)联合阿扎胞苷治疗骨髓增生异常综合征(MDS)患者的I/II期研究(ASPEN-02)未达到主要研究终点。与阿扎胞苷单药相比,evorpacept联用阿扎胞苷的治疗效果未达到优效性标准;药物总体耐受性良好。ALX Oncology公司计划终止Evorpacept的ASPEN-02项目,以及终止evorpacept联合阿扎胞苷+维奈克拉治疗急性髓系白血病(AML)的ASPEN-05项目。
4.CG Oncology公司融资推进膀胱癌溶瘤病毒上市。CG Oncology公司宣布完成由新投资者Foresite Capital和TCGX共同领投的1.05亿美元(约7.6亿人民币)融资。此轮融资将用于继续推进膀胱癌溶瘤病毒疗法CG0070以获得FDA的监管批准。CG0070目前处于单药治疗卡介苗(BCG)无应答的非肌层浸润性膀胱癌(NMIBC)的Ⅲ期临床开发当中;该药与PD-1抑制剂联合治疗膀胱癌的Ⅱ期临床也在进行当中。乐普生物拥有该新药的中国开发权益。
5.RNA药物公司ADARx完成C轮融资。ADARx公司宣布完成2亿美元C轮融资,以用于进一步推进其RNA靶向技术平台,创新mRNA沉默或RNA编辑候选药物的开发,以及支持其先导项目(包括ADX-324和ADX-038)用于IND申请的(IND-enabling)临床前毒理学研究。ADX-324是治疗遗传性血管性水肿的创新疗法;ADX-038靶点是补体因子B,拟开发用于治疗多种补体介导的疾病。
6.司美格鲁肽2023年H1营收超660亿元。近日,诺和诺德公布2023年上半年业绩报表,净销售额1076.67亿丹麦克朗,同比增长29%,净利为392.42亿丹麦克朗,同比增43%。2023年H1,司美格鲁肽系列产品合计营收621.66亿丹麦克郎,约合91.3亿美元(折合人民币约660.86亿元),其中皮下注射制剂Ozempic(用于降糖)营收达417.41亿丹麦克朗(+58%);口服片剂Rybelsus(用于降糖)销售额达83.44亿丹麦克朗(+97%),减重产品Wegovy销售额则达120.81亿丹麦克朗(+367%)。
医药热点
1.京津冀骨肿瘤专科联盟成立。8月6日,天津市天津医院与北京积水潭医院、河北医科大学第三医院共同牵头组建的京津冀骨肿瘤专科联盟正式成立。该联盟的成立,旨在联盟汇集京津冀三地16家三级医院搭建平台、整合资源,促进优质医疗资源扩容和均衡布局,为京津冀地区乃至华北、东北地区的骨肿瘤疾病患者提供精准诊疗和防控管理。
2.全国规模最大肛肠专科医院项目封顶。近日,全国规模最大肛肠专科医院项目——深圳市中医肛肠医院(福田)新址建设工程举行主体封顶仪式。该项目位于福田区梅林片区梅坳一路和五路交界处,总投资约8.45亿元,总工期1096天,总建筑面积约为7.02万平方米。整体项目建设完成后,预计总共增加420张床位。
3.阿斯利康中国架构调整。8月14日,阿斯利康中国宣布团队架构调整和相关人事变动。阿斯利康中国将呼吸、消化及自体免疫事业部正式拆分为两大事业部:呼吸吸入和生物制剂事业部;呼吸雾化、消化、疫苗和免疫疗法、自体免疫事业部。林骁将担任呼吸吸入和生物制剂事业部负责人,同时他还将担任香港及澳门地区负责人,并接任公司南区SMT sponsor。陈曦将加入阿斯利康中国,担任呼吸雾化、消化、疫苗和免疫疗法、自体免疫事业部负责人,同时担任阿斯利康中国副总裁、SMT成员,向阿斯利康中国总经理赖明隆先生汇报。
评审动态
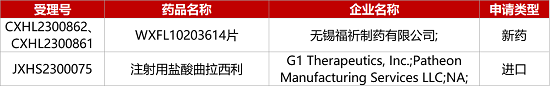
1. CDE新药受理情况(08月14日)
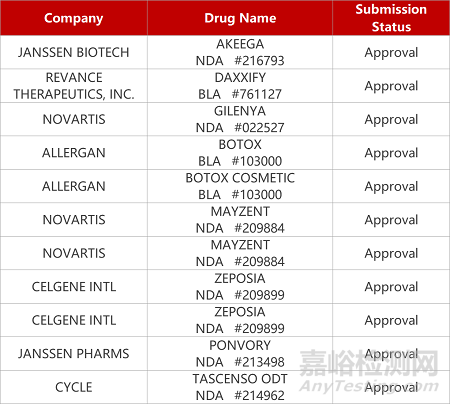
2. FDA新药获批情况(北美08月11日)