您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-10-18 21:19
本篇主要介绍无创测血糖技术之微波法及电化学方法。重点解析微波法及电化学方法技术原理和问题点以及研究现状。
一、微波法
1. 原理
微波是波长在1毫米到1米之间的电磁波,对应着300GHz到300MHz之间的频率,可以很容易穿透毫米厚的生物组织,尤其是在低频范围内,具有一些光学检测方法所没有的优势。微波辐射的单个光子的能量较低,在大气中的散射较少,因此微波可以穿透更深的组织,获得更真实的血糖数据。另外,微波的反射、透射和吸收与组织的介电特性密切相关,而组织的介电常数又是随着葡萄糖的浓度而变化的。基于上述原理,可以开发用于测量血糖的微波传感器。
2. 问题点及研究现状
正常组织与异常组织之间介电特性的差异是微波检测的核心。近年来,在无创连续血糖监测中,血液或其他生物液体中葡萄糖浓度与其介电特性的相关性引起了许多研究者的关注,并引起了对微波传感器的进一步研究1。
对于微波传感器来说,找到血糖水平与有效介电常数之间的关系仍然是一个核心挑战。目前的研究主要集中在如何提高微波传感器的特异性和灵敏度。就特异性而言,组织的介电性质只是一个平均值,其变化可能是由组织的多种成分的变化组合而成。如何将介电特性的测量变化归因于血糖可能需要后续的持续探索。有关研究表明1,多传感器集成、大数据计算和机器学习技术在一定程度上削弱了内部和外部因素的影响。就灵敏度而言,人体血糖浓度的变化只会对介电特性产生轻微的变化,这需要一个高度敏感的传感器。这也意味着,不仅需要有一个高精度、高稳定性、多频谐振器来衰减噪声的影响,还需要随后采用适当的信号处理技术,在振幅变化较大的情况下提取低振幅变化的信号1。
总体而言,微波传感器在无创血糖领域受到许多研究人员的青睐,主要因为其高穿透深度、非电离、低成本和便携性,具有广阔的发展前景。然而,微波技术的灵敏度和特异性仍然是限制发展的主要因素,未来应该在这两个方面做出进一步的努力。
二、电化学方法
1. 反向离子导入(RI)技术
1.1 原理
经皮反向离子导入(RI)是一种无针技术,它可以通过完整的皮肤提取生物分子包括血糖,以达到检测血糖的目的。这里需要说明的是RI技术提取的是组织间液中的血糖1。
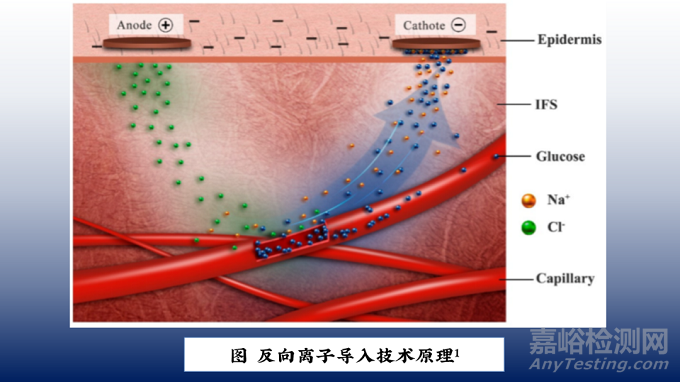
如上图所示,RI涉及两种机制:(i)电迁移,即带电离子和外加电场之间的直接相互作用,以及(ii)电渗透,即从阳极流向阴极的连接溶剂。对于带电部分,电迁移是主要的传输机制。总电荷传输量取决于电场的强度和持续时间。对于不带电部分,电压驱动的电渗透是主要的提取机制。Na+作为主要的电荷载体,电迁移形成了从阳极到阴极的离子电流。组织间液(ISF)中的离子主要由Na+和Cl-组成, 而在正常生理条件下,表皮带负电,因此皮肤会促进Na+的运输,导致Na+的电迁移数大于Cl-. 因此,在RI期间,阳极上的NaCl减少,阴极侧的NaCl增加。这种电化学梯度促进了水从阳极向阴极的渗透流动,ISF中的中性分子也沿着渗透方向向阴极移动。因此,RI可以从阴极提取阳离子和中性物质,从阳极提取阴离子。
1.2 问题点及研究现状
然而,有多种因素可能会影响葡萄糖分子的提取效果:
(1) 表皮厚度
通常情况下,皮肤越厚,渗透性越低,提取效果越差。根据种族、年龄、性别、皮肤状况和疾病状态等,不同个体的皮肤厚度差异很大。
(2) 电流强度
一般情况下,RI采用直流电,电流强度与提取量几乎呈线性关系。电流强度的增加可以增加离子迁移,但随着电流强度的不断增加,迁移速率趋于稳定,表明已经达到饱和状态。此时,电流强度的进一步增加对离子迁移没有显著贡献。
(3) 恒流还是脉冲电流
如果持续向皮肤施加直流电,可能会导致表皮刺痛和红斑。脉冲电流可以有效地减少这种副作用并且可以让患者忍受更高水平的电流。
(4) 电流持续时间
当电流强度恒定时,葡萄糖提取与施加电流的持续时间成正比。皮肤可以在一段时间内恢复正常。但当皮肤长时间暴露在高电流下时,会发生不可逆的损伤。通常,电流强度应在01至03mA之间,每次持续时间不应超过20分钟。
(5) 电极材料
电极的大小、形状和位置也是RI的关键因素。电流密度与电极尺寸密切相关。电极有多种形状,比如薄圆盘形(如GlucoWatch)等。不仅要求电极与人体皮肤紧密相连,还要求电极与皮肤表面保持适当的微小距离。因此,电极通常选用柔性材料和柔性设计。早期研究中会使用铝、铂和锌电极,但它们会导致水电解,从而导致pH值变化,并产生积聚在皮肤表面和电极上的气体,干扰电流分布。为了避免水在电极上发生电化学反应,通常使用低氧化还原电位的材料。例如,Ag/AgCl电极具有良好的生物相容性、可逆性和耐pH变化性,是RI电极材料的合适材料。
RI测血糖技术其实在二十年前就已经实现了商业化,GlucoWatch就是一个典型代表,2001年3月经FDA批准上市。它大致由水凝胶盘、离子导入电极和生物传感器组成。水凝胶圆盘含有GOx,它与RI提取的葡萄糖发生反应。当该装置像手表一样佩戴时,会产生电流(300µA),影响皮下分子。在电场的影响下,正离子向阴极终端移动,负离子向阳极移动,中性葡萄糖分子由于电渗的影响向阴极移动。传感器可以识别转移的电子数量与提取的葡萄糖分子的比例。通过数据转换算法将当前信号转换为相应的血糖水平。
但是,GlucoWatch有很多局限性,如需要使用标准血糖仪进行校准,预热时间长,每12小时需要更换一次垫片,设备在出汗时不能使用,长时间的电流会对用户的皮肤造成损伤等。该设备在2007年停止销售。然而,GlucoWatch是FDA批准的第一个使用RI技术上市的无创血糖监测产品,对后来的许多RI传感器产生了非常深远的影响。
2. 无创体液(唾液、眼泪、汗液和组织间液(ISF))葡萄糖监测
2.1 原理
无创体液测量法通过测量便于采集的体液中某些成分的变化,间接推算出血糖的含量。国内外学者尝试用到的体液主要包括:唾液、泪液、汗腺、呼出气体、组织间液等,研究团队众多。下面举一个商业化的例子。
谷歌血糖检测隐形眼镜,通过使用一个特殊的镜片检测眼泪中的葡萄糖浓度来预测身体葡萄糖浓度,该项目于2014年启动,通过植入隐形眼镜中的微型传感器检测泪液中的葡萄糖含量,但是2018年该项目被中止,原因是临床研究表明泪液葡萄糖和血糖浓度之间的相关性不满足医疗器械的要求。谷歌表示,它确实在受控环境中取得了一定成功,但由于眼睛所处的动态环境,在实际测试中的表现却不尽人意。其技术挑战已经超过了谷歌的能力范围。
谷歌之后,以泪液作为生物标志物的血糖检测隐形眼镜的研究仍在其他研究团队中进行,开发了诸如石墨烯-AgNW复合传感器和安培传感器,通过使用葡萄糖氧化酶来检测泪液中的葡萄糖,因此泪液仍然是进行无创血糖检测的一个非常有前途的靶点。此外,在最新的研究报道中,研究人员利用分子印迹聚合物(MIP)成功检测到尿液中的葡萄糖含量,这一发现使得尿液有可能成为新的血液替代物用于无创血糖检测2。
2.2 问题点及研究现状
上述体液检测方法虽然测量方式简单,但是体液中的葡萄糖浓度与血液中的葡萄糖浓度并没有明显的相关性,所以测量准确性缺乏基础性的原理支撑2。各体液检测的问题总结整理如下:
唾液在实际检测过程中的主要问题:
(1) 食品残渣的分解可能导致在持续监测期间产生大量的分泌性蛋白质活性化学物质和其他干扰杂质,将严重干扰目标分析物的提取、检测和传感。
(2) 口腔内存在适合细菌生长和繁殖的温度和湿度条件,这可能会导致细菌在传感器表面迅速积聚,形成生物膜,影响灵敏度。
(3) 此外,未受刺激和受刺激的唾液以及通过不同方法产生的唾液的成分和浓度也存在差异。
b. 基于呼吸丙酮的无创葡萄糖传感器主要问题点
(1) 影响丙酮生产的因素很多,不同的实验条件会改变相关性。例如,胰岛素注射、食物摄入、剧烈运动、酒精摄入、个体生理差异、糖尿病类型和其他类型的疾病都会对丙酮代谢率产生影响这些因素使呼吸丙酮和血糖水平之间的关系变得非线性。这也是基于呼吸丙酮的无创葡萄糖传感器的核心问题。
(2) 丙酮是脂肪代谢的产物,不是葡萄糖直接产生的,因此血糖和呼吸丙酮的映射变化可能存在时滞。滞后时间也因人而异。
c. 测量眼泪的可穿戴传感器主要问题点:
(1) 由于传感器和传输电路的原因,隐形眼镜的透射率会降低,需要后续在材料选择和电路设计中增加透射率。
(2) 传感器一般采用无线供电和无线传输,这对信号传输的能量供应提出了很高的要求。如果这些传感器在使用过程中发热,会导致眼睛刺痛和不适。
(3) 有关团队检测到,血糖和血糖之间的平均滞后时间达到13分钟,相关系数R2仅为0.7544,因此测量精度无法满足临床要求3。
d. 基于汗液的非侵入式葡萄糖传感器的问题点:
(1) 大多数方案通过长时间剧烈运动、加热、压力和电离能刺激来提取和收集汗液,但都有各自的缺点(例如,糖尿病患者不适合长时间运动,加热和电离刺激会带来疼痛和不适)。
(2)由于汗液中的葡萄糖含量较少,灵敏度较低。
(3)相对于血糖有一定的滞后性。
e. 基于组织间液葡萄糖传感器的问题点:
(1) 更高的电流有利于提高传感器的检测极限和灵敏度,但高电流会导致皮肤高度干燥,这可能会导致皮肤发红、肿胀和刺痛等症状,降低用户的舒适度。
(2) 由于血液和ISF之间的物质交换存在一段时间,测量结果往往滞后,可能无法反映血糖的实时值。
参考文献:
[1] Tang L, Chang SJ, Chen CJ, Liu JT. Non-Invasive Blood Glucose Monitoring Technology: A Review. Sensors (Basel). 2020 Dec 4;20(23):6925. doi: 10.3390/s20236925. PMID: 33291519; PMCID: PMC7731259.
[2] 杨宇祥, 吴彬, 林海军,等. 无创血糖检测技术研究进展[J]. 分析测试学报, 2022, 41(4):9.
[3] La Belle, J.T.; Adams, A.; Lin, C.-E.; Engelschall, E.; Pratt, B.; Cook, C.B. Self-monitoring of tear glucose: The development of a tear based glucose sensor as an alternative to self-monitoring of blood glucose. Chem. Commun. 2016, 52, 9197–9204.

来源:和义广业创新平台


