您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-10-09 15:39
2001年,Sharpless和Meldal 发表Cu(I) 催化的 [3+2] 环加成反应 (通常称为“Click Chemistry”)的发现,这大大丰富了多肽蛋白偶联的反应手段。在Cu (I) 催化剂存在下,可以将含有炔基和叠氮基团的不同多肽/蛋白片段通过click chemistry高度选择性/正交性地偶联在一起,构建结构更复杂,生物功能性更强的多肽/蛋白大分子(图1)。
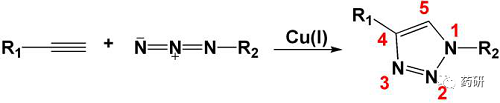
图1. Cu(I) 催化的Click Chemistry过程
Click chemsitry 本质上属于上世纪就发现的Huigsen 环加成反应,但后者需要较高的反应温度和较长的反应时间,对于多肽合成来说构成稳定性方面的问题。在发现Cu (I) 催化后,Click chemistry可以实现在较低温度(室温)下很短时间内的反应,通过炔基与叠氮之间环加成为三唑的反应,极大地丰富了复杂多肽合成的反应手段。这个反应可以在诸如叔丁醇、乙醇或者水等极性溶剂中进行。
Click chemistry在多肽合成领域发挥重要的作用,不仅仅在于它可以将两个多肽片段通过正交方式偶合在一起,组建更复杂的分子体系,而且也在于它可以将多肽骨架的酰胺键替换为等电体的三唑基团,以提高多肽的化学稳定性,或者赋予多肽分子新的特殊的空间结构。
通常肽含有通过酰胺键连接的 L-氨基酸,这些氨基酸易受酶促肽键裂解。蛋白酶和肽酶,例如胰蛋白酶、α-胰凝乳蛋白酶和二肽基肽酶 IV(DPP 4),能够切割蛋白质和肽中的特定位点。为了增加多肽药物的稳定性,很多非蛋白质氨基酸被嵌入多肽分子之中,除此之外,包括末端封闭,环化,骨架修饰等诸多手段都被多肽药物分子设计者所利用,以多肽类似物的手段提升多肽分子的成药性。1,2,3-三唑作为酰胺的等电体,它在多肽类似物设计中的作用也逐渐受到重视。它们的空间尺寸、偶极矩、氢键受体等诸多方面都存在着较大的相似度。1,2,3-三唑环,具有sp2-杂化氮原子N(2) 和N(3),可以作为弱氢键受体。并且1,2,3-三唑环的强偶极矩使 C(5) 质子极化到可以充当类似于酰胺 NH 的氢键供体的程度。此外,1,2,3-三唑环有一个大的偶极,可以与所处多肽中的其他酰胺在二级结构上相关联。重要的是,1,2,3-三唑对水解极为稳定。总体而言,1,2,3-三唑可以成为多肽类似物中酰胺键的潜在替代物。
Click化学在多肽合成中的应用:
一三唑环替换二硫键
2011 年Empting 等人首先使用 1,5-二取代的 1,2,3-三唑作为二硫键的替代物。 1,5-二取代的 1,2,3-三唑是在钌 (II)-催化反应(RuAAC) 中生成的。他们将 1,4- 和 1,5-二取代的 1,2,3-三唑引入向日葵胰蛋白酶抑制剂-I (SFTI-1[1,14]) 的单环变体中,通过click chemistry取代二硫键,并且表明 1,5-二取代三唑类似物与 1,4-二取代三唑类似物相比保留了几乎全部的生物活性。同年,Morten Meldal (2022年诺贝尔化学奖得主之一) 等人使用 1,4-二取代的 1,2,3-三唑取代 tachyplesin I (TP-I) 中的两个二硫键,这是一种具有抗菌活性的 17 个残基双环肽。TP-I在其活性形式中具有β-发夹带状结构,三唑环类似物可以模仿 TP-1 的二级结构并产生抗菌活性。
二替代芳香环和双键
除了用作酰胺键和二硫键的替代物外,1,2,3-三唑在小分子药物设计中还经常被赋予模拟芳香环、酰基磷酸酯和反式烯烃替代物的角色。目前还没有关于多肽药物修饰中这种替代的报道。1,2,3-三唑是碱性芳族杂环化合物,可能无法直接替代中性芳族 Phe 和 Tyr 侧链。然而,在某些情况下,替代物可能有助于增强结合亲和力或生物活性。因此,可以在未来的多肽药物或许能发现它的作用。
三β-转角替代物
多肽药物的空间结构对于它们的成药性起着至关重要的作用,Guan等人通过 Cu(I) 催化的两条肽链末端之间的炔烃-叠氮化物环加成构建 β-转角模拟单元,根据这个发现,他们提出用叠氮化物和末端炔烃衍生的肽链之间的环加成可能提供合成β-转角单元的方法。 他们设计并合成了一系列具有不同间隔长度的 1,4-二取代 1,2,3-三唑基四肽,并通过 NMR 和 FT-IR 对其进行了表征。他们发现三唑系统形成β-转角的趋势在很大程度上取决于手臂长度。三碳手臂(图2)是稳定 β 转角形成的最佳选择。
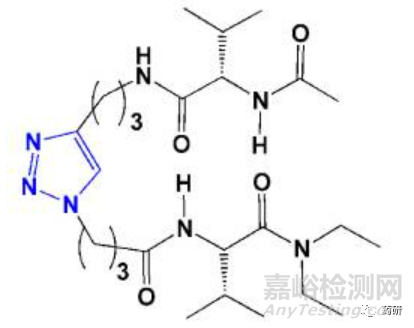
图2. 形成β 转角最佳结构的三唑多肽
四三唑多肽环化
Click chemistry 为合成环肽提供了重要的手段。多肽首尾环化是增加肽结构刚性和稳定性的重要途径。外切蛋白酶可以识别N-或C-末端基团并水解多肽分子,因此多肽首尾环化可以显著增加分子的外切酶水解稳定性。Morten Meldal 使用铜催化的闭环反应制备了首尾环化的多肽分子(图 3)。关键步骤的click chemistry是在2当量的CuI催化,并在50当量的DIPEA存在下过夜完成的。该反应也可以在其它活性氨基酸侧链不保护的情况下实现。
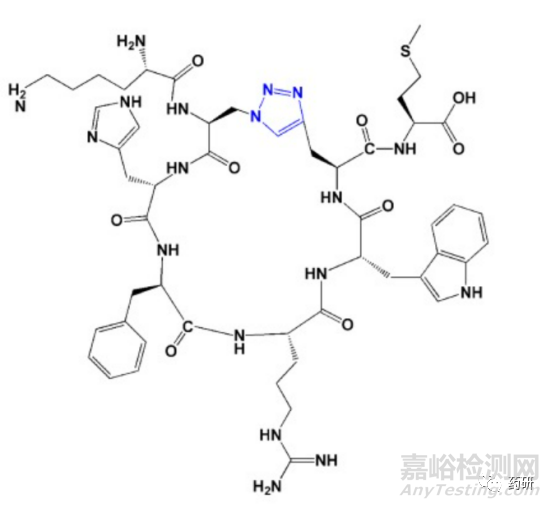
图3. Click Chemistry介导的环肽结构
常规的酰胺化环化很难实现四元肽的环化,但三唑环化却可以突破这一限制。一项研究返现,从对酪氨酸酶具有潜在抑制活性的细菌中分离出的模型四肽:环-[Pro-Val-Pro-Tyr] 由于过大的张力很难用传统的肽环化合成(尽管存在两个有利于环化的Pro残基)。但当Pro-Val之间的酰胺键被三唑环替代后,环化可以顺利完成(图4)。
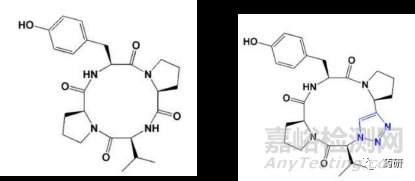
图4. 环-[Pro-Val-Pro-Tyr](左)和三唑环类似物(右)
五生物共轭反应
生物共轭是共价连接两个或多个生物分子结构单元,以开发双功能和多功能分子的过程。 它还包括将合成分子连接到诸如碳水化合物、肽、蛋白质、核酸等生物分子上,用于各种体内治疗和成像应用。 Sharpless 小组的开创性工作使点击化学成为生物医学研究中的强大工具。 点击化学因其具有生物正交性、生物相容性、化学选择性和立体特异性潜力而在生物偶联中获得了特殊的重要性。
碳水化合物在从细胞信号传导到病原体防御的不同生理过程中发挥着重要作用。 糖基化多肽在药物研发过程中起着越来越重要的作用,例如在疫苗、治疗剂和抗生素领域。 click chemistry为实现糖基化多肽的合成提供了强大的工具。图5的多肽类似物就是通过click chemistry实现的糖基化多肽结构,应用于抗癌候选疫苗 。
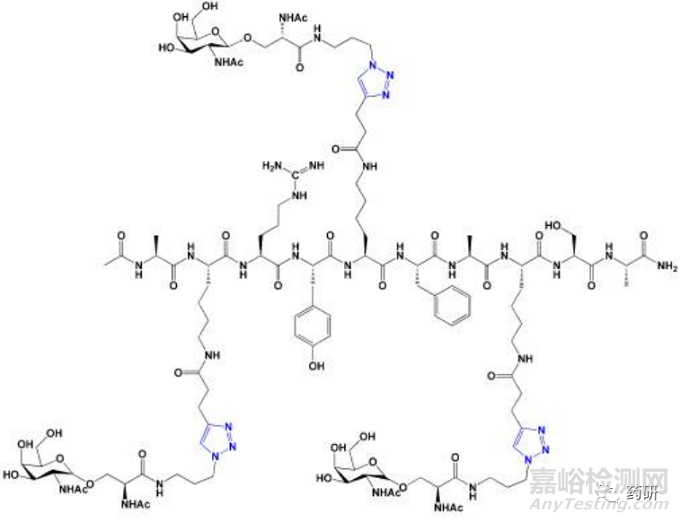
图5. 三唑手臂糖基化多肽疫苗
六总结
Click chemistry已广泛用于多肽药物的研究。三唑环已被作为酰胺键和二硫键的替代物广泛引入多肽类似物分子中,这对于多肽化学修饰以增加代谢稳定性非常有用。由于click chemistry的选择性、高效性以及温和的反应条件,它成为了多肽化学修饰的重要武器,例如多肽片段缩合,肽环化,以及包括糖基化在内的修饰,都可以利用click chemistry实现。三唑的引入可以模拟或促进肽的二级结构。此外,与各种功能结构或基团(如碳水化合物、聚乙二醇和放射性标记/光标记试剂)缩合可以有效增加肽的功能。尽管click chemistry在多肽药物研究中是一种吸引人的方法,但迄今为止在开发临床药物中并不常见。三唑类在生物系统中的代谢途径有待进一步研究。此外,oligomerization副反应也需要有效控制。尽管点击化学存在潜在限制,但它促进多肽药物开发领域内必将发挥更大的潜力,或许不久的将来,三唑结构的身影也能出现在上市多肽药物或者诊断试剂之中。

来源:药研


