您当前的位置:检测资讯 > 实验管理
嘉峪检测网 2025-08-22 21:51
摘 要: 建立了一种连续流动分析-在线镉柱还原法检测肉及肉制品中亚硝酸盐及硝酸盐的含量。试样经处理沉淀蛋白质并除去脂肪后,用流动分析仪自动进样且采用气泡隔断样品,通过透析膜进行透析除杂,亚硝酸盐与磺胺重氮化后,再与盐酸萘乙二胺偶合成紫红色化合物,在538 nm处进行测试,从而测得亚硝酸盐的含量;硝酸盐在镉柱的还原下转化为亚硝酸盐,通过计算测得的亚硝酸盐总量与试样中原有亚硝酸盐含量的差值,得到试样中硝酸盐的含量。亚硝酸盐、硝酸盐质量浓度分别在0.025~1.0 mg/L、0.25~5.0 mg/L内与测定信号值线性关系良好,相关系数分别为0.999 9、0.999 5,加标回收率分别为93.0%~103.3%、95.8%~104.6%,相对标准偏差分别为2.16%~7.55%、3.49%~6.02%(n=6),二者的准确度和精密度均满足技术要求。该方法高效、准确、自动化,为肉及肉制品中亚硝酸盐与硝酸盐的快速检测提供了一种新的解决方案,具有显著的技术优势和应用前景。
关键词: 连续流动分析; 肉及肉制品; 亚硝酸盐; 硝酸盐
肉及肉制品是人们日常饮食生活中摄取蛋白质的主要来源,在肉及肉制品加工过程中会添加或者产生亚硝酸盐及硝酸盐,高剂量的亚硝酸盐和硝酸盐摄入会对人体产生毒害作用,这主要是因为进入人体的硝酸盐可转化为亚硝酸盐,而亚硝酸盐会转化为亚硝胺,亚硝胺是一种强致癌物,如果长期或高剂量摄入这类化合物,会严重危害人体健康[1‒2]。轩伟等[3]对2014~2018年市场上售卖的熟肉制品中亚硝酸盐残留量数据进行分析,发现市场上不同场所销售的熟肉制品都存在一定量的亚硝酸盐及硝酸盐,部分产品甚至存在含量超标的问题。张雪茹等[4]研究发现,不同加工方式会对牛肉中的亚硝酸盐和硝酸盐含量产生很大的影响,如经脱水工艺加工的牛肉制品中亚硝酸盐的含量明显低于其他加工方式制备的牛肉制品,因此,通过研究肉及肉制品中亚硝酸盐和硝酸盐的含量,可以帮助公众合理选购及加工肉及肉制品,控制来自这些食品中的亚硝酸盐和硝酸盐的摄入量,减少因过量摄入亚硝酸盐和硝酸盐所带来的健康隐患。
目前亚硝酸盐和硝酸盐检测方法主要有分光光度法[5‒7]、电化学法[8‒11]和色谱法等。分光光度法由于部分肉及肉制品通常呈色泽较深,样品溶液有颜色干扰,且镉柱还原硝酸盐过程非连续,面对大批量样品检测时耗时多,速度慢,而采用活性炭脱色后,硝酸盐的测定仍会受到共轭离子和亚硝酸盐的干扰,需要额外步骤来消除这些干扰因素。电化学方法电极的制备过程繁琐且成本较高。高效毛细管电泳法[12‒13]中的氯离子会对测定结果产生干扰,影响亚硝酸根离子的测定;离子色谱法[14‒16]在测定部分肉及肉制品特别是以腌制、熏烤为工艺加工的产品时会因为高盐分而使Ag柱和Na柱的损耗增加,应用受到一定的限制[17]。基于此,笔者提出一种连续流动分析-在线镉柱还原法来同时测定肉及肉制品中的亚硝酸盐和硝酸盐,样品经处理沉淀蛋白质、脱脂、制成样品溶液后进入连续流动分析仪进行测定。样品溶液先经膜分离器分离除杂脱色后,其中的亚硝酸盐先与磺胺重氮化,再与盐酸萘乙二胺偶合生成紫红色化合物,于538 nm波长处比色测定,得到亚硝酸盐含量。同时,待测溶液中的硝酸盐经镉柱还原为亚硝酸盐,按同样方法测得亚硝酸盐总量,其中硝酸盐含量即为亚硝酸盐总量减去直接测得的亚硝酸盐含量。与传统检测方法相比,该方法通过在线透析滤除杂质,排除颜色干扰,结果准确,数据稳定,可同步、连续测定并即时得到亚硝酸盐和硝酸盐的含量。
1 实验部分
1.1 主要仪器与试剂
连续流动分析仪:SAN++型,荷兰Skalar公司。
振荡水浴槽:SW22型,德国Julabo公司。
分析天平:AL204型,感量为0.1 mg,瑞士梅特勒-特利多公司。
亚硝酸钠、硝酸钠标准溶液:质量浓度均为200 μg/mL,标准物质编号分别为GBW(E) 100156、GBW(E) 100157,北京海岸鸿蒙标准物质技术有限公司。
三水亚铁氰化钾、二水乙酸锌、冰乙酸、十水硼酸钠、聚氧乙烯月桂醚、氯化铵、乙二胺四乙酸二钠、氨水、磷酸、磺胺、盐酸萘乙二胺:均为分析纯,国药集团化学试剂有限公司。
1.2 溶液配制
亚铁氰化钾溶液:106 g/L。称取106 g亚铁氰化钾,加入约500 mL水溶解,移入1 000 mL容量瓶中,用水稀释至标线并混匀。
乙酸锌溶液:220 g/L。称取220 g二水乙酸锌,加入30 mL冰乙酸和约500 mL水,加热或超声至其完全溶解,移入1 000 mL容量瓶中,用水稀释至标线并混匀。
饱和硼砂溶液:50 g/L。称取50 g十水硼酸钠,加入约500 mL热水溶解,冷却后移入1 000 mL容量瓶中,用水稀释至标线并混匀。
聚氧乙烯月桂醚溶液:0.3 g/mL。称取30 g聚氧乙烯月桂醚,加入约50 mL水溶解并转移至100 mL容量瓶中,用水稀释至标线并混匀。
氯化铵缓冲溶液:pH值为8.5。称取85 g氯化铵和1.0 g乙二胺四乙酸二钠溶于800 mL水中,混合均匀,用氨水调节pH值至8.5±0.1,转移至1 000 mL容量瓶中,用水稀释至标线并混匀,再加入1 mL聚氧乙烯月桂醚溶液。于0~4 ℃冰箱避光保存,有效期一周。
磺胺显色液:将100.0 mL磷酸加入到600 mL水中,放置冷却至室温,再加入10.0 g磺胺和1.0 g盐酸萘乙二胺,搅拌至全部溶解,转移至1 000 mL容量瓶中,用水稀释至标线并混匀。于0~4 ℃冰箱避光保存,有效期一周。
亚硝酸盐标准中间液:5.0 μg/mL。吸取亚硝酸盐标准储备液2.5 mL,置于100 mL容量瓶中,加水稀释至标线,临用现配。硝酸盐标准中间液:5.0 μg/mL。吸取硝酸盐标准储备液5.0 mL,置于200 mL容量瓶中,加水稀释至标线,临用现配。
亚硝酸盐系列标准工作液:分别吸取0.0、0.25、0.50、1.00、3.00、5.00、10.0 mL亚硝酸盐标准中间液,置于7只50 mL带塞比色管中并加水定容至标线,配制成亚硝酸盐(以亚硝酸钠计)的质量浓度分别为0.0、0.025、0.05、0.10、0.30、0.50、1.0 mg/L的亚硝酸盐系列标准工作液。
硝酸盐系列标准工作液:吸取0.0、2.50、5.00、10.0、15.0、25.0、50.0 mL硝酸盐标准中间液,分别置于50 mL带塞比色管中并加水稀释至50 mL,配制成硝酸盐(以硝酸钠计)的质量浓度分别为0.0、0.25、0.50、1.00、1.50、2.50、5.00 mg/L的硝酸盐系列标准工作液。
1.3 仪器工作条件
电源类型:220 V、50 Hz的交流电源。
连续流动分析仪:常温下,在538 nm波长处进行测试。其中,缓冲液的流量设置为1.0 mL/min,单个样品进样体积为1.0 mL。
1.4 实验方法
1.4.1 样品处理及提取取
适量样品粉碎至均匀粉末或制成匀浆,称取5 g制备好的样品,置于250 mL锥形瓶中,加入12.5 mL 50 g/L饱和硼砂溶液,再加入150 mL 70 ℃左右的水,混匀加盖置于沸水浴中加热15 min后取出,放置在冷水浴中冷却至室温,之后转移至200 mL容量瓶中,加入5 mL 106 g/L亚铁氰化钾溶液,摇匀,再加入5 mL 220 g/L乙酸锌溶液用以沉淀蛋白质,然后加水定容至200 mL,振摇混匀,静置30 min (必要时可增加离心操作保证滤液澄清),将上清液用滤纸过滤并弃去初滤液30 mL,后续滤液备用。同时进行空白试验,空白样品溶液采用实验用水代替样品,按前述同样步骤操作。1.4.2 标准曲线及样品测定
(1) 标准曲线的绘制
将标准工作液倒入样品杯中,放置在样品架上,由进样器按程序依次进行取样、测定。以亚硝酸盐或硝酸盐质量浓度为横坐标,分光光度计测定信号值(峰高)为纵坐标进行校准曲线的绘制。
(2) 样品测定
将空白样品溶液和样品溶液按照上述相同的条件进行测定,分别得到信号值(峰高),根据标准曲线得到样品溶液中亚硝酸盐(以亚硝酸钠计)或硝酸盐(以硝酸钠计)的浓度。若样品的亚硝酸盐含量或硝酸盐含量超出标准曲线的检测范围,应进行稀释后再测定。
2 结果与讨论
2.1 实验条件优化选择
2.1.1 称样质量
分别选取称样质量为1.0、2.0、5.0、10.0、15.0 g进行试验,亚硝酸盐质量分数测定值随称样质量变化如图1所示。由图1可以看出,随着称样质量增加,亚硝酸盐检测含量逐渐上升,但在5.0 g后开始下降,最终确定称样质量为5.0 g。
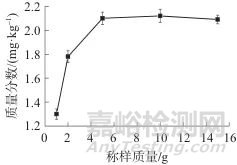
图1 不同称样质量时亚硝酸盐的质量分数
Fig. 1 Mass fraction of nitrite in different sample weight
2.1.2 提取时间
分别在提取时间为5、10、15、20、25 min条件下进行试验,结果如图2所示。由图2可以看出,亚硝酸盐质量分数测定值随着提取时间增加有所上升,但在15 min后趋于稳定,最终确定提取时间为15 min。
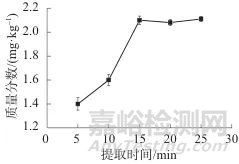
图2 不同提取时间时亚硝酸盐的质量分数
Fig. 2 Mass fraction of nitrite at different extraction time
2.1.3 沉淀剂选择
乙酸锌和亚铁氰化钾反应生成的氰亚铁酸锌沉淀具有很强的吸附能力,能够有效地裹挟和吸附溶液中的蛋白质,从而实现蛋白质的沉淀。相比其他沉淀剂,如硫酸铵、硫酸钠等中性盐,乙酸锌和亚铁氰化钾的沉淀效果更为显著,且沉淀物更易于分离和去除,而三氯乙酸因其酸性条件与实验酸碱性条件不符,所以最终选择乙酸锌和亚铁氰化钾作为沉淀剂。
2.1.4 在线透析条件优化
通过透析膜在线透析,在线滤除蛋白、脂肪等大分子化合物,很好地解决了颜色干扰问题,选择红肠类样品使用不同品牌透析膜进行试验,结果如图3所示。由图3可以看出,亚硝酸盐质量分数测定值在Skalar透析膜条件下效果最好,最终确定透析膜为Skalar公司生产。
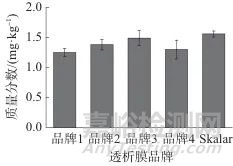
图3 不同品牌透析膜时亚硝酸盐的质量分数
Fig. 3 Mass fraction of nitrite in different brands of dialysis membranes
2.1.5 波长选择使用亚硝酸钠标准溶液进行试验,在波长范围为340~800 nm条件下进行比色,绘制吸收曲线如图4所示。由图4可以看出,最大吸收波长为538 nm,故采用538 nm作为测定波长。
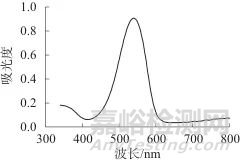
图4 亚硝酸盐吸收曲线
Fig. 4 Absorption curve of nitrite
2.1.6 镉粒选择
分别使用纯镉粒和镀铜镉粒装填镉柱进行实验,观察记录镉柱还原效率,结果见图5。由图5可以看出,镀铜镉粒相比纯镉粒具有更高的还原效率,因此选用镀铜镉粒进行实验效果最好。
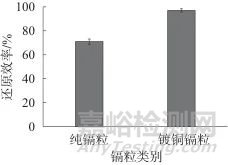
图5 不同镉粒类别时镉柱还原效率
Fig. 5 Cadmium column reduction efficiency in different cadmium particle categories
2.2 线性范围及定量限
根据前述方法对亚硝酸盐系列标准工作液和硝酸盐系列标准工作液进行测定,根据测得结果绘制标准曲线并得到线性回归方程,结果列于表1。由表1可知,亚硝酸盐质量浓度在0.025~1.0 mg/L内、硝酸盐质量浓度在0.25~5.0 mg/L内,两者的质量浓度与分光光度计信号值线性关系良好,相关系数均超过0.999。根据GB/T 5009.1—2003《食品卫生检验方法 理化部分 总则》附录A的定义,把3倍空白值的标准偏差(测定次数n≥20)相对应的质量或浓度称为检出限,定量限为10倍标准偏差。根据方法的称样量和定容体积,亚硝酸盐检出限为0.3 mg/kg,定量限为1 mg/kg,硝酸盐检出限为3 mg/kg,定量限为10 mg/kg。
表1 亚硝酸盐及硝酸盐标准曲线的线性方程及相关系数
Tab. 1 Linear regression equations,coefficients and linear ranges of standard curves

2.3 样品加标回收试验
向5种肉及肉制品样品中分别添加低、中、高3个不同浓度水平的标准溶液,按照前述方法进行样品处理,之后再进行亚硝酸盐和硝酸盐含量的测定,每个添加水平进行6次平行测定后,分别计算亚硝酸盐和硝酸盐的加标回收率并取均值作为最终结果,同时分别计算不同样品不同水平浓度下测定结果的相对标准偏差(RSD),结果见表2和表3。由表2和表3可知,亚硝酸盐的平均加标回收率为93.0%~103.3%,RSD为2.16%~7.55%;硝酸盐的平均加标回收率为95.8%~104.6%,RSD为3.49%~6.02%。该方法在亚硝酸盐及硝酸盐含量的检测中具有良好的准确度和精密度,能够满足实际应用需求。
表2 肉及肉制品中亚硝酸盐加标试验结果
Tab. 2 Results of the spiking test for the determination of nitrite in meat and meat products
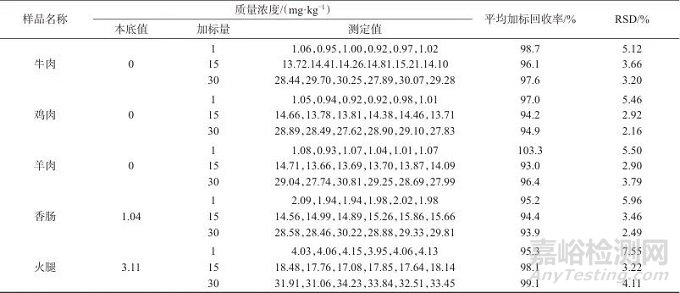
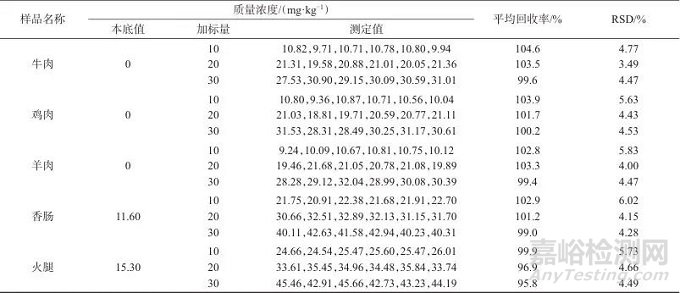
表3 肉及肉制品中硝酸盐加标试验结果
Tab. 3 Results of the spiking test for the determination of nitrate in meat and meat products
3 结语
创新性地提出了一种高效、精确检测肉及肉制品中亚硝酸盐与硝酸盐含量的方法。相较于传统手段,该方法巧妙利用透析技术在线滤除蛋白、脂肪等大分子杂质,从根本上攻克了颜色干扰这一长期存在的技术难题。其操作简便快捷,不仅显著提升了检测的灵敏度与准确性,还凭借双通道同步测定功能,实现了亚硝酸盐与硝酸盐含量的即时并行分析,极大地缩短了检测周期,提高了工作效率。鉴于此方法的显著优势,其在肉类及肉制品安全监控领域具有广泛的应用前景,同时,也为其他食品中亚硝酸盐及硝酸盐含量的高效检测开辟了全新的路径,展现出广阔的推广与应用潜力。
参考文献
1 李卉,李莉.食品中亚硝酸盐检测方法的研究进展[J].食品工业科技,2022,43(23): 429.
LI Hui,LI Li. Research progress on the determination of nitrite in food[J]. Science and Technology of Food Industry,2022,43(23): 429.
2 张雪莲,刘颖,朱晓俊.腌肉制品中亚硝酸盐检测方法研究现状[J].现代食品,2024,30(14): 82.
ZHANG Xuelian,LIU Ying,ZHU Xiaojun. A review of current research on detection methods of nitrite in cured meat products[J]. Modern Food,2024,30(14): 82.
3 轩伟,付传鹏,丁文燮.2014—2018年商丘市散装熟肉食品亚硝酸盐含量分析[J].河南医学高等专科学校学报,2022,34(5): 575.
XUAN Wei,FU Chuanpeng,DING Wenxie. Analysis of nitrite content in bulk cooked meat food in Shangqiu from 2014 to 2018[J]. Journal of Henan Medical College,2022,34(5): 575.
4 张雪茹,宋志超,刘婷婷,等.常见市售袋装熟制牛肉产品的营养安全品质调查与分析[J].食品与发酵工业,2020,46(15): 282.
ZHANG Xueru,SONG Zhichao,LIU Tingting,et al. Investigation and analysis of nutrition,safety and quality of the cooked and packaged beef products in the market[J]. Food and Fermentation Industries,2020,46(15): 282.
5 黄双杰,常亚丽,赵雅梅,等.活性炭脱色—比色法测定茶叶硝态氮[J].茶叶学报,2022,63(3): 143.
HUANG Shuangjie,CHANG Yali,ZHAO Yamei,et al. Colorimetric nitrate determination of tea extract with activated carbon pretreatment[J]. Acta Tea Sinica,2022,63(3): 143.
6 刘玲,陈俊秀,赵香梅,等.分光光度法测定肉制品中的亚硝酸盐[J].实验室检测,2023,1(1): 12.
LIU Ling,CHEN Junxiu,ZHAO Xiangmei,et al. Determination of nitrite in meat products by spectrophotometry[J]. Laboratory Testing,2023,1(1): 12.
7 陈银珊.活性炭脱色测定调味酱中亚硝酸盐方法探讨[J].食品安全导刊,2021(12): 91.
CHEN Yinshan. Discussion on the method of using activated carbon decolorization to determine nitrite in seasoning sauce[J]. Food Safety Guide,2021(12): 91.
8 徐艺伟,朱丹,石吉勇,等.原位合成铜基金属有机框架差分脉冲伏安法快速检测肉制品中亚硝酸盐[J].食品科学,2021,42(16): 267.
XU Yiwei,ZHU Dan,SHI Jiyong,et al. Rapid detection of nitrite in meat products by in-situ synthesized Cu-based metal organic frameworks coupled with differential pulse voltammetry[J]. Food Science,2021,42(16): 267.
9 ZHANG M S,YANG Y,GUO W C. Electrochemical sensor for sensitive nitrite and sulfite detection in milk based on acid-treated Fe3O4@SiO2 nanoparticles[J]. Food Chemistry,2024,430: 137 004.
10 周鸿燕,李晓乐.基于NiO@Pt-离子液体/玻碳电极传感器检测肉制品中的亚硝酸盐[J].食品安全质量检测学报,2021,12(24): 9 377.
ZHOU Hongyan,LI Xiaole. Detection of nitrite in meat products based on NiO@Pt-ionic liquid/glassy carbon electrode sensor[J]. Journal of Food Safety & Quality,2021,12(24): 9 377.
11 陈林林,吴松遥,郝熙,等.酚酸基纳米金修饰电极检测食品中的亚硝酸盐和亚硫酸盐[J/OL].食品工业科技,2025,46(1): 274.
CHEN Linlin,WU Songyao,HAO Xi,et al. Determination of Nitrite and Sulfite in Foods by Phenolic Acid-based Gold Nanoparticles Electrode[J]. Science and Technology of Food Industry,2025,46(1): 274.
12 李秀明,马俪珍. HPCE法同时检测果蔬及肉制品中硝酸盐和亚硝酸盐含量[J].食品科学,2018,39(12): 301.
LI Xiuming,MA Lizhen. Simultaneous determination of nitrate and nitrite in vegetables and meat products by high performance capillary electrophoresis[J]. Food Science,2018,39(12): 301.
13 BOLSHAKOV D S,AMELIN V G. Capillary electrophoresis in assessing the quality and safety of foods[J]. Journal of Analytical Chemistry,2023,78(7): 815.
14 周正会.离子色谱法在常见食品添加剂检测中的应用研究[J].食品安全导刊,2023(21): 186.
ZHOU Zhenghui. Ion chromatography method in the application of common food additives[J]. China Food Safety Magazine,2023(21): 186.
15 苏家杰,孙家豪,杜磊.离子色谱法对腌制食品中亚硝酸盐的定量及优化[J].广州化学,2022,47(4): 76.
SU Jiajie,SUN Jiahao,DU Lei. Optimization of determination of nitrite in pickled food by ion chromatography[J]. Guangzhou Chemistry,2022,47(4): 76.
16 李营,张建,孙海录,等.离子色谱法测定香肠中的亚硝酸盐和硝酸盐[J].中国调味品,2020,45(2): 146.
LI Ying,ZHANG Jian,SUN Hailu,et al. Determination of nitrite and nitrate in sausage by ion chromatography[J]. China Condiment,2020,45(2): 146.
17 ZHANG L J,ZHANG L,XU Y. Effects of Tetragenococcus halophilus and Candida versatilis on the production of aroma-active and umami-taste compounds during soy sauce fermentation[J]. Journal of the Science of Food and Agriculture,2020,100(6): 2 782.

来源:化学分析计量


