您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-10-10 06:31
〔摘 要〕镍合金在医疗领域已经有广泛的应用,在为患者带来诸多临床获益的同时也增加了镍金属过敏的风险,但对于镍过敏是否为导致镍合金植入物使用失败的原因目前业界仍存在争论。基于此,该研究总结了镍合金过敏的流行病学、既往的临床不良反应报道和体内镍的释放和分布等方面的研究现状,并汇总了镍过敏相关细胞和分子机制的文献证据,以期全面了解镍的免疫毒理研究现状,为开展镍合金医疗器械的免疫学评价提供思路。
〔关键词〕镍合金;医疗器械;过敏;免疫毒性
〔中图分类号〕R197.39
〔文献标识码〕A
〔文章编号〕1002-2376(2022)17-0193-04
镍合金在医疗领域的应用十分广泛,例如,被用于制备各类心血管器械(血管支架、心脏瓣膜和封堵器)、修复器械(正畸丝和根管锉等)及骨科骨折固定器械等[1-2]。近年来,随着镍合金器械使用量的不断增加,可能与其存在关联的过敏相关并发症的报道亦逐渐增多,其免疫原性也引起了学者们的广泛关注。但目前尚无研究证实某一镍合金器械的临床使用失败与其过敏反应之间具有明确的联系[3-6]。本研究就镍合金免疫原性研究进展进行综述,以便相关人员全面了解含镍医疗器械的免疫毒性风险,为开展镍合金器械的免疫学评价提供参考。
1 镍/镍合金过敏的流行病学
许多金属都具有免疫活性并可引起一定的过敏反应,该现象在临床骨科、牙科、妇科、心血管及泌尿科等均有报道[7]。目前已知的金属敏化剂(半抗原)包括铍、镍、钴和铬,据估计,就一般人群而言,镍、钴和铬的过敏反应发生率均在10%~15%之间,其中,镍的过敏反应发生率最高,约为14%,在一些新近报道中,镍的过敏反应发生率甚至高达20%~30%[8-9]。
在所有的金属过敏症状中,最常见的是镍引起的变应性接触性皮炎,且部分因素会增加该病变的发生风险。例如,镍相关接触性皮炎在女性中的患病率是男性的4倍,在有耳洞人群中的患病率是其他人群的3.2倍。此外,金属过敏的患病率在采矿、金属和陶器加工从业人员中相对更高[10]。有研究表明,使用镍合金关节置换装置患者的过敏反应发生率高于普通人群,达到了25%[6,11]。但相对于每年进行的手术数量而言,植入后的镍过敏反应及严重后遗症的报道仍然较少,总体风险较低。人工关节置换术后,约1%的患者会出现明显的金属过敏症状。一项针对使用镍钛合金封堵器患者的调查结果显示,镍引起的过敏反应的发病率约为2%(33/1 600)[12]。另一项多中心调查结果显示,在13 736例接受经皮卵圆孔未闭封堵术(植入术)进行治疗的患者中,仅14例是由于镍过敏导致设备摘除,摘除率约为0.1%[13]。尽管皮肤镍过敏是在一般人群中最为常见的金属过敏症状,但并非所有的皮肤相关镍过敏均会表现于其他组织中,因此,镍合金植入物的超敏反应现象并不常见,但在使用中仍需考虑易感个体局部的组织过敏反应有可能带来的风险。
2 镍合金医疗器械过敏的临床表现
绝大多数金属(包括镍合金)的过敏反应类型为Ⅳ型(迟发型)超敏反应,常见症状包括湿疹、荨麻疹、大疱和血管炎爆发,更复杂的过敏反应可发展至植入体周围,造成疼痛、无菌性炎症和植入体松动等[10]。而大部分患者在去除植入体后,症状便即刻好转。
Guerra和Kirkwood[14]的研究表明,镍过敏患者在植入腘动脉镍钛合金支架后出现了斑丘疹、痒疹等严重全身皮炎,取出支架后症状消失。另有研究报道,在镍过敏患者右股动脉植入镍钛合金支架后,会引起全身严重瘙痒和右腿湿疹性皮炎加重,使用聚四氟乙烯移植物替换后症状完全消失[15]。Kounis综合征是一种严重过敏反应诱发的急性冠脉综合征[16],一项对46例使用了镍钛合金房间隔缺损封堵器患者的评估发现,在9例镍斑贴试验呈阳性的患者中,8例(6例采用了高镍含量的镍钛诺Amplatzer封堵器,2例采用了低镍的Premere封堵器)在术后2~3d开始出现短暂的胸部不适、劳累性呼吸、虚弱、心悸、偏头痛加重和轻度白细胞增多等类Kounis综合征症状,而其他37例无镍过敏患者在术后均未出现此症状[17]。
根据以上报道可以看出,对术前有镍过敏史的患者,含镍植入物效果不佳的可能性高于无镍过敏史的患者。多数学者认为,金属过敏可能是导致手术失败的危险因素之一。近年来的研究发现,植入假体磨损的颗粒在少数情况下可能导致假体周围区域出现慢性炎症反应,导致巨噬细胞刺激无菌性骨溶解,从而造成植入失败[18]。
Granchi等[19]近30年的随访也发现,有金属过敏史的患者全髋关节置换术失败率是普通患者的4倍。但有部分学者持不同观点。Thyssen等[20]对356例斑贴试验过敏患者接受关节置换术治疗后进行了1~12年的随访,发现植入失败的风险并未增加。另一项对147例接受金属冠状动脉支架植入术治疗的皮炎患者的评估显示,皮炎患者中镍过敏反应似乎并不会增加冠状动脉支架植入术后支架内再狭窄的总体风险[21]。
3 体内镍合金中镍的释放
镍合金虽然具有较强的耐腐蚀和耐磨损性,但在复杂的体内环境中,仍会出现不同程度的松动、点蚀、沉积或腐蚀,从而可直接导致镍离子释放量的增加。同时,器械表面与机体组织之间的磨损也在所难免,大颗粒的磨屑颗粒(150nm~10μm)会经巨噬细胞的吞噬作用进入胞内,同样也增加了镍的析出。近年来,国内外研究者对镍钛记忆合金植入人体后的生物相容性进行了大量的研究,认为镍钛合金植入体内后经缓慢释放、电解、腐蚀等过程,以镍钛、镍及其化合物3种形式进入循环系统[22]。
Wataha等[23]将含镍种植体植入大鼠体内以研究镍在植入部位的分布,结果发现,在植入物附近的镍浓度可达到48μg/g,在距离植入物3~4mm处镍浓度呈指数下降直至无法检出;当组织中镍浓度高于25μg/g时,出现了严重的炎症和坏死,而低于5μg/g,则不会引起明显的炎症反应;此外,在术后第7天,镍的分布从种植体中心向外延伸了3~4mm,组织炎症延伸至5mm,表明当植入含镍种植体后,镍在组织中的分布模式与组织炎症之间具有明显的相关性,且炎症反应的范围超过了镍的分布范围。
有研究表明,在植入镍钛合金封堵器后的几个月至几年中,患者血液中的镍含量会增加2~5倍[24-25]。Elkiran等[26]在研究中测定了38例植入镍钛合金封堵器患者血清中镍的水平,结果显示,在术后24h、1个月和3个月,患者血清中镍浓度的中位数分别为1.01、1.72、1.96ng/ml,与术前的0.44ng/ml比较,均有所升高(P<0.0001),随后,含量又逐渐下降至植入前水平。此外,另有研究发现,析出的镍会影响机体内T淋巴细胞亚群的表达,患者术后3个月外周血CD3+、CD4+细胞百分率有所下降,之后随着血清中镍离子析出量的减少,CD3+、CD4+细胞百分率逐渐上升[22]。
4 镍合金过敏的机制
截至目前,大量的科学研究揭示出镍对免疫系统具有一定危害性,例如,抑制免疫器官发育、加速淋巴细胞凋亡等[27],但对于镍过敏反应的机制目前尚不完全清楚。
有学者认为,镍合金植入物在体内发生磨损时释放的镍离子和产生的含镍金属颗粒均可激活免疫系统,诱导迟发型过敏反应的发生[25,28,29]。含镍植入物与免疫系统相互作用的示意图见图1。具体过敏机制为:磨损时释放的镍离子和含镍金属颗粒可直接与Toll样受体4(Toll-likereceptor 4,TLR-4)结合,或半抗原化与MHC-Ⅱ受体相互作用[30];这两种途径均可激活抗原递呈细胞(antigen-presentingcells,APCs),随后活化的APCs会将免疫原呈现给初始辅助性细胞(helper T cell,Th 细胞),并释放细胞因子白细胞介素-12,使初始Th细胞分化为Th1细胞,Th1细胞会释放多种细胞因子,包括激活巨噬细胞的IFN-γ;而活化的巨噬细胞能够释放白细胞介素-1β、白细胞介素-6和肿瘤坏死因子-α,引起内皮细胞受体的表达,招募更多的白细胞到该区域;同时,还能释放活性氧和溶酶体酶,导致组织损伤;此外,APCs释放的白细胞介素-6和其他细胞因子,可导致初始Th细胞分化为Th17细胞,Th17细胞释放白细胞介素-17,激活该区域的中性粒细胞;再次接触同一过敏原会导致特异性T细胞的激活,这些T细胞随后进入血液,并在接触过敏原后产生明显的超敏反应[31]。
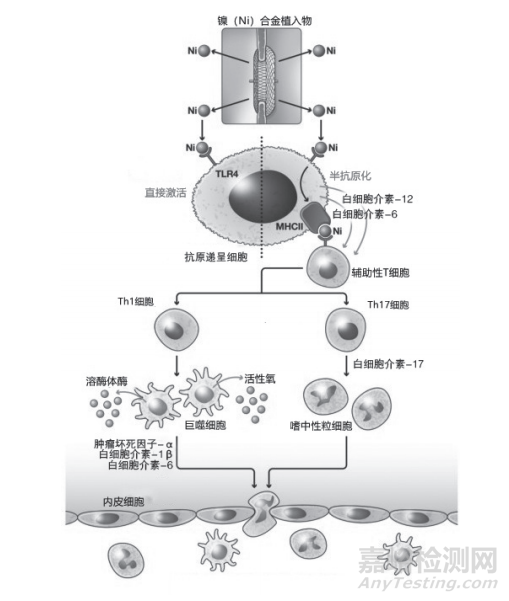
图1 含镍植入物与免疫系统相互作用的示意图[2]
Cavani[32]研究发现,镍产生的过敏反应与血液中金属特异性CD8+T细胞水平的升高呈正相关。从镍过敏患者外周血分离的CD25+T细胞不具有或具有有限的抑制金属特异性CD4+和CD8+T细胞反应的能力。相比之下,来自非过敏受试者外周血的CD25+T调节性细胞,能够以细胞接触依赖性及细胞因子非依赖性机制积极调节镍的免疫应答[33]。以上研究结果表明,在健康个体中,CD25+调节性T细胞可以控制幼稚型和效应型镍特异性T细胞的激活。此外,一项有关体外淋巴细胞转化的研究发现,金属过敏患者的淋巴细胞不仅会发生T细胞的活化,同时还会发生B细胞活化,表明金属过敏可能存在比T细胞介导的迟发型超敏反应更加复杂的免疫反应[34],但目前此方面的研究相对较少,仍需开展进一步的研究以揭示金属过敏的确切机制。
5 小结
尽管镍能够激活免疫细胞和免疫系统,引起迟发型超敏反应,临床上也有许多使用镍合金器械患者出现斑丘疹、痒疹以及Kounis综合征等过敏反应的报道,但对于镍过敏导致植入物使用失败仍无明确定论,部分文献结论也相互矛盾。因此,使用镍合金医疗器械可能会给有镍过敏史的患者带来一定的风险,建议对镍具有高度敏感性的个体尽量避免使用该类医疗器械,或者使用其他不含镍的合金进行替代。而通过对镍免疫原性进一步的研究以明确阐述其过敏反应机制,对于镍合金材料的生物安全性评价具有重要意义。
【参考文献】
[1]Sharma N, Raj T, Jangra K. Applications of NickelTitanium Alloy[J]. J Eng Technol, 2015, 5(1): 1-7.
[2]崔跃,张宝祥,马连彩,等 . 镍钛合金在医疗器械领域应用和表面改性研究进展 [J]. 材料导报,2017,31(S2):206-209.
[3]Ahlström MG, Thyssen JP, Wennervaldt M, et al. Nickel allergy and allergic contact dermatitis: A clinical review of immunology, epidemiology, exposure, and treatment[J]. Contact Dermatitis, 2019, 81(4): 227-241.
[4]Naimo PS, Konstantinov IE. Commentary: A nickel for your thoughts: An overlooked allergen in implantable devices? [J]. J Thorac Cardiovasc Surg, 2020, 160(2): 512-514.
[5]Nagaraja S, Di Prima M, Saylor D, et al. Current practices in corrosion, surface characterization, and nickel leach testing of cardiovascular metallic implants[J]. J Biomed Mater Res B Appl Biomater, 2017, 105(6): 1330-1341.
[6]Hallab N, Meeeitt K, Jacobs JJ. Metal Sensitivity in Patients with Orthopaedic Implants[J]. J Bone Joint Surg Am, 2001, 83(3): 428-436.
[7]Stamm A, Kozlowski P, Brandenberger J. Surgical solution to an intracorporeal nickel allergy[J]. Rev Urol, 2017, 19(3): 195-197.
[8]汤菊莉,贺学英 . 镍合金医疗器械的生物学研究进展 [J]. 医疗装备,2017,30(13):193-197.
[9]Es-Souni M, Es-Souni M, Fischer-Brandies H. Assessing the biocompatibility of NiTi shape memory alloys used for medical applications[J]. Anal Bioanal Chem, 2005, 381(3): 557-567.
[10]Baumanna C, Crist B. Nickel allergy to orthopaedic implants: A review and case series[J]. J Clin Orthop Trauma, 2020, 11(S4): S596-S603.
[11]Lu LK, Warshaw EM, Dunnick C. Prevention of Nickel Allergy: The Case for Regulation[J]. Dermatol Clin, 2009, 27(2): 155-161.
[12]Gordon BM, Moore JW. Nickel for your thoughts: Survey of the Congenital Cardiovascular Interventional Study Consortium (CCISC) for nickel allergy[J]. J Invasive Cardiol, 2009, 21(7): 326-329.
[13]Verma, SK, Tobis JM. Explantation of patent for amenovale closure devices: a multicenter survey[J]. J ACC Cardiovasc Interv, 2011, 4(5): 579-585.
[14]Guerra A, Kirkwood M. Severe generalized dermatitis in a nickel-allergic patient with a popliteal artery nitinol stent[J]. J Vasc Surg Cases Innov Tech, 2017, 3(1): 23-25.
[15]Almpanis GC, Tsigkas GG, Koutsojannis C, et al. Nickel allergy, Kounis syndrome and intracardiac metal devices[J]. Int J Cardiol, 2010, 145(2): 364-365.
[16]Rigatelli G, Cardaioli P, Giordan M, et al. Nickel allergy in interatrial shunt device-based closure patients[J]. Congenital Heart Dis, 2007, 2(6): 416-420.
[17]Sharma V, DeShazo RA, Skidmore CR, et al. Surgical explantation of atrial septal closure devices for refractory nickel allergy symptoms[J]. J Thorac Cardiovasc Surg, 2020, 160(2): 502-509.
[18]Hallab NJ, Jacobs JJ. Biologic effects of implant debris[J]. Bull NYU Hosp Jt Dis, 2009, 67(2): 182-188.
[19]Granchi D, Cenni E, Trisolino G, et al. Sensitivity to implant materials in patients undergoing total hip replacement[J]. J Biomed Mater Res B Appl Biomater, 2010, 77(2): 257-264.
[20]Thyssen JP, Jakobsen SS, Engkilde K, et al. The association between metal allergy, total hip arthroplasty, and revision[J]. Acta Orthop, 2009, 80(6): 646-652.
[21]Thyssen JP, Engkilde K, Menné T, et al. No association between metal allergy and cardiac in-stent restenosis in patients with dermatitis-results from a linkage study[J]. Contact Dermatitis, 2011, 64(3): 138-141.
[22]边巴卓嘎 . 采用镍钛合金封堵器介入治疗左向右分流型先天性心脏病后镍离子析出及其对机体免疫机能影响的研究 [D]. 成都:四川大学,2007.
[23]Wataha J, O'DelL ML, Singh BB, et al. Relating nickelinduced tissue inflammation to nickel release in vivo[J]. J Biomed Mater Res, 2001, 58(5): 537-544.
[24]Burian M, Neumann T, Weber M, et al. Nickel release, a possible indicator for the duration of antiplatelet treatment, from a nickel cardiac device in vivo: a study in patients with atrial septal defects implanted with an Amplatzer occluder[J]. Int J Clinical Pharmacol Ther, 2006, 44(3): 107-112.
[25]Ries MW, Kampmann C, Rupprecht HJ, et al. Nickel release after implantation of the Amplatzer occlude[J]. Am Heart J, 2003, 145(4): 737-741.
[26]Elkiran O, Karakurt C, Kocak G, et al. Serum Nickel and Titanium Levels after Transcatheter Closure of Atrial Septal Defects with Amplatzer Septal Occluder[J]. Cardiol Res Pract, 2019 (2019): 1-6.
[27]Guo HR, Liu H, Jian ZJ, et al. Immunotoxicity of nickel: Pathological and toxicological effects[J]. Ecotoxicol Environ Saf, 2020(203): 111006.
[28]王成健,孟增东,张玉勤,等 . 镍钛形状记忆合金的生物相容性研究进展 [J]. 生物骨科材料与临床研究,2016,13(1):65-68,72.
[29]冯均伟,王跃,朱宗,等 . 骨科人工关节置换术后金属过敏研究进展 [J]. 实用医院临床杂志,2012,9(3):166-169.
[30]Schmidt M, Raghavan B, Müller V, et al. Crucial role for human Toll-like receptor 4 in the development of contact allergy to nickel[J]. Nat Immunol, 2010, 11(9): 814-819.
[31]Tsou TC, Liou SH, Yeh SC, et al. Crucial role of Tolllike receptors in the zinc/nickel-induced inflammatory response in vascular endothelial cells[J]. Toxicol Appl Pharmacol, 2013, 273(3): 492-499.
[32]Cavani A. Breaking tolerance to nickel[J]. Toxicology, 2005, 209(2): 119-121.
[33]Cavani A, Nasorri F, Ottaviani C, et al. Human CD25+ Regulatory T Cells Maintain Immune Tolerance to Nickel in Healthy, Nonallergic Individuals[J]. J Immunol, 2003, 171(11): 5760-5768.
[34]Hallab NJ, Caicedo M, Epstein R, et al. In vitro reactivity to implant metals demonstrates a persondependent association with both T-cell and B-cell activation[J]. J Biomed MaterResearch Part A, 2010, 92(2): 667-682.

来源:医疗装备杂志


