您当前的位置:检测资讯 > 实验管理
嘉峪检测网 2022-08-07 20:25
在化学分析中,样品前处理是一个最常见的问题,在色谱检测中检测误差30%来自于样品前处理过程,生物样本分析的主要障碍包括浓度低、干扰大、个体差异大等,样品处理目的主要是去除样品中的杂质,富集样品,血液样本进入质谱分析前通常会用到蛋白沉淀、液液萃取、固相萃取等前处理过程以提高检测的灵敏度,减少基质干扰,提高检测的准确性。
消解方法
1、湿式消解法
硝酸消解法(对于较清的水溶液样品)
硝酸-高氯酸消解法(消解含难氧化有机物的样品)
硝酸-硫酸消解法(硝酸:硫酸=5:2,常加入少量过氧化氢)
硫酸-磷酸消解法(有利于测定时消除Fe3+等离子的干扰)
硫酸-高锰酸钾消解法(常用于测定汞的水溶液样品)
硝酸-过氧化氢消解法:有人用该方法消解生物制品测定氮、磷、钾、硼、砷、氟等元素7.多元消解方法:需采用三元以上酸或氧化剂消解体系。
2、干灰化法(高温分解法)
灰化法分解样品不使用或使用少量化学试剂,并可处理较大称量的样品,故有利于提高测定微量元素的准确度。
灰化温度一般为450~550℃,不宜处理测定易挥发组分的样品,灰化所用用时间也较长。
根据样品种类和待测组分的性质不同,选用不同材料的坩埚和灰化温度。常用的有石英、铂、银、镍、铁、瓷、聚四氟乙烯等性质的坩埚。原则是坩埚不与样品发生反应并在处理温度下稳定。
通常灰化生物样品不加其他试剂,但为促进分解,抑制某些元素挥发损失,常加适量辅助灰化剂。样品灰化完全后,经稀硝酸或盐酸溶解供分析测定。
固相萃取
(1)固相萃取(张海霞、朱彭龄,分析化学2000,28(9):1172)它的优点是:节省时间,交叉污染机会小,重现性好,回收率高,特别适用于微量试液处理。固相萃取的关键是根据样品的性质正确选择固相萃取小柱及洗脱条件。
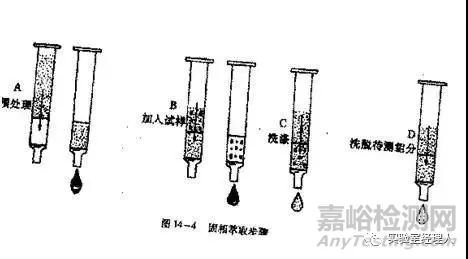
活化(再生) 加样 洗涤 洗脱
(2)固相微萃取固相微萃取集“采样、萃取、浓缩、进样”于一体,能够与气相色谱或高效液相色谱仪联用样品前处理技术。
※与SPE 相比SPME具有以下优点:
(1)不使用有机溶剂萃取,降低了成本,避免了二次污染;
(2)操作时间短,从萃取进样到分析结束不足1h;
(3)样品用量少,几mL~几十mL;
(4)操作简便,可减少待测组分的挥发损失;
(5)检测限达 μg/L~ng/L水平;
(6)适于挥发性有机物、半挥发性有机物及不具挥发性的有机物。 ※固相微萃取的使用:关键在于“纤维头的选择”,这种情况类似于色谱柱的选择,主要根据分析对象的分子量和极性。固相微处理技术适用于气体、水样、生物样品(如,血、尿、体液等)的萃取提取。
浓缩法
食品样品经提取、净化后,有时净化液的体积较大,被测组分的浓度太低,会影响最后结果的测定。此时需要对被测样液进行浓缩,以提高被测成分的浓度。常用的方法有常压浓缩和减压浓缩两种:
1.常压浓缩法:
常压浓缩法只能用于待测组分为非挥发性的样品试液的浓缩,否则会造成待测组分的损失。操作可采用蒸发皿直接挥发。如果溶剂需要回收,则可用一般蒸馏装置或旋转蒸发器。该法操作简便、快速,是常用的方法。
2.减压浓缩法:
减压浓缩法主要用于待测组分为热不稳定性或易挥发的样品净化液的浓缩,其样品净化液的浓缩需采用K-D浓缩器。浓缩时,水浴加热并抽气减压,以便浓缩在较低的温度下进行,且速度快,可减少被测组分的损失。食品中有机磷农药的测定(如,甲胺磷、乙酰甲胺磷)多采用此法浓缩样品净化液。
蛋白纯化
蛋白质的分离、纯化对蛋白质结构功能研究具有重要意义,蛋白质分离技术是利用蛋白质的特性,如,溶解度、分子质量大小、等电点、吸附特性和其它离子的生物亲和力等的不同,选择合适的分离模式并建立最佳的纯化方法。常用的分离方法包括沉淀法、色谱法和电泳及毛细管电泳。 几种方法供你选择!
(1)沉淀法利用蛋白质在溶液中的不同溶解度。蛋白质的溶解度取决于分子中氨基酸的类型和电荷数,通过改变缓冲液pH值、离子强度、介电常数或温度而改变蛋白质的溶解度。主要使用的沉淀分离技术有盐析、等电点沉淀、溶剂分级分离。
(2)透析法利用半透膜只允许小分子透过而大分子不能透过的原理来分离溶液中的蛋白质。通常至少需要12h。
(3)超滤法采用半透膜在一定压力下,按照分子质量大小分离溶质的一门技术。与透析相似,但速度快得多。 蛋白质的构成成分:氨基酸前处理1.氨基酸的分离和检测手段,以往用化学分析法、层析法、比色法、气相色谱法、氨基酸自动分析仪。
2.随着高效液相色谱及填料的发展,HPLC在氨基酸检测方面显示了其特有的优越性,但大多数氨基酸无紫外吸收和荧光发射特性,为提高分析检测灵敏度和分离选择特性,通常将氨基酸衍生,衍生方式有柱前衍生法与柱后衍生法。
3.HPLC与各种衍生相结合的氨基酸分析技术,构成了具有广泛适用性的现代氨基酸分析技术。 样品处理测定蛋白质中的总氨基酸,必须先把蛋白质水解成游离氨基酸。可采用酸水解、碱水解和酶水解方法,其中以酸水解法应用最广泛。
(1)酸水解条件:常用硫酸或盐酸进行水解。一般用6mol/LHCl,4mol/L H2SO4煮沸回流24小时左右。优点:可蒸发除去盐酸,水解彻底,终产物为L-α-氨基酸,产物单一,无消旋现象。缺点:色氨酸破坏,丝氨酸和苏氨酸有一小部分被水解,同时天冬酰胺和谷氨酰胺的酰胺基被水解下来。
(2)碱水解条件:分析色氨酸可采用碱水解法,一般与5mol/L NaOH煮沸10~20小时。优点:水解彻底,色氨酸不被破坏,水解液清亮。缺点:产生消旋产物,破坏的氨基酸多。
(3)酶水解某些氨基酸对酸或碱不稳定,在酸或碱水解时易被破坏,某些蛋白质样品在酸或碱水解不完全,影响某些氨基酸的回收率。对这些样品可采用酶水解法。酶水解法可定量测定天东氨酸、谷氨酸和色氨酸。条件:蛋白酶,如,胰蛋白酶、糜蛋白酶,常温37~40℃, pH值5~8 。优点:氨基酸不被破坏,不发生消旋现象。缺点:水解不完全,中间产物多。
生物样品分析前处理技术
为什么要进行前处理? 存在形式多样:游离型药物、与蛋白质结合型药物、代谢物、葡萄糖醛酸苷、硫酸酯缀合物等。 成分复杂:蛋白质、糖、脂肪、尿素、Na+、K+、X-等。
(1)去除蛋白质释放结合型药物、减少提取过程中乳化、保护仪器、提高灵敏度。。。加入与水混溶的有机溶剂中性盐强酸加入含锌盐、铜盐的沉淀剂酶解法
(2)缀合物的水解酸水解/酶水解
(3)有机破坏测定生物样品中的金属离子,常用HNO3-HClO4作为消解剂,一般得到高价态金属离子。
(4)分离、纯化和浓集使被测物在所用分析技术的检测范围内,常用萃取法:液-液萃取法(LLE)液-固萃取法(LSE)相当于缩小的柱色谱法浓集末次萃取液尽量少挥去萃取溶剂
(5)化学衍生化可使药物:具有能被分离的性质提高灵敏度增强稳定性提高对光学异构体分离的能力

来源:Internet


