您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-05-19 11:39
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
恒瑞CTLA-4单抗获批Ib/II期临床。恒瑞医药2.2类新药SHR-8068注射液获国家药监局临床试验默示许可,拟联合PD-L1阿得贝利单抗、及贝伐珠单抗或含铂化疗开展用于治疗晚期实体肿瘤的Ib/II期临床。SHR-8068是恒瑞引进的一种全人源抗CTLA-4单克隆抗体,可增强抗肿瘤免疫效应。目前同类产品仅有BMS的伊匹木单抗获批上市,其2021年全球销售额为20.26亿美元。
国内药讯
1.创新钙通道阻滞剂在华启动Ⅲ期临床。Milestone公司与箕星药业联合开发的etripamil鼻喷雾剂在中国登记启动一项Ⅲ期临床。该项临床评估Etripamil鼻喷雾剂自行用药用于中国患者终止阵发性室上性心动过速自发性发作的有效性和安全性。主要研究者由首都医科大学附属北京安贞医院医学博士马长生担任。etripamil是Milestone开发的一款新型钙通道阻滞剂,该新药也正在Ⅱ期试验中用于治疗心房颤动伴快速心室率(AFib-RVR)患者。
2.君实新冠口服药临床数据积极。君实生物与旺山旺水生物合作开发的核苷类抗新冠病毒药物Renmindevir(VV116)针对Omicron感染者的初步临床结果发表在Emerging Microbes & Infections上。结果显示,在首次核酸检测阳性5日内接受VV116治疗的患者核酸转阴时间为8.56天,而对照组为11.13天;在首次核酸检测阳性5日后接受VV116治疗的患者核酸转阴时间为11.46天,与对照组相比没有显著差异;VV116治疗组未观察到严重不良反应。
3.恒瑞PD1单抗食管癌最新结果积极。恒瑞医药PD1卡瑞利珠单抗联合紫杉醇和奈达铂新辅助治疗局部晚期食管鳞癌的Ⅱ期临床(ESPRIT)积极结果将在AATS2022年会上以口头报告形式分享。初步结果显示,卡瑞利珠单抗组合疗法用于新辅助治疗能够缩小肿瘤并完成降期,35%患者达到病理完全缓解;治疗药物引起的不良反应可控,无不良反应导致的治疗延迟事件发生。
4.复宏汉霖注射用曲妥珠单抗增效扩产。复宏汉霖宣布公司已收到NMPA核准签发关于汉曲优® (注射用曲妥珠单抗,欧洲商品名:Zercepac®)的《药品补充申请批准通知书》,同意汉曲优®变更生产场地、优化生产工艺及扩大制剂规模等补充申请。此次获批标志着松江基地(一)的24000L产能可以全部应用于汉曲优®的商业化生产,积极助力汉曲优®增效扩产,也表明公司的商业化总产能扩增至48000L。
5.森朗生物完成2亿元人民币融资。河北森朗生物宣布完成2亿元人民币融资,本轮融资由前海母基金独家投资。易凯资本担任独家财务顾问。森朗生物目前已建成高效的细胞治疗创新技术平台,并在此平台上研发生产了包括新型靶向CD19 CAR-T、靶向CD7 CAR-T、组合(Combo)CAR-T、通用型 CAR-γδT 以及针对实体瘤的多个领先产品。本轮融资主要用于公司现有管线的推进、新产品的研发及技术平台的升级迭代。
国际药讯
医药热点
1.武汉大学人民医院分子医学研究院成立。武汉大学人民医院日前与武汉大学化学与分子科学学院召开战略合作会议,双方签署战略合作框架协议,共同成立“武汉大学人民医院分子医学研究院”并揭牌。该研究院旨在推动医学与化学、分子科学的交叉融合,聚焦分子医学前沿,搭建创新研究与转化平台。中科院院士、武汉大学化学与分子科学学院教授周翔受聘担任武汉大学人民医院分子医学研究院名誉院长。
2.易学锋任广东省卫健委副主任。5月17日,广东省人民政府新闻办公室官方微信公众号发布任免工作人员名单,涉及医药卫生健康领域的人员共有4位。其中,任命易学锋为广东省卫健委副主任,试用1年。根据卫健委官网信息,此前易学锋任广东省职业病防治院党委书记。任命翟理祥为广东药科大学校长,试用1年。此前翟理祥任广东省中医院党委副书记、副院长兼珠海医院院长、党委书记。任命肖炜为广东药科大学副校长,试用1年。此前肖炜任南方医科大学中医药学院院长、党委副书记。免去郭姣的广东药科大学校长职务。
3.上海:驾车离沪证明6小时内有效。根据上海市疫情防控“防外溢”要求,在沪人员原则上“非必要不离沪”。对有工作、学习、生活等确需驾驶机动车离沪的人员,在符合疫情防控规定的前提下,可向有关单位提出申请。离沪证明自申报的出发之时起,6小时内有效。相关人员凭离沪证明驾驶机动车离沪,点对点前往外省市目的地。
4.体内模型证实Omicron毒力低于原始毒株。5月16日,Nature杂志发表美国威斯康星大学和日本东京大学的著名病毒学家、全世界最顶级的流感病毒专家,美国科学院院士Yoshihiro Kawaoka(河岡義裕)组的研究成果。研究选取了在日本分离的Omicron BA.2活病毒,感染人源化k18-hACE2小鼠和仓鼠。该研究首次通过金标准检测证实BA.2的毒力确实低于原始野生型。
评审动态
1. CDE新药受理情况(05月18日)

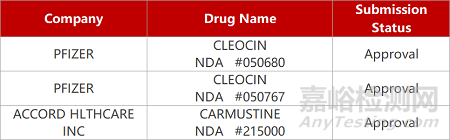

来源:药研发