您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-06-22 14:16
本文以流化床底喷上药为例,从起始丸芯“大与小”的选择,包衣膜的“厚与薄”简要转述前人的研究结论,以期加深对微丸包衣的理解。
所用内容参考Colorcon公司官网技术资料、《质量源于设计在ANDA中的应用缓释制剂示例》一书、陈挺老师部分学术报告资料和KAN shl的文献,在此表示感谢!
微丸制备考察因素
微丸制备影响因素众多,如下鱼骨图所示,列举出一般微丸生产常需考察的因素,涉及人、处方、过程控制、设备、环境五个方面,其中前四个方面大家平时较为关注,而环境因素(温、湿度)平时容易忽略,药事纵横文章《浅谈流化操作中空气湿度的重要性》简述流化床操作中湿度的重要性。
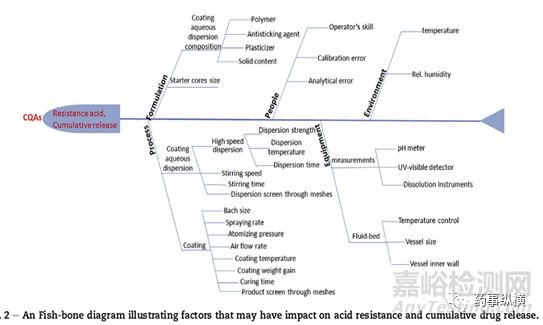
KAN shl , LU J , LIU JP ,ect. A quality by design(QbD)case study on enteric-coated pellets: Screening of critical variables and establishment of design space at laboratory scale [J]. Asian Journal of Pharmaceutical Sciences,2014.
起始丸芯的大与小
微丸的比表面积主要取决于粒径大小与分布情况,在符合灌装胶囊的前提下,尽量采用粒径较大的微丸,既可以节约包衣材料,缩短工艺时间,又有利于批内包衣均匀性和批间重现性。
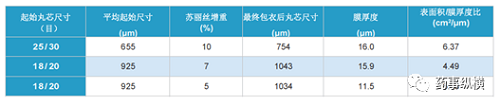
从下表中可以看出要同样形成10微米厚度的衣膜,当选用的起始丸芯的直径为1.0毫米时,包衣增重只需达到4.7%;而当选用的起始丸芯为0.25微米时,若药达相同的包衣增重,则包衣增重需达到20%,较小的丸芯和较大的包衣增重对工艺的耐受性提出较高的挑战,特别是在大生产级别时微丸的包衣,有时可能连续包衣数十小时,对设备耐受性、人的顺应性都是极大的挑战。
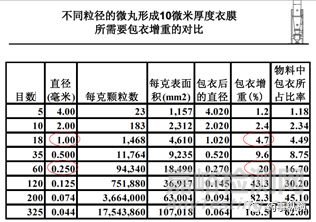
(《流化床包衣技术及其在缓控释制剂上的应用》陈挺 德国Glatt公司上海实验室 2013.02.06 上传于百度文库)
借助膜厚度实现大与小的转换
如处方一:起始丸芯使用25/30目,使用为粘合剂将扑尔敏上药于药用丸芯上。应用同样的欧巴代配方(增重5%)做封闭包衣(隔离层),随后应用乙基纤维素水分散体B型 (增重10%)进行控释膜包衣(功能包衣层),制成多颗粒缓释制剂。现将起始丸芯调整为18/20目,包衣增重如何调整?
(《为什么选择更大的丸芯?》Gus LaBella, Jason Hansell, Scott Vass Colorcon,Inc., Harleysville, PA USA www.colorcon.com)

(图摘自《流化床包衣技术及其在缓控释制剂上的应用》陈挺德国Glatt公司上海实验室 2013.02.06 上传于百度文库)
|
项目 |
处方一 |
处方二 |
|
起始丸芯 |
25/30目 |
18/20目 |
|
含药层 |
17% |
同剂量 |
|
封闭层 |
5% |
待预测 |
|
功能层 |
10% |
待预测 |
摘自Colorcon 公司技术资料《为什么选择更大的丸芯?》
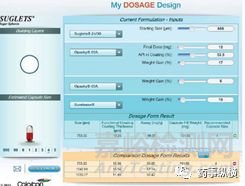
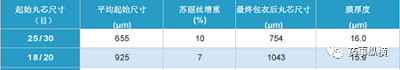
摘自Colorcon 公司技术资料《为什么选择更大的丸芯?》
卡乐康公司开发的“多颗粒处方设计”器可以提供理论支持,通过“多颗粒处方设计”,可以计算出在工艺不同阶段与多颗粒制剂相关连的变量;包括粒度、表面积、膜厚度、最终剂型的体积以及需要填充的胶囊壳的尺寸。通过计算,发现若要达到与小丸芯(25/30)相同的功能性包衣膜厚度,使用用大丸芯(18/20)则需将包衣增重由7%提高至10%。这样我们获得了相同的功能性包衣膜厚度。但按照理论包衣增重包衣时,发现使用大丸芯(18/20)包衣的微丸溶出慢于小丸芯(25/30),可能的原因为两者的包衣膜厚度虽然相同,但两者的微丸的数目不相同,导致其表面有较大的差异,尽而影响溶出速率。
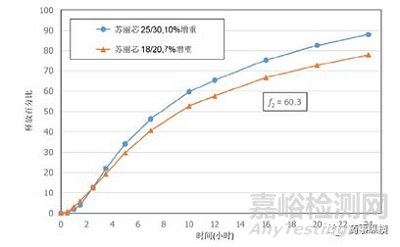
摘自Colorcon 公司技术资料《为什么选择更大的丸芯?》
借助“表面积(SA)和膜厚度(FT)的比率”实现大与小的转换
如果只考虑释膜的厚度,如上图所示,可以看出溶出方面的差别,原因在于丸芯更大时,暴露于溶出介质的总的表面积就会变小;导致药物释放率变慢。虽然相似因子f2值达到60.3,但从溶出曲线上可以看出明显的差别。使用设计工具可以计算出表面积以及与更大丸芯相似的表面积(SA)和膜厚度(FT)的比率,可以使不同大小的丸芯得到相似的药物释放。第三批18/20目的丸芯按相近的表面积:膜厚度比率来制备,如下图所示,这两批丸芯的f2 值是80.3。从另一个角度说明功能性材料包衣增重与膜厚度对体内外的重要影响。
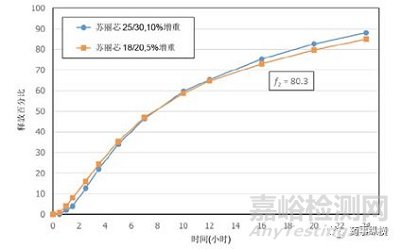
摘自Colorcon 公司技术资料《为什么选择更大的丸芯?》
相同剂量不同初始丸芯灌装胶囊通过“多颗粒处方设计”,起码解决了溶出更相似的问题,后续可结合溶出稳定性问题略作调整。也证明了无论起始丸芯的大小如何,都可以获得相似的药物释放。而当使用尺寸更大的丸芯包衣时,工艺过程变得更容易,而且起始丸芯的大小不会影响胶囊的填充体积。对于“特种微丸”(微丸压片)而言,需要得杂考量,如起始微丸大小影响片剂的微丸的数量,尽而影响外加辅料的量,每个微丸压片时所受的“应力”尽而可能不同,同时还需考虑可能的分层风险,因为粒径越小,压片时物料分层的可能性越小。
微丸放大时的“厚与薄”
通常情况下,从实验室工艺到中试、生产放过程中,进风温度不变,为了提高喷液速率,可提高进风温度,但必须保持物料温度恒定不变,减小季节性环境湿度增大的影响,可适当提高进风温度,以保证恒定的物料温度。
通过维持进风风量和分布板面积比例,以及喷雾速度和风量的比例,可以使用流化床对层积上药进行线性放大。在工艺放大时,设备中的线性空气流速一般保持恒定,进风量根据分布板面积按比例放大,从而尽量保证微丸通过“物色柱”的时间相同,接授包衣液的机率相同。
《质量源于设计在ANDA中的应用缓释制剂示例》一书提到商业化大生产规模的首个验证批没有通过溶出度检测。随后研究发现,相同的理论包衣增生条件下,中试批薄膜厚度为41±2微米,而商业化大生产规模的厚度为46±3微米;尽而导致溶出曲线不相似。
通过分析必现,商业化大生产规模的生产设备利用了71%的容积,而中试规模生产只利用了62%的容积;紧紧由于规模扩大,效率的提高,30%理论聚合物包衣的含药微丸总的膜厚度即有所增加,验证首批的薄膜厚度相较中试批薄膜厚度增加了5个微米,预测的T50从5.6小时增加到6.6小时,不符合预定的关键质量属性合格标准。为了获得与中试规模相同的释放和生物等效性结果,即将理论聚合物包衣水平从30%降至28%。在第二个验证批生产时,就把理论聚合物的包衣水平从30%降低到28%,后来研究发现获得预定的目标。
讨论
以上两个事例的共同特点是微丸溶出形为高度依赖于功能性包衣膜的厚度,提示我们在相关仿制药研发的过程中关注点在哪,当然功能性包衣的膜的厚度可以通过扫描电镜或太赫兹脉冲成像(TPI)进行检测,但功能性包衣的膜的另一关键性质膜的致密性往往不好直接评价,有时常通过体外释放形为来间接评价,这里需要关注膜的厚度与致密程度的叠加影响,即膜的致密性比较差,但增重较后,体外释放形为可能相近,需将膜厚度与体外溶出情况综合对比、考量研究。微丸功能性包衣是一个系统复杂的综合工程,需人、机、料、环等因素完美配合,才能持续、可控生产出期望的产品。
展望
与普通剂型(single-unit dosgeform)相比,微丸及其制剂作为多单元给药系统(Multiple-unitpellet system),具有吸收充分、均一与胃肠道接触位点多;个别微丸的缺陷不影响整体的释药行为;避免突释,药物释放稳定、变异少;释药模式多样:定速、定位、定时;副作用少,生物利用度高等特点。同时微丸制备工艺相对复杂,仿制难高较高,相信在未来一段时间内,仍将各大仿制药公司争角逐的焦点。
【参考文献】
1.FDA《质量源于设计在ANDA中的应用缓释制剂示例》
2.《流化床包衣技术及其在缓控释制剂上的应用》陈挺,德国Glatt公司上海实验室 2013.02.06 上传于百度文库
3.Colorcon 公司技术资料《为什么选择更大的丸芯?》Gus LaBella, Jason Hansell, Scott Vass Colorcon,Inc., Harleysville, PA USA
4.KAN shl , LU J , LIU JP ,ect. A quality bydesign(QbD)case study on enteric-coated pellets:Screening of critical variables and establishment of design space at laboratoryscale [J]. Asian Journal of Pharmaceutical Sciences,2014.

来源:药事纵横


