您当前的位置:检测资讯 > 热点事件
嘉峪检测网 2022-10-26 06:48
近期,南开大学生命科学学院/药物化学生物学国家重点实验室赵强教授与Adam C. Midgley副教授在科爱出版创办的期刊Bioactive Materials上联合发表题为“Anti-Sca-1 antibody-functionalized vascular grafts improve vascular regeneration via selective capture of endogenous vascular stem/ progenitor cells”的研究论文。该研究利用血管干/祖细胞特异性标志物Sca-1抗体对静电纺丝技术制备的聚己内酯人工血管进行功能化修饰。功能化人工血管在植入体内后可以通过选择性捕捉内源性血管干/祖细胞促进血管组织再生。
01 研究内容简介
心血管疾病(CVD)因其高发病率和致死率,已成为全球范围内的重大公共卫生问题。近年来,由合成可降解材料制备的小口径(< 6 mm)人工血管因其具有良好的生物相容性和力学性能受到了广泛关注。然而,由于合成材料缺乏抗凝血活性和诱导组织再生的功能,血管植入体内后常发生血栓和内膜增生等问题,导致血管再狭窄。因此,构建具有诱导组织再生功能的活性生物材料是解决人工血管再狭窄问题并实现其临床转化的有效途径之一。
血管干/祖细胞(Stem/progenitor cell, SPC)具有自我更新和多向分化潜能,在维持血管稳态和调控血管重构中发挥重要作用。研究表明,SPC可以在体内和体外条件下分化为血管细胞,包括血管内皮细胞(EC)和平滑肌细胞(SMC),是血管组织修复再生的重要细胞来源。
该研究首先利用静电纺丝技术制备了聚己内酯(PCL)人工血管。然后,通过生物素-亲和素(Biotin-Avidin)反应将Sca-1抗体修饰到PCL人工血管表面(图1A),获得了一种Sca-1抗体功能化修饰的人工血管(PCL-Sca-1 Ab)。在材料的制备和表征方面,该研究首先通过扫描电子显微镜(SEM)和激光共聚焦成像(CLSM)考察了PCL-Sca-1 Ab人工血管的微观结构和表面形态(图1B和C)。其次,力学测试显示了抗体修饰前后两种人工血管的力学强度和爆破压均能满足体内移植的要求(图1D和F)。此外,表面功能化修饰提高了人工血管的亲水性(图1E),降低血小板和纤维蛋白原的粘附,从而改善人工血管的血液相容性(图1G和H)。
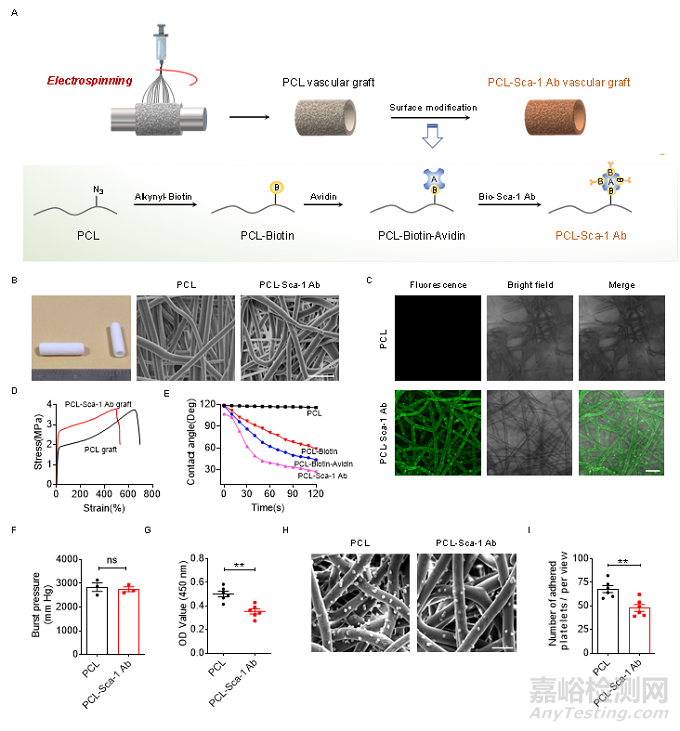
图1 Sca-1抗体功能化修饰的人工血管的制备与表征
为了考察Sca-1抗体功能化修饰后的人工血管对Sca-1+的血管干/祖细胞(Sca-1+ SPCs)的作用,研究人员首先从大鼠的血管外膜中分离出Sca-1+ SPCs。然后,在静态培养的条件下比较了Sca-1抗体功能化修饰前后人工血管对Sca-1+ SPCs的粘附情况。此外,还利用3D流动培养生物反应器在模拟生理条件下比较了PCL和PCL-Sca-1 Ab人工血管对Sca-1+ SPCs的捕捉以及细胞在血管的驻留情况。结果表明,无论是在静态还是流动培养条件下,Sca-1抗体功能化修饰均显著改善了人工血管对Sca-1+ SPCs细胞的粘附和捕捉(图2)。
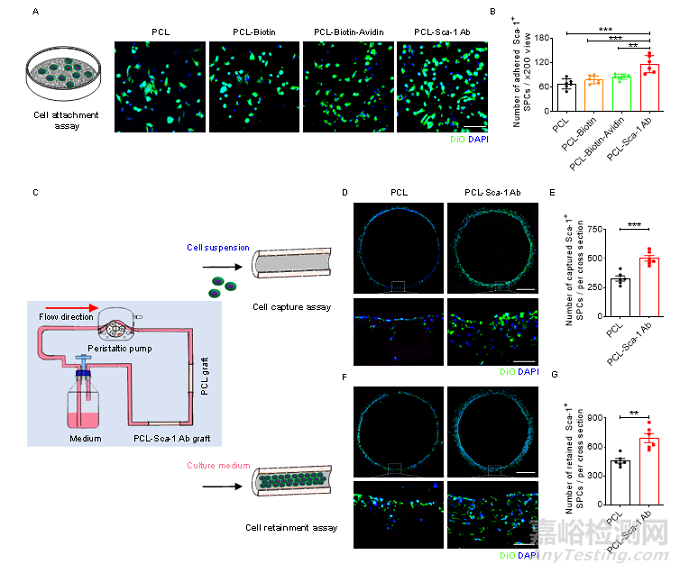
图2 体外细胞粘附和捕捉实验
将PCL和PCL-Sca-1 Ab两组人工血管分别移植到大鼠腹主动脉来比较两组人工血管的体内组织再生情况(图3)。在移植后的2周和4周时取材分析,通过H&E、番红O、Masson和VVG染色来分别考察人工血管植入后组织再生和细胞外基质(ECM)的分泌。染色结果显示,相比于PCL对照组,PCL-Sca-1 Ab的组织再生更好,而且人工血管的管壁中分布着更多的胶原和糖胺聚糖。
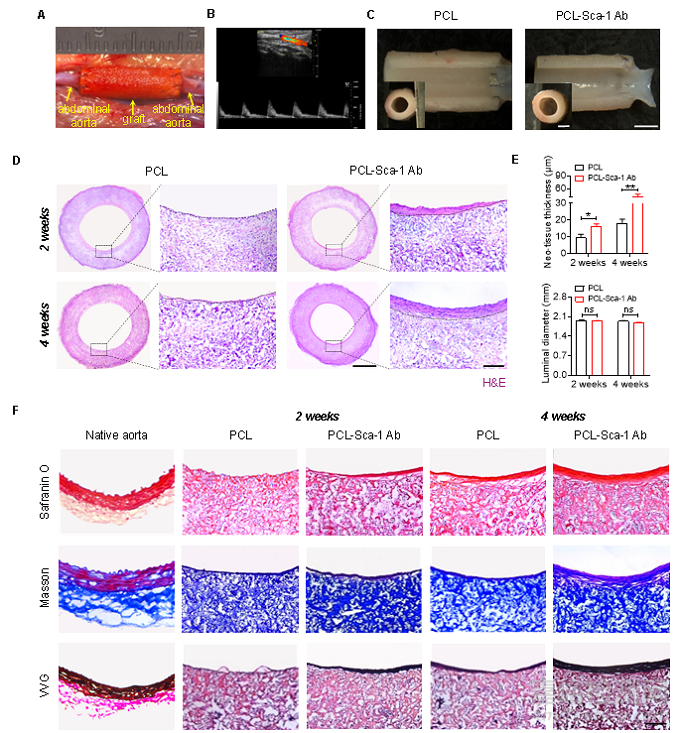
图3 人工血管体内移植后的组织再生情况
血管内皮为防止血栓形成和再狭窄提供了良好的天然屏障,是维持人工血管长期通畅的重要保障。因此,人工血管植入后的内皮化程度是反映血管组织再生的一个重要指标。在该研究中,研究人员通过SEM和En face免疫荧光染色观察人工血管表面的内皮覆盖情况。结果显示,PCL-Sca-1 Ab人工血管的内皮覆盖率显著高于对照组,且再生的ECs呈鹅卵石样形态,并沿血流方向规则排列,与天然动脉相似(图4)。
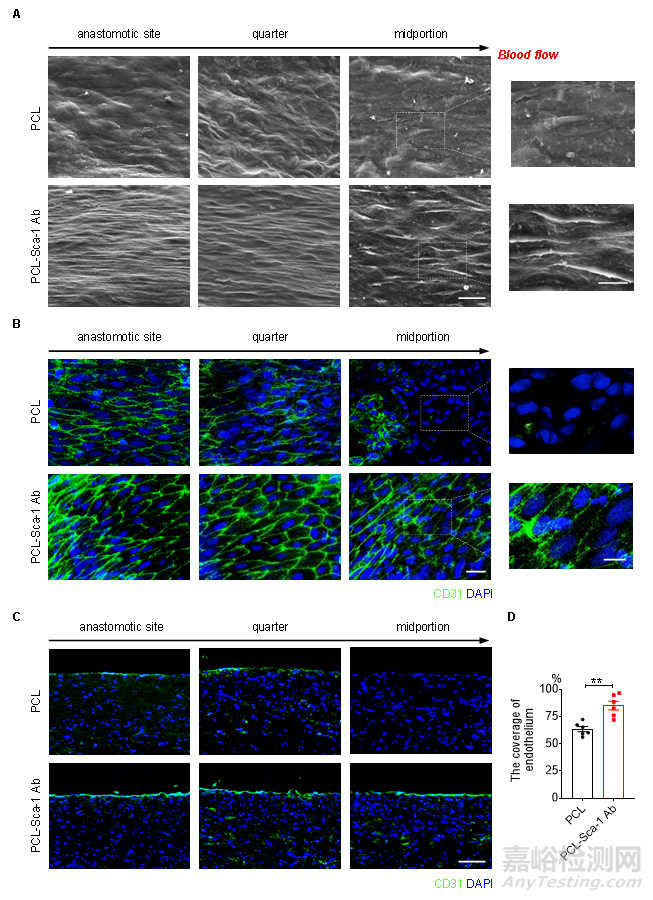
图4 人工血管体内移植后的内皮再生情况
血管平滑肌层在维持血管的力学强度、调节血管的舒张收缩功能等方面发挥着重要作用。因此,研究人员分别用α-SMA和SM-MHC免疫荧光染色对再生平滑肌的表型进行了考察(图5)。α-SMA+的免疫荧光照片显示,2周时PCL-Sca-1 Ab组可观察到均匀分布的α-SMA+细胞,4周时细胞排列更为紧密。而PCL人工血管,2周时,α-SMA+细胞的再生有限,4周时,α-SMA+细胞数量有所增加(图5A)。SM-MHC+平滑肌再生表现出类似的趋势(图5C)。
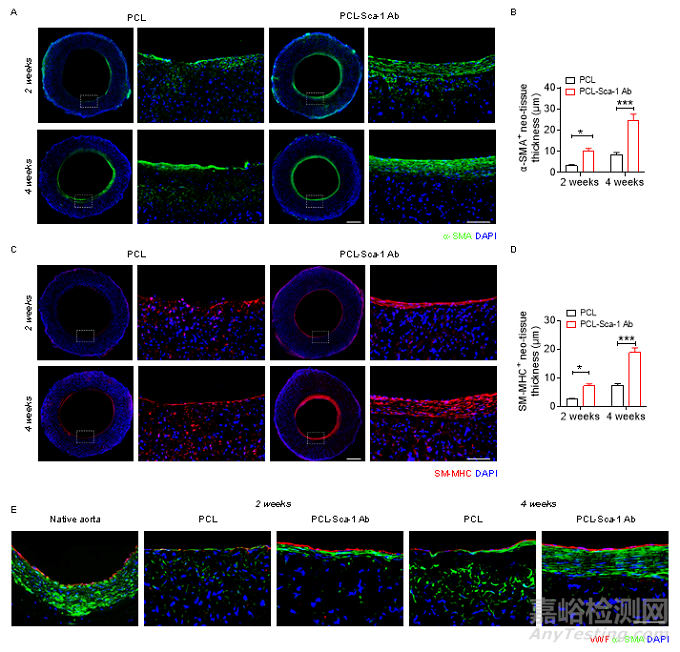
图5 人工血管体内移植后的平滑肌再生情况
体外实验结果显示Sca-1抗体功能化修饰提高了人工血管对Sca-1+ SPCs的粘附和捕获。进一步,研究人员在大鼠腹主动脉移植模型中深入研究了Sca-1+ SPCs的体内浸润情况(图6)。结果显示,在植入2周和4周后,PCL-Sca-1 Ab人工血管中Sca-1+ SPCs细胞的数量显著高于对照组。这些Sca-1+ SPC可进一步分化成为EC和SMC细胞,促进血管组织再生。
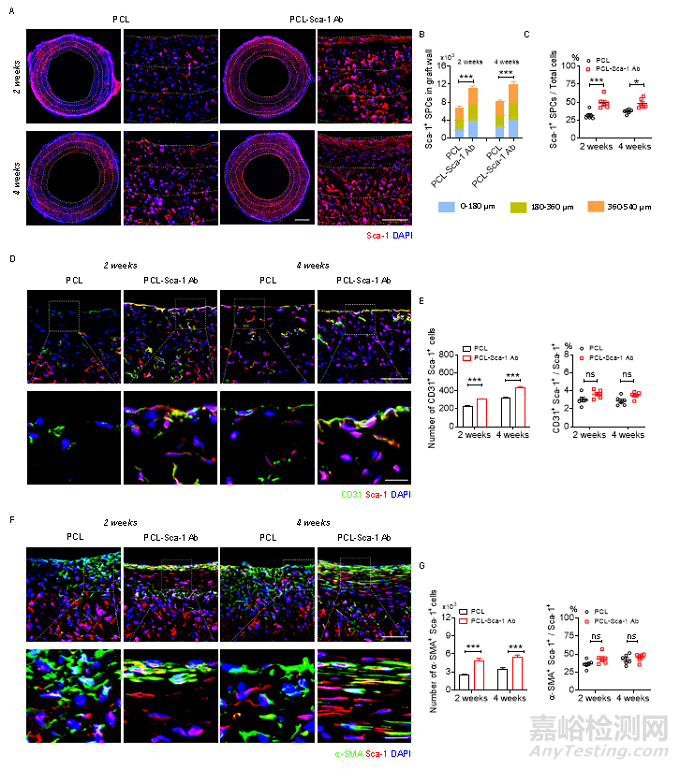
图6 人工血管体内移植后的Sca-1+ SPCs的浸润和分化情况
接下来,研究人员利用Sca-1 2A-CreER; Rosa-RFP遗传谱系示踪小鼠并构建了骨髓移植模型(BMT)来考察参与血管组织再生的SPCs的来源和命运(图7)。
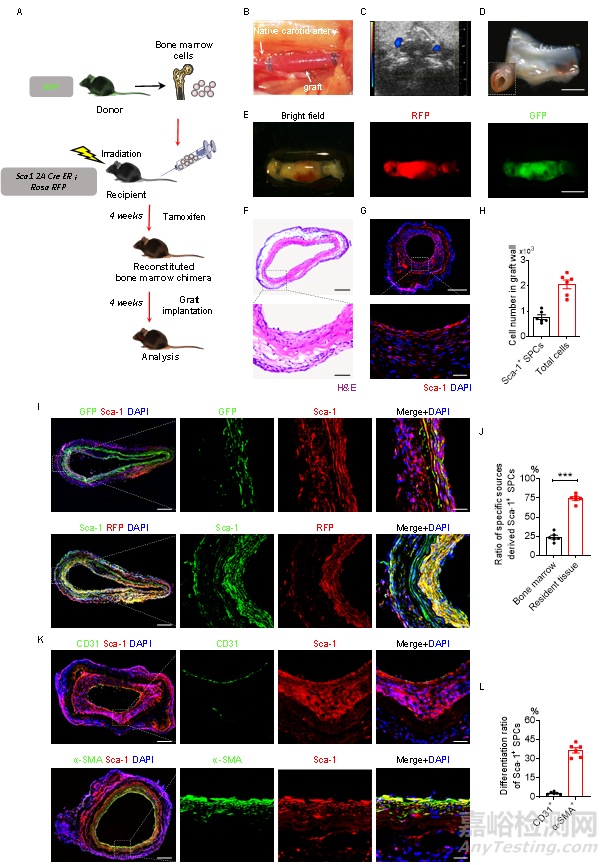
图7 利用骨髓移植模型并结合遗传谱系示踪小鼠揭示参与血管组织再生的Sca-1+ SPCs的来源和命运
在BMT小鼠颈动脉移植模型中,研究人员发现参与血管组织再生的Sca-1+ SPCs大部分来自血管外周组织,也有少量来自骨髓/外周血(图7I)。这些募集的Sca-1+ SPCs会进一步的向ECs和SMCs分化来参与血管组织再生(图7K)。
综上,该研究设计制备了一种Sca-1抗体功能化修饰的人工血管,其能够捕捉内源性血管干/祖细胞,有效改善血管组织再生。同时利用遗传谱系示踪小鼠并结合骨髓移植模型,进一步考察了参与血管再生的干/祖细胞来源和分化情况。该研究成果不仅为功能型小口径人工血管制备提供了新的策略,而且为血管干细胞和组织再生机制研究提供了有力的支撑。

来源:BioactMater生物活性材料


