您当前的位置:检测资讯 > 监管召回
嘉峪检测网 2022-07-05 13:23
近日,河南药监局发布了一则行政处罚的案例,一械企因未建立质量管理体系并保持有效运行被行政处罚:
处罚详情
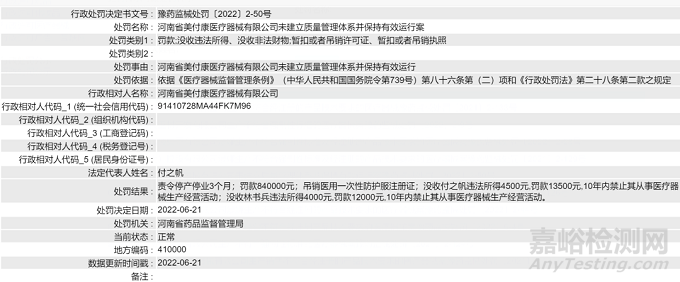
处罚结果
责令停产停业3个月;罚款840000元;吊销医用一次性防护服注册证;没收付之帆违法所得4500元,罚款13500元,10年内禁止其从事医疗器械生产经营活动;没收林书兵违法所得4000元,罚款12000元,10年内禁止其从事医疗器械生产经营活动。
处罚依据
依据《医疗器械监督管理条例》(中华人民共和国国务院令第739号)第八十六条第(二)项和《行政处罚法》第二十八条第二款之规定
《医疗器械监督管理条例》第八十六条
有下列情形之一的,由负责药品监督管理的部门责令改正,没收违法生产经营使用的医疗器械;违法生产经营使用的医疗器械货值金额不足1万元的,并处2万元以上5万元以下罚款;货值金额1万元以上的,并处货值金额5倍以上20倍以下罚款;情节严重的,责令停产停业,直至由原发证部门吊销医疗器械注册证、医疗器械生产许可证、医疗器械经营许可证,对违法单位的法定代表人、主要负责人、直接负责的主管人员和其他责任人员,没收违法行为发生期间自本单位所获收入,并处所获收入30%以上3倍以下罚款,10年内禁止其从事医疗器械生产经营活动:
(一)生产、经营、使用不符合强制性标准或者不符合经注册或者备案的产品技术要求的医疗器械;
(二)未按照经注册或者备案的产品技术要求组织生产,或者未依照本条例规定建立质量管理体系并保持有效运行,影响产品安全、有效;
(三)经营、使用无合格证明文件、过期、失效、淘汰的医疗器械,或者使用未依法注册的医疗器械;
(四)在负责药品监督管理的部门责令召回后仍拒不召回,或者在负责药品监督管理的部门责令停止或者暂停生产、进口、经营后,仍拒不停止生产、进口、经营医疗器械;
(五)委托不具备本条例规定条件的企业生产医疗器械,或者未对受托生产企业的生产行为进行管理;
(六)进口过期、失效、淘汰等已使用过的医疗器械。

来源:CMDRA


