您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-04-14 10:50
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
拜耳“不限癌种”疗法在华获批。拜耳口服TRK抑制剂硫酸拉罗替尼胶囊获国家药监局批准上市,用于治疗携带NTRK融合基因的实体瘤成人和儿童患者。在多项临床试验中,拉罗替尼在成人和儿童TRK基因融合癌症,包括中枢神经系统癌症中,均显示出高缓解率,且持续缓解时间超过3年。在美国,FDA曾授予该新药突破性疗法认定、孤儿药资格和罕见儿科疾病认定,并于2018年加速批准上市,商品名为Vitrakvi。
国内药讯
1.百济神州PD-1单抗获批治疗ESCC。百济神州PD-1替雷利珠单抗(百泽安)获国家药监局批准第8项适应症,用于治疗既往接受过一线标准化疗的局部晚期或转移性食管鳞状细胞癌(ESCC)患者。在一项Ⅲ期临床RATIONALE 302中,替雷利珠单抗在ITT人群的中位总生存期达8.6个月,降低死亡风险超过30%。替雷利珠单抗用于上述适应症的上市申请已在美国递交,PDUFA日期为2022年7月12日。
2.正大天晴安罗替尼新适应症获批上市。正大天晴抗血管生成创新药安罗替尼获国家药监局批准新适应症,此前该新药已获批用于治疗非小细胞肺癌、软组织肉瘤、小细胞肺癌和甲状腺髓样癌等4项适应症,此次获批的新适应症推测为分化型甲状腺癌。目前,正大天晴正在开发安罗替尼与PD-L1单抗TQB2450,或与康方生物派安普利单抗联合治疗多个癌种的潜力。
3.赛诺菲罕见病新药启动国际Ⅲ期临床。赛诺菲口服葡糖神经酰胺合成酶(GCS)抑制剂venglustat在国内登记启动一项国际Ⅲ期临床,评估与法布雷病标准治疗相比,venglustat治疗18个月对法布雷病伴左心室肥大受试者左心室质量指数的影响。该研究中国主要研究者为上海交通大学医学院附属瑞金医院金玮博士,拟在中国入组12例患者,国际入组90例患者。GCS是糖鞘脂(GSL)代谢途径中的关键调节因子。
4.志健金瑞RET抑制剂临床前研究积极。志健金瑞在AACR2022年会上公布其高选择性RET抑制剂APS03118临床前研究结果。与selpercatinib和pralsetinib相比,APS03118对野生型和一系列RET突变和融合有效,特别是对导致RET抑制剂耐药的溶剂前沿突变 (SFMs)RET G810R/S/C,屋顶突变RET L730I/M,守门员突变RET V804M/L/E和铰链突变RET Y806 H。APS03118在KIF5B-RET PDX、KIF5B-RET V804M CDX和KIF5B-RET G810R CDX等小鼠异种移植瘤肿模型中有强效抑瘤活性。在CCDC6-RET脑原位移植瘤PDX模型中,APS03118治疗组肿瘤完全消退,小鼠存活率为100%。
5.贝达药业恩沙替尼新适应症获批临床。贝达药业ALK抑制剂恩沙替尼胶囊新适应症获批临床,拟用于ALK阳性非小细胞肺癌(NSCLC)术后辅助治疗。恩沙替尼是目前唯一一款获批上市的国产ALK抑制剂,已获批用于既往接受过克唑替尼治疗的ALK阳性、局部晚期或转移性NSCLC患者,以及用于一线治疗ALK阳性的NSCLC患者。该新药已通过医保谈判进入新版医保目录。
国际药讯
1.艾伯维navitoclax骨髓纤维化Ⅱ期临床积极。艾伯维在AACR 2022年会上公布口服BCL-XL/BCL-2抑制剂navitoclax联合JAK1/2抑制剂ruxolitinib治疗骨髓纤维化(MF)患者的Ⅱ期临床REFINE(NCT03222609)新数据。经过2年以上的随访,对于BMF改善≥1级或VAF减少≥20%的患者,生存率估值达到100%;所有患者的总生存期尚未达到;没有发生出血严重不良事件。
2.阿斯利康PARP1抑制剂早期临床积极。阿斯利康在AACR大会上公布新一代PARP1抑制剂AZD5305首个人体试验积极结果。在40例可评估的晚期实体瘤患者中,10例获得部分缓解,11例疾病稳定。而且临床获益与此前是否接受过PARP抑制剂治疗无关。在接受循环肿瘤DNA(ctDNA)检测的13例患者中,8例患者的ctDNA水平下降,包括所有携带BRCA2突变的前列腺癌患者。目前,AZD5305正在国内开展一项国际I/IIa期临床PETRA。
3.Numab三抗公布临床前研究结果。Numab公司开发的PD-L1/4-1BB/HSA多特异性抗体NM21-1480(CS2006)在AACR2022年会上公布临床前研究成果。数据表明,NM21-1480仅在与肿瘤细胞表面的免疫检查点配体PD-L1结合时,才能条件性地诱导免疫共刺激受体4-1BB,激活T细胞;NM21-1480独特的单价结构设计可同时达到最佳的PD-L1抑制与4-1BB激活;此外,通过结合HSA可延长其半衰期,为患者提供更加便利的给药频率。基石药业拥有NM21-1480在大中华区、韩国和新加坡的独家授权。
4.Telix引进礼来放射性标记olaratumab。Telix公司宣布与礼来签订独家许可协议,获得礼来放射性标记形式的olaratumab抗体,用于诊断和治疗人类癌症。Olaratumab最初被礼来开发作为靶向血小板衍生生长因子受体 α (PDGFRα) 的(非放射性标记)单克隆抗体,2016年10月获FDA批准用于治疗成人软组织肉瘤(STS)。根据协议,礼来将获得500万美元预付款,以及可能高达2.25亿美元的里程碑潜在付款。
5.BioNTech布局开发口服mRNA疫苗。BioNTech公司与Matinas BioPharma将利用后者的脂质纳米晶体(LNC)递送平台技术,合作推进mRNA疫苗的新剂型开发,包括开发一种口服疫苗的潜在制剂。临床前和临床数据表明,这项新技术可以为小分子和更大、更复杂的分子(如mRNA、DNA质粒、反义寡核苷酸和疫苗)实现安全有效的细胞内递送提供解决方案。根据协议,Matinas将从BioNTech获得预付独家准入费以及额外的研究资金。
6.吉利德Trodelvy遭英国NICE拒绝批准。英国国家卫生与临床优化研究所(NICE)发布一份指南草案,建议拒绝批准吉利德TROP2-ADC新药Trodelvy用于治疗三阴性乳腺癌。NICE认为该药物成本效益估计值高于国家医疗服务系统(NHS)的标准。目前,NICE已推荐使用罗氏的Tecentriq与化疗联合治疗三阴性乳腺癌。吉利德计划与NICE合作解决围绕成本效益所提出的问题,争取在5月10日前达成协议。
医药热点
1.重庆首家三甲传染病专科医院成立。重庆市卫健委4月11日下发通知,确定重庆市公卫医疗救治中心为国家三级甲等专科医院。重庆市公卫医疗救治中心也是重庆首个三甲传染病专科医院。该中心建成多个结核病亚专科、艾滋病亚专科,涵盖内、外、中医等多个学科,覆盖结核病、艾滋病诊疗全领域,是重庆市及周边地区传染病急危重症患者的主要收治机构。
2.“抗菌抗病毒”口罩或存在安全风险。4月12日,国家药监局发布《“抗菌抗病毒”口罩消费风险提示》指出,目前市面上出现的宣称“抗菌抗病毒”非医用口罩,一般通过共混、喷涂等方式添加各类抗菌剂,主要添加物包括纳米二氧化钛、纳米银、季铵盐、铜离子/氧化铜、中药提取物等。该类产品的安全性有效性应当开展充分研究和验证。建议消费者依据新冠疫情联防联控机制印发的口罩选择与使用技术指引,科学选择合适的口罩类型。
3.两家医药公司被SEC列入“预摘牌名单”。当地时间4月12日,美国证劵交易委员会(SEC)再将12家中概股公司加入“预摘牌”名单,这是自3月以来第四批被纳入名单的中概股公司。这12家中概股公司包含传奇生物、康乃德生物两家医药公司。2022年3月29日,SEC官网显示,百济神州、再鼎医药、和黄医药等未能从《外国公司问责法》(HFCAA)的暂定名单中清除,被正式列入确认订单。
4.恒瑞首席医学官邹建军离职。恒瑞医药发布公告,宣布首席医学官(CMO)兼副总经理邹建军离职;聘任张晓静女士为公司副总经理、 首席医学执行官(肿瘤)。邹建军在恒瑞工作6年多期间,恒瑞医药将7款创新药、17个新适应症推向上市,包括硫培非格司亭、吡咯替尼、卡瑞利珠单抗、氟唑帕利、海曲泊帕乙醇胺、达尔西利、恒格列净。此外,还有3个产品的NDA(PDL1、AR、DPP-4)在审评中,预计在2022年获批上市。
评审动态
1. CDE新药受理情况(04月13日)
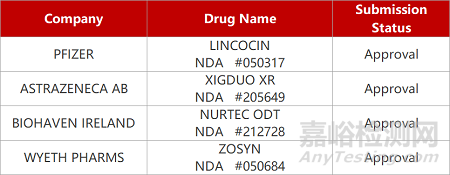
2. FDA新药获批情况(北美04月11日)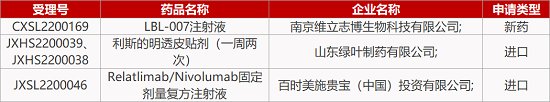

来源:药研发


