您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-04-04 17:45
2021年2月FDA发布关于亚硝胺杂质控制的指南 Control of Nitrosamine Impurities in Human Drugs Guidance for Industry

小编和大家一起学习一下,不是全文翻译,有翻译错误的地方还请谅解。
背景
自2018年以来,包括以缬沙坦为代表的沙坦类药物,还有雷尼替丁、尼扎替丁,甚至二甲双胍中均检出亚硝胺杂质。
产生亚硝胺杂质的典型反应,二级胺、三级胺或者季铵盐与亚硝酸试剂在酸性条件下反应得到亚硝胺类杂质。
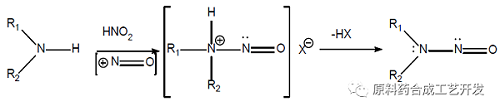
FDA已经鉴定了7种可能存在于沙坦药物中的亚硝胺杂质,结构式如下:
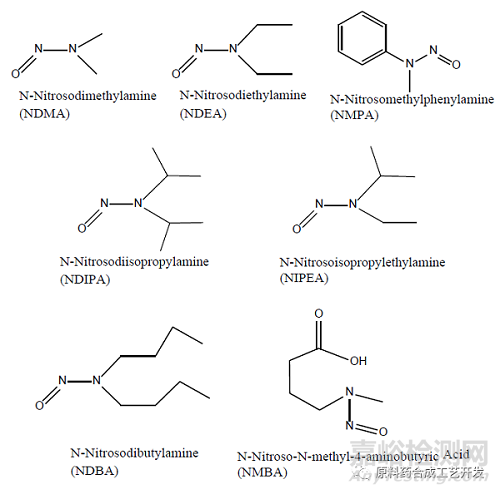
亚硝胺杂质产生根源
通常条件下,二级胺、三级胺或者季铵盐与亚硝酸试剂在酸性条件下反应得到亚硝胺类杂质。
无论在哪里引入亚硝酸类物质,都可能衍生到后续步骤里,所以一旦工艺中亚硝胺盐类物质和二级胺,三级胺,季铵盐类物质存在,就一定要评估亚硝胺类杂质。
注意:这里没有伯胺。
工艺中使用的二级胺、酰胺类溶剂分解产生的二级胺、三级胺和季铵盐中含有的二级胺杂质,均是产生亚硝胺杂质的条件。
例如:三乙胺中含有低水平的二丙胺和异丙基乙胺杂质;四丁基溴化铵中含有三丁胺和二丁胺杂质。
供应商物料污染
亚硝胺杂质可能因为新鲜的邻二甲苯、二氯甲烷或甲苯,在运输转移过程被污染产生。
叠氮钠和硝酸钾中均含有亚硝酸钠。
有些试剂和溶剂中含有二级或者三级胺。
供应商起始原料的生产设备,可能因为生产其他工艺,涉及亚硝胺杂质的交叉污染。
回收物料的污染。
淬灭试剂和络合试剂亚硝酸钠的使用。
缺乏工艺优化和控制,FDA曾注意到不同批次间反应条件相差大。
药品中除API污染源外的亚硝胺杂质
辅料中可能含有亚硝酸盐,药品制备过程和货架期贮存过程可能会产生亚硝胺杂质;一些药品可以通过降解产生亚硝胺杂质。
指南建议
FDA建议药品制造商,根据本指南中亚硝胺杂质产生的可能途径和潜在来源,评估API中和药品制备过程产生亚硝胺杂质的风险和被亚硝胺杂质污染的风险。
可接受限度
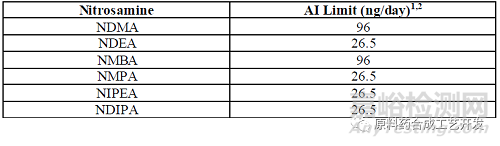
亚硝胺杂质限度ppm=AI/MDD(maximum daily dose)。上表中可接受限度是针对药品中只含有一种亚硝胺杂质。
如果一个药品中含有多个亚硝胺杂质,亚硝胺杂质总和不能超过其中一个低的杂质AI限度。
FDA指南中有一条,小编没有完全理解,原文中指出,对于最大日剂量不过880mg/day的药品, 建议多个亚硝胺杂质总量不得过0.03ppm(26.5 ng/day 除以880mg/day),对于最大日剂量高于 880 mg/day的药品,多个亚硝胺杂质总量不得过26.5ng/day。
疑问:低于880mg的药品都按照880mg计算吗?
小编理解,根据FDA指南文件,单个的亚硝胺杂质按照实际最大日剂量计算,和ICH M7一样。但是多个亚硝胺杂质时,采用更保守的策略,最大日剂量低于880mg的药品也以880mg为基础计算,不得过26.5ng/day,也就是0.03ppm,而不是96ng/day。
原料药和制剂制造商应该使用LOQ等于或者低于0.03ppm的方法,通常制造商应该把定量限和检测限做的尽可能的低,以满足最大日剂量超高880mg的药品,例如最大日剂量是1200mg,LOQ应该低于0.02ppm。
原料药和制剂制造商应该采用如下步骤,降低产品中亚硝胺杂质:
评估原料药,在售产品和在申请产品中亚硝胺杂质风险;
如果亚硝胺杂质风险存在,进行分析检验方法确认,分析方法是否可靠;
向FDA报告为防止和减少亚硝胺杂质而采取的变更。
给API制造商的建议
降低原料药中亚硝胺杂质的存在
制造商应该在合成路线设计和工艺优化期间,最大程度的防止和减少亚硝胺杂质的产生。如果不能避免,则必须采用合理控制和去除手段。
如果路线中可能产生亚硝胺,则尽量不使用二级胺、三级胺或季铵盐。注意酰胺类溶剂的使用。
采用非亚硝盐类物质淬灭分解叠氮化物。
采用合理的优化的工艺,设计去除亚硝胺杂质的工艺。
API制造商应该审核他们的供应链,评估原材料等,防止被亚硝胺杂质污染。
回收物料的谨慎使用,建立合理的质量标准,防止亚硝胺杂质污染;同时做好设备的清洁验证,避免交叉污染。
API制造商,采用的饮用水可能含有亚硝酸盐,甚至亚硝酸胺杂质,需要分析,控制,避免亚硝胺杂质超标。
原料药可以按照ICH Q7进行返工和再加工,以控制亚硝胺杂质。如有类似操作,必须在质量部门监督下进行。
亚硝胺杂质的控制
如果亚硝胺杂质件处理高于定量限,应该制定策略,采用办法,确保亚硝胺杂质在限度内。
给药品制造商的建议
药品制造商应进行风险评估,以确定药品中亚硝胺杂质存在的可能性。
风险评估应涉及与API制造商的合作,评估原料药中亚硝胺杂质。
风险评估还应对药品生产或者贮存过程中引入亚硝胺的任何途径包括降解的评估。
一旦确定有风险,必须建立合理的检验手段。
小结
先评估有没有亚硝胺存在风险,如有,采用可信的分析方法确认是否存在亚硝胺杂质,来源分析,限度制定,内容感觉有血有肉了!

来源:原料药合成工艺开发


