您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-11-24 20:45
摘要 目的:研究注射用醋酸奥曲肽微球体外释放度加速试验方法,并探讨与体内释放的相关性,为该制剂的有效性评价研究提供参考。方法:分别采用转瓶法和流池法考察了温度、pH、转速、流速、样品池的种类、膜的排列方式、玻璃珠以及加样方式等影响因素,建立了体外加速释放在温度 37 ℃、片剂池(22.6 mm)、流速 16 mL·min-1 和 pH 10.0 缓冲液中进行的流池法,并与在温度 37 ℃、转速 6 r·min-1 和 pH 10.0 缓冲液中进行的转瓶法进行对比。结果:注射用醋酸奥曲肽微球在流池法中的释放均快于转瓶法中的释放;且 2 种制剂样品不同方法测定结果趋势一致,制剂 A 释放快于制剂 B;对流池法体外加速释放 - 体内释放进行线性回归,制剂 A 和 B 相关系数 r 分别为 0.998 2、0.960 9。结论:采用流池法测定的体外加速释放快于转瓶法,且与体内释放具有良好的相关性(r>0.9),为评价奥曲肽微球制剂的体内外释放提供参考。
注射用醋酸奥曲肽微球临床主要用于治疗肢端肥大症等疾病,肌肉注射给药,给药周期为 28d[1]。该微球制剂由诺华制药原研,于 2003 年在我国获批上市,目前国内尚未有仿制制剂上市。奥曲肽微球[2]在处方和工艺上均与亮丙瑞林[3]等其他多肽微球注射剂不同,采用葡萄糖星型丙交酯和乙交酯共聚物作为生物可降解缓释辅料,采用相分离法制备微球,其质量控制与药学评价技术方法面临挑战。释放度是评价缓释微球制剂的关键质量指标,体外释放试验一般分为突释释放、加速释放和常速释放。针对注射用醋酸奥曲肽微球的体外释放度,FDA 溶出度数据库[4]推荐采用流池法、桨法等装置进行研究;文献[5]建立了常速释放转瓶测定法,试验周期为 36d,重点对突释阶段进行了研究;尚未见体外加速试验方面的研究报道。为提高注射用微球制剂质量监测与评价的效率,有必要对该制剂的体外加速释放度试验方法进行研究。
文献报道[6-12]注射用微球制剂的体外释放度方法有直接释药法、透析膜扩散法、流池法等,各有特点。采用水浴转瓶装置的直接释药法,虽然操作简便,但微球易聚集或浮动,且在进行分离时样品容易损失,对最终试验结果产生影响。流池法即美国药典溶出度测定第Ⅳ法[13],包括开环和闭环 2 种模式,将微球置于样品池中,释放介质往复通过样品池中的微球,定时取样并补充相应的释放介质。此方法因能更好的模拟人体内环境,生物相关性良好,被美国 FDA推荐作为测定 PLGA 微球释放度的最适方法[14],但其成本过高,且存在反压力和过滤器堵塞的风险。
本文通过考察温度、流速、pH、样品池、样品装填方式等条件,建立了流池法测定注射用醋酸奥曲肽微球体外加速释放度,并与转瓶法进行对比研究,同时采用 LC-MS 法测定大鼠血浆中奥曲肽的浓度,探讨分析体外加速释放和体内释放行为,为醋酸奥曲肽微球注射剂的有效性评价研究提供参考。
1 材料与方法
1.1 仪器与试药
仪器:Agilent 1260 高 效 液 相 色 谱 仪、Agilent 1290 高效液相色谱(Agilent 公司);QTRAP 5500MS/MS 系 统(Agilent 公 司);转 瓶 装 置(Rotating Bottle Apparatus,Agilent 公司);CE-7 流通池(Sotax 公司);ZKT-7F 真空脱气仪(天津市天大天发科技有限公司);Fresco 21 XIR 台 式 离 心 机(ThermoHeraeus 公司);VORTEX 多功能漩涡混合器(Scientific 公司);Turbo Vap 蒸发仪(Biotage 公司)。
试药:醋酸奥曲肽对照品(批号 140730-201303,含 量 87.6%,中 国 食 品 药 品 检 定 研 究 院);13C6-Lys Octreotide Tri(TRC 公司);注射用醋酸奥曲肽微球和溶媒样品(生产企业 A、生产企业 B);滤膜(GF/F:0.7 μm,批号 9565828,GF/D:2.7 μm,批号 9739611,Whatman 公司);滤头(2 μm;Upchurch 公司);固相萃取柱(Oasis WCX 1 cc/30 mg,30 µm,WATERS OASIS 公司)。
试 剂:甲 醇(批 号 SB6SF66072;MERCK 公 司)、甲 酸(批 号 402907,FLUKA 公 司);丙 酸(批 号SHBC7498V,FLUKA 公 司);磷 酸(≥ 85.0%)、冰醋 酸(≥ 99.5%)、三 水 乙 酸 钠(≥ 99.0%)、氯 化 钠(≥ 99.5%)、氯化铵(≥ 99.5%)均来源国药集团化学试剂有限公司;四甲基氢氧化铵五水合物(97%,北京百灵威科技有限公司);乙腈(99%,Fisher Scientific公 司);十 二 烷 基 硫 酸 钠(批 号 100809-201302, ≥95%中国食品药品检定研究院)。
1.2 体外释放度测定-转瓶法
1.2.1 试液配制
缓冲液(pH 4.0):称取 0.9 g 冰醋酸,用 250 mL 水溶解,用 5 mol·L-1 氢氧化钠溶液调节 pH 4.0。加入 5.25 g 十二烷基硫酸钠,慢慢搅拌使溶解。缓冲液(pH 7.0):称取 1.35 g 氯化铵至 250 mL 量瓶,用水溶解后用三乙胺调节 pH 为 7.0±0.1。加入 5.25 g 十二烷基硫酸钠,慢慢搅拌使溶解。缓冲液(pH 10):称取 2.7 g 氯化铵至 500 mL 量瓶,用 450 mL 水溶解,量取 6.0 mL 三乙胺加入瓶中,混匀,用水定容至刻度。用三乙胺调节 pH 为 10.0±0.1,加入10.5 g 十二烷基硫酸钠,慢慢搅拌使溶解。
供试品溶液:取适量微球,置 40 mL 转瓶中,加入 30 mL 缓冲液,拧紧瓶盖,立即将转瓶与装置连接并开始旋转。在 1、4、24 h 从装置上移除转瓶,取出500 μL,过滤,将 300 μL 滤液倒回转瓶中,将剩下的200 μL 滤液置于自动进样瓶中。
1.2.2 实 验 装 置
水 浴 转 瓶 装 置(Rotating Bottle Apparatus,Agilent 公司)
1.3 体外释放度测定——流池法
1.3.1 试液配制
缓冲液(pH 4、7、10):同“1.2”项下方法。
供试品溶液:取适量微球,置样品池中,加入 60 mL 缓冲液于瓶中。在 1、4、8、12、24、36、48 h 时取出 500 μL 等分部分,过滤,将 300 μL 滤液倒回瓶中,将剩下的 200 μL 滤液置于自动进样瓶中。
1.3.2 实验装置
采用美国药典溶出度测定第Ⅳ法 - 流池法装置[13]。
1.4 HPLC 条件
色谱柱:Brownlee NEW GUARD,RP-18,Aquapor, (7 μm,3 mm×15 mm),Brownlee Spheri-5,RP-18(5 μm,4.6 mm×100 mm);流动相:水 - 乙腈 - 四甲基氢氧化铵溶液(1 200∶600∶200);流速:1.2 mL·min-1;检测器 DAD;检测波长:210 nm;柱温:室温;进样器温度:8 ℃;进样体积:10 μL;等度洗脱。
1.5 体内释放测定
1.5.1 动物实验
供试品溶液制备:分别精密称取微球样品(生产厂 A 和 B)适量,加入溶媒 5 mL,配制成质量浓度约为 2 mg·mL-1 混悬液。
动物与给药:取 18 只雄性成年鼠,体重为 200~ 250 g,均分为 3 组,分别为 A 组、B 组、空白组,每组6 只。按给药体积为 1.0 mL·kg-1,对 A 组、B 组分别肌肉注射给药样品 A、B 混悬液,各组应在 5 min 之内完成给药,避免悬浮液中沉淀生成。
样品的采集与储存:于 0、0.25、0.5、1、2、6 h 和 1、 2、3、4、7、9、11、13、15、18、21、25、28、32、35、42、49、56 d 从 SD 大鼠的眼眶后静脉丛采血 0.5 mL,将血液加入预置 5 µL 浓度为 50 TIU·mL-1 的抑肽酶和5 µL 肝素的抗吸附 EP 管中(冰盒上),混匀。4 ℃下,12 000 r·min-1 离心 10 min,取上清液至另一抗吸附 EP 管中,-80 ℃保存待测。
1.5.2 样品前处理
精密移取大鼠空白血浆 100 µL,加稀释液(甲醇 - 水 - 甲酸(60∶40∶0.2)100 µL,内标(13C 6Octretide 20 ng·mL-1)100 µL,于 1.5 mL 离心管中,加入 4% 磷酸水溶液 100 µL,混匀;活化固相萃取柱;将样品加于固相萃取柱中后离心,先后加洗涤液,离心洗去杂质,再加入洗脱液洗脱样品,离心(1 000 r·min-1,2 min)用玻璃管收集洗脱液;洗脱液置于 50 ℃水浴,N2 吹干后,用 100 µL 稀释液溶解后进样至液相色谱质谱仪。
1.5.3 LC-MS 分 析 法
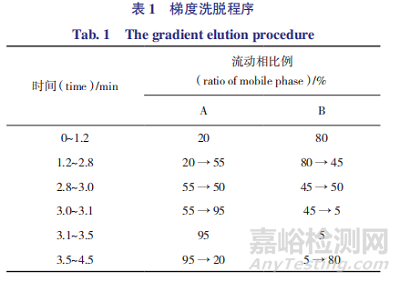
色 谱 条 件:色 谱 柱 Eclipse plus RRHD C18(50 mm×2.1 mm,1.8 μm),流动相甲醇(A)-0.02% 丙酸水溶液(B),流速 0.5 mL·min-1,柱温 45℃,进样体积 10 μL,梯度洗脱(见表 1)。
质谱条件:离子源,电喷雾离子化源,正电子方式检测;温度 500 ℃ ;气帘气体(CUR,N2)压力0.2 MPa;离子喷射电压 5 000 V;源内气体 1(GS1, N2)压 力 0.4 MPa;源 内 气 体 1(GS2,N2)压 力0.4 MPa;扫描方式,多反应监测(MRM);
奥曲肽 m/z510.4>120.1;去簇电压(DP)120 V;碰撞能量(CE),25 V;内 标 13C6Octretide m/z 513.5>120.1;去 簇 电 压(DP)100 V;碰撞能量(CE):25 V
2 结果
2.1 体外加速释放实验影响因素考察
2.1.1 转瓶实验法影响因素
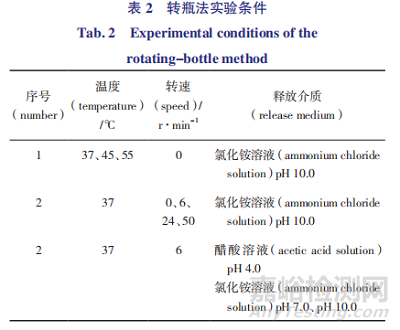
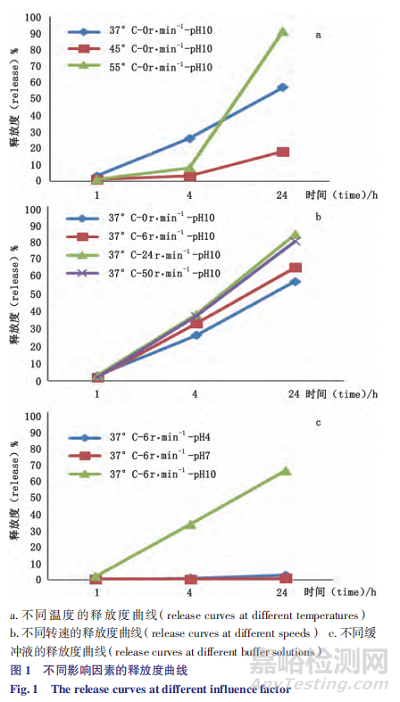
转瓶法实验按照表 2设计进行,实验因素考察结果见图 1。温度:如图 1-a所示,4 h 内微球在 45℃、55℃条件下释放较慢,推测是由于高温使聚合物 PLGA 发生形态变化,闭合了表面孔隙从而减少了药物的扩散;4 h 后在 55 ℃时条件下微球中药物释放突增,推测是由于更高的温度加快了聚合物的溶蚀作用,这与文献[6-12]报道相一致;在 37℃下释放平稳且 24 h 释放量超过 60%。综合考虑,最终选择 37℃作为体外加速释放试验的温度。
转速:由图 1-b 可见,转瓶法转速 24 r·min-1 以内,转速增加释放增多,转速超过 24 r·min-1 释放并未继续增加。
释放介质:如图 1-c 所示,pH 4.0、pH 7.0 条件下24 h 内基本不释放,pH 10 条件下 24 h 内释放量超过60%。根据酸碱催化理论[4],大量的氢离子或氢氧根离子都会诱导 PLGA 内酯键裂解,从而达到加速释放的目的。
转瓶法体外加速释放条件最后选择为温度37℃、转速 6 r·min-1、pH 10 释放介质。
2.1.2 流通池实验法影响因素
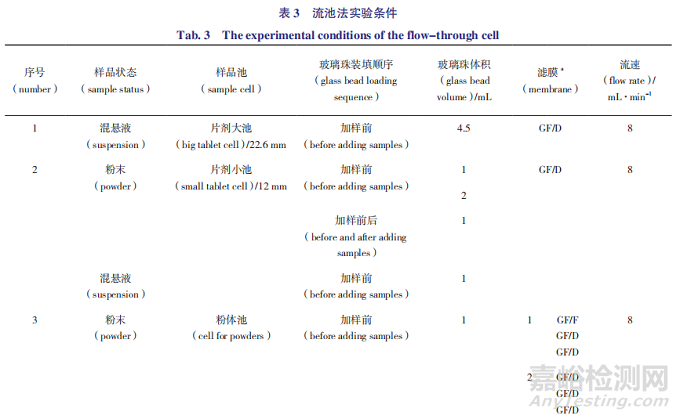
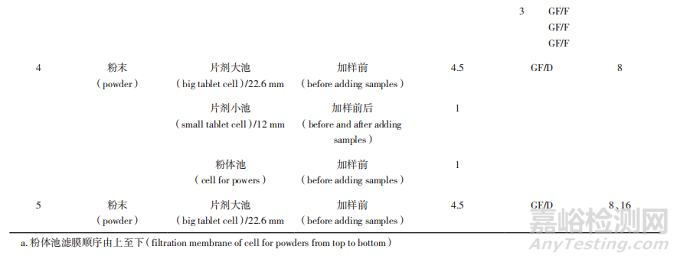
在转瓶法实验条件基础上,利用流通池对玻璃珠及样品装填方式、粉体池滤膜、样品池、样品浓度、流速等条件进行考察,实验按照表 3 设计进行。
样品量:由图 2-a 可见,含 3.10 mg·mL-1 奥曲肽的混悬液释放最快。
玻璃珠体积及样品装填方式:由图 2-b 可见,玻璃珠体积、溶媒的加入对微球释放的影响较小,加样前后均加入玻璃珠释放较快。
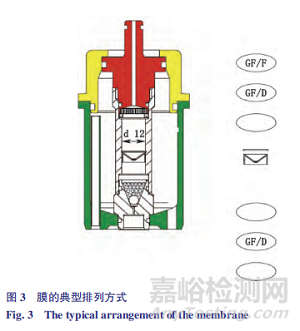
粉体池中过滤膜:膜的典型排列方式如图 3,由图 2-c 结果可见,膜的排列方式对释放的影响不大。
样 品 池:由 图 2-d 可 见,使 用 片 剂 大 池(22.6 mm)、片剂小池(12 mm)、粉体池的释放度依次递减,这可能是由于片剂小池(12 mm)和粉体池的体积较小,微球中 PLGA 溶胀后易堵住过滤器而造成的。
流速:从图 2-e 可知,流速增加释放度增大。
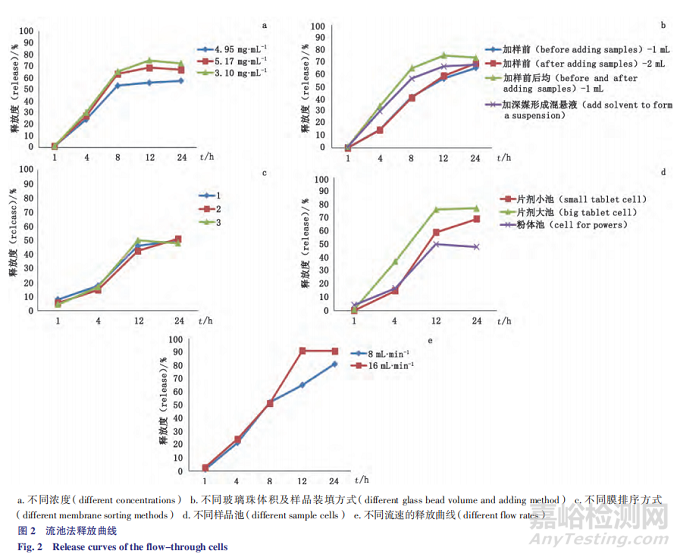
流池法最后选择的条件为温度 37 ℃、片剂大池、流速 16 mL·min-1、pH 10 释放介质。
2.2 体外加速释放度测定
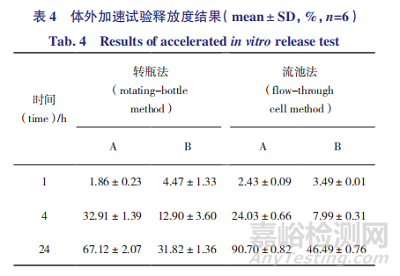
本研究通过改变温度、pH、转速 / 流速等条件加速了药物从 PLGA 微球中释放,最终建立了流池法体外加速释放测定方法,分别测定不同企业微球样品,并与转瓶法结果进行对比。由表 4 可见,2 种方法测定的体外加速释放度,4 h 后样品 A 的释放度均大于样品 B,且采用流池法测定体外释放度,样品 A 和 B的释放度均明显大于转瓶法。
2.3 体内释放测定
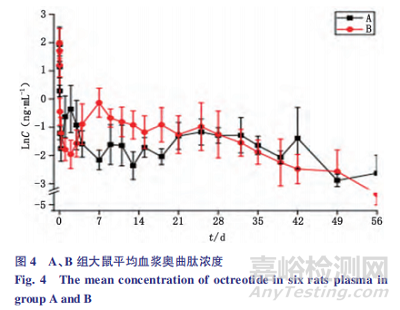
微球经皮下或肌肉注射给药后,药物从微球中释放后通过皮下或骨骼肌的结缔组织扩散,再经毛细血管吸收进入血液循环分布到靶器官发挥药效[16]。本文利用大鼠对 2 家企业的醋酸奥曲肽微球进行体内释放试验,通过 LC-MS 检测大鼠体内奥曲肽血药浓度,研究该微球制剂药物的体内释放行为。A、B 2 组大鼠血浆中奥曲肽浓度测定结果见图 4 。
3 讨论
3.1 体外加速释放测定方法
对比 2 种体外加速释放测定方法,转瓶法的操作更为简单,但需注意取样时勿粘取微球造成损失,导致释放结果偏低;流通池法需要选择合适的样品池,避免微球溶胀,池内压力过大,导致释放结果不准确。微球样品在流池法条件下的释放速率快于转瓶法,针对释放机制为扩散和溶蚀作用的微球而言,流池法更为适合作为体外加速释放的测定方法。
3.2 体内释放曲线和数学模型
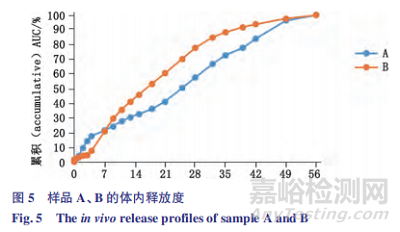
将大鼠体内释放数据与流池法体外加速释放数据利用 Origin Pro 8.0 软件进行相关性分析。根据D’Souza S 等[9]。的研究,体内释放度可以利用曲线下面积的百分数所表示,图 5 为微球样品 A、B 的体内释放曲线。
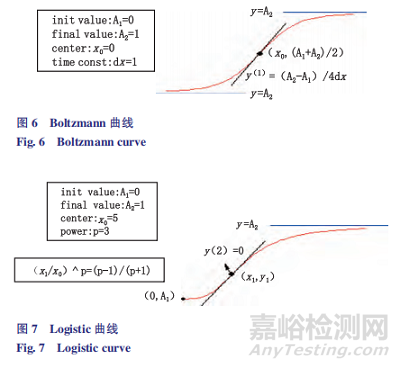
对体内释放数据利用 Origin Pro 8.0 软件中的Boltzmann、Logistic 等数学模型拟合曲线。Boltzmann 方程:y=A2+(A1-A2)(/ 1+exp(x-x0/dx))见图 6 Boltzmann曲 线;Logistic 方 程:y=A2+(A1- A2)/(1+(x/x0)p)见 图 7 Logistic 曲线。
3.3 体内外释放度分析
本文结合体内药动学研究,对体内与体外释放数据进行分析,探索体外加速释放 - 体内释放的相关性。由表 5 和图 8-10 可见,体外加速释放(流池法)线性拟合后,与将体内释放拟合曲线对应的点利用最小二乘法进行线性回归。微球样品 A、B 体外加速释放线性拟合曲线的决定系数 r2 分别为 0.987 3、0.927 5;对体外加速释放 - 体内释放进行线性回归相关性分析,样品 A、B 回归直线的相关系数 r 分别为0.998 2、0.960 9。
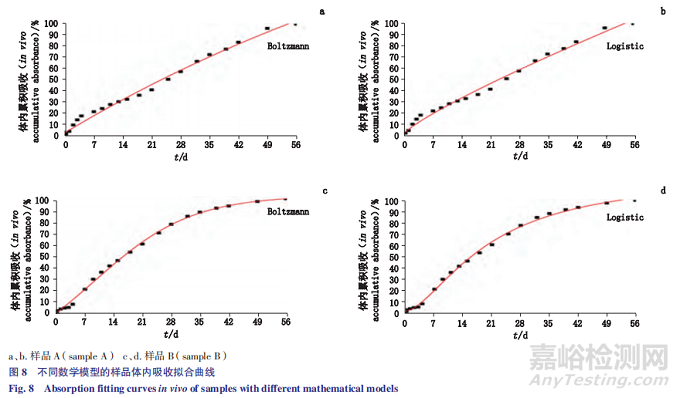
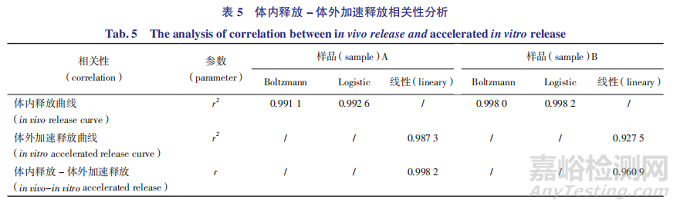
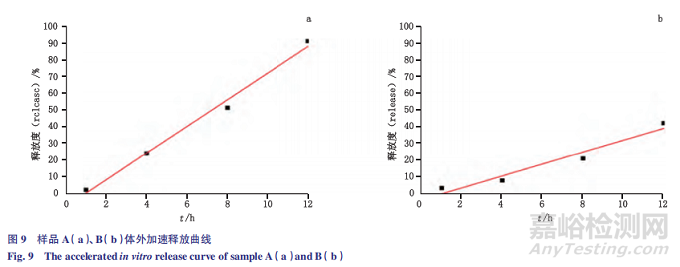
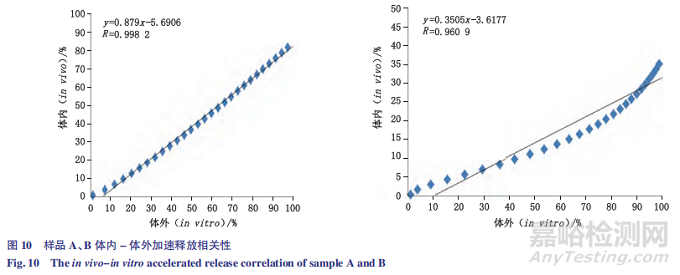
结果表明,采用流池法测定体外加速释放度,微球样品 A 和样品 B 的体外释放与体内释放均具有良好的相关性。
4 小结
本文以注射用醋酸奥曲肽微球为研究对象,进行了体外释放度测定方法研究和体内外释放相关性初步研究。通过体外加速释放试验方法研究,探索了影响奥曲肽微球释放的因素,如温度、pH、转速、流速、样品池的种类、膜的排列方式、玻璃珠以及样品装填方式等。建立了流池法测定奥曲肽微球制剂的释放度,并比较了与转瓶法的适用性。通过体内外释放相关性的探索性研究,建立了体内释放、体外加速释放的拟合曲线,结果表明体外加速释放与体内释放呈线性相关。本文建立的体外加速释放流通池测定方法对于不同微球样品有较好的区分力和良好的体内外线性相关,可用于注射液醋酸奥曲肽微球的质量控制,与 FDA 推荐的 PLGA 缓释微球体外释放分析策略一致,本研究为评价奥曲肽微球制剂的体外释放度提供了新的测定方法,为深入开展肽类缓释注射剂体内药代参数的预测研究积累了技术数据。

来源:Internet


