由于对周围环境的适应性,软性微型机器人已经发展成为医学领域的各种治疗应用,包括血管疏通、细胞运输和药物传递。然而,大多数软性微型机器人在删除外部驱动场后,无法快速进入、检索和维护其原始位置的操作。为此,中国医科大学Guannan He和中国科学院沈阳自动化研究所焦念东副研究员介绍了一种用于靶向药物输送的软磁性微型机器人,它可以通过导管运输到体内并锚定在组织上。该微型机器人有一个双层粘附体,带有一个贻贝启发的水凝胶层和一个章鱼启发的磁性结构层。根据水凝胶层在空气和水中的粘附程度的差异,在医疗导管的帮助下完成进入和回收。该微型机器人在外加磁场和在水下组织粘附的条件下,可以实现多种运动模式。利用胃模型证明了微型机器人的适应性和可回收性。结合超声(US)成像,在分离的小肠中显示生物体的操作可行性。此外,利用荧光成像系统确定了一种高效的靶向给药方法。因此,本研究所提出的软磁性微型机器人在医学上具有巨大的应用潜力。
相关研究内容以“Catheter-Assisted Bioinspired Adhesive Magnetic Soft Millirobot for Drug Delivery”为题于2023年10月25日发表在《Small》上。
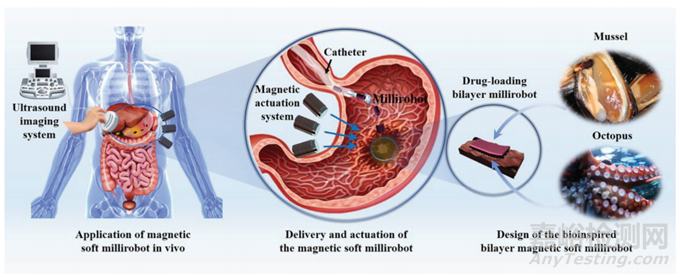
示意图 生物启发磁力微型机器人原理图及其生物医学应用
本文利用PDA水凝胶和磁性粒子掺杂的聚二甲基硅氧烷(PDMS)开发了一种软粘接剂磁性微型机器人。该微型机器人通过以一种可重构的方式拉伸自己来适应环境。如示意图所示,微型机器人通过粘附“快速通道”导管,有效地进入人体深层和狭窄的空间,脱离导管,不造成损伤。这防止了与人体复杂流体环境的直接接触,并使微型机器人能够穿过崎岖不平和复杂的器官。
图1 多层微型机器人的制造与表征
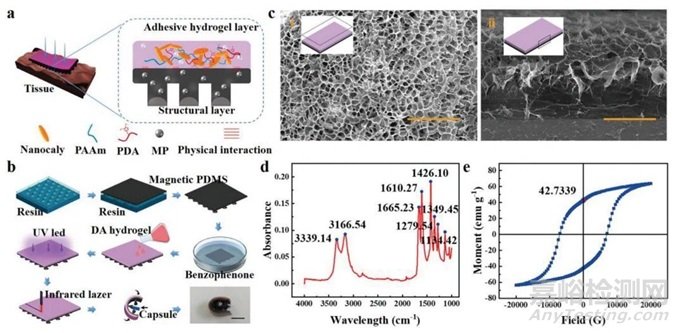
图1a显示了一个软磁性微型机器人的详细结构。多层微型机器人由磁性PDMS粘合剂层和生物粘附水凝胶层组成。利用三维打印树脂模具固化结构磁性PDMS,制作磁性吸盘阵列结构层(图1b)。扫描电镜(SEM)图像(图1ci)显示,该微型机器人的亲水水凝胶具有紧凑、均匀的多孔结构,为载药提供足够的空间,使该水凝胶具有良好的载药能力(图1c i)。侧剖面显示,亲水水凝胶与磁性PDMS界面紧密结合(图1c ii)。在1665.23cm−1处,一个与酰胺基C═O相关的显著峰表明丙烯酰胺基的存在(图1d)。接着描述了磁性PDMS层的磁化强度(图1e)。磁滞回线具有较大的剩余力和强制力,因此可以在外加磁场的作用下有效地驱动磁性微型机器人。
图2 多层微型机器人胶层的胶粘机理及性能
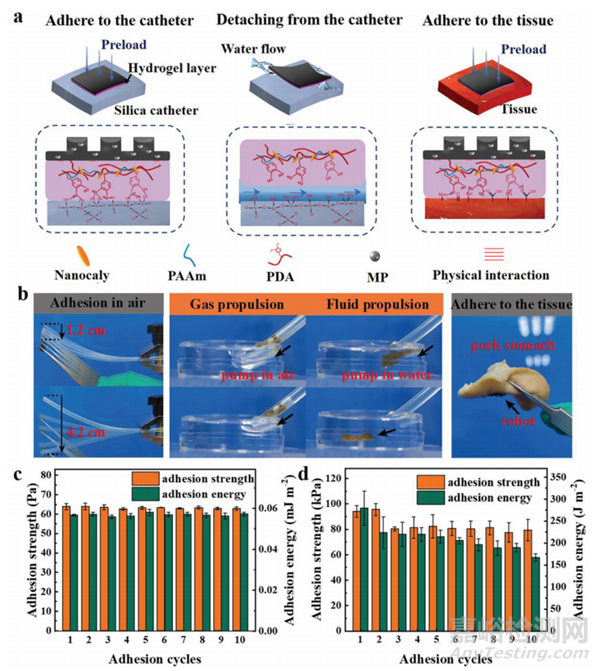
这个微型机器人可以通过向导管中注射生理盐水来释放。图2a显示双分子层微机器人的生物粘附层与导管的粘附,由电流冲刷引发的分离,以及与生物组织的粘附。图2b显示微型机器人的不同层与空气中导管的附着力,并附着在猪的胃表面。水凝胶在空气中具有较高的粘附强度和粘附能,在初始重复粘附过程中能保持较强的粘附性能(图2c)。而在水中粘附强度和能量显著下降(图2d)。本研究方法利用水凝胶在空气中的优良附着力和在水中的低附着力的区别,实现微型机器人的加载和释放。
图3 多层微型机器人磁性吸盘结构层的粘附机理及性能
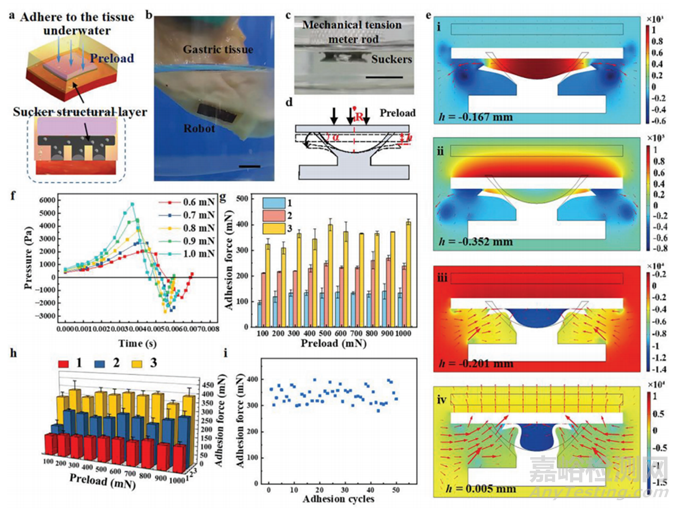
本研究利用3D打印模板设计并制作一个磁性吸盘结构层,在体液中,微型机器人的吸盘结构侧面对生物表面,在磁力的作用下实现吸附(图3a)。该微型机器人可以很好地吸附在水下组织表面,并在振动干扰下保持附着,模仿患者的日常活动(图3b)。通过控制张力机,在预加载的条件下,测量微型机器人吸盘结构层的吸附力,在杆下按压时,吸盘的变形如图3c所示。吸盘在下压杆过程中的变形如图3d所示。图3e为在600 mN预载荷下下压拉玻璃片过程中吸盘及周围流体状态的模拟结果。图3f显示不同预载荷下吸盘内部压力的变化,预负荷在0.005 s时反转。预载大于100 mN形成的玻璃衬底的吸附力相似,单个吸盘形成的平均吸附力为120mN(图3g)。水下对软生物组织的粘附得出相同结论(图3h)。接着还验证吸盘结构层表现出良好的重复性(图3i)。在重复水下粘附50次后,微型机器人的粘附力没有下降趋势。
图4 多种磁性运动模式和体外实验
图5 微型机器人的多种磁性运动模式和体外实验
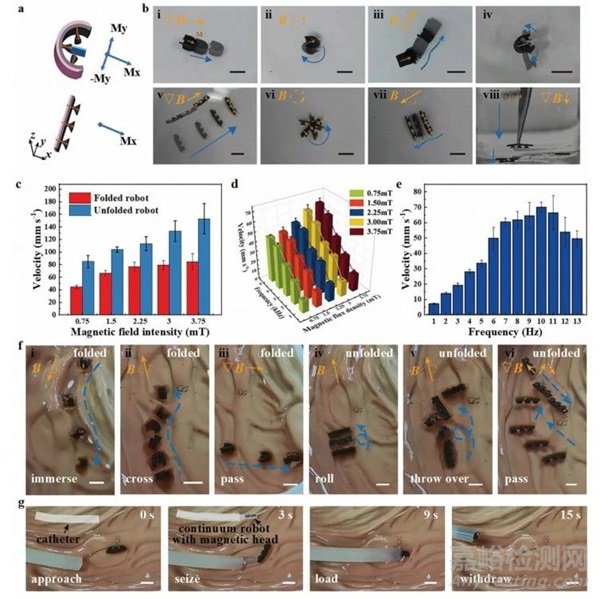
除了通过导管输送外,该微型机器人还可以被磁性引导到目标区域。由于在PDMS固化过程中施加的强外磁场的磁化,微型机器人表现出铁磁性(图4a)。在图4b中,蓝色箭头表示磁控制运动过程中的运动轨迹,黄色符号表示外部驱动磁场(梯度、旋转和翻滚磁场)。在折叠和展开状态下,微型机器人的速度随着外部磁场强度的增加而增加(图4c)。在滚动运动中,折叠状态下的微型机器人的速度随着外场强的增加而增加,并且在1-5Hz范围内随频率呈增加的趋势(图4d)。在展开状态下,在1-10hz范围内,其滚动速度也随频率呈上升趋势,而当频率为大于10 Hz时,就会出现不受控制的失步现象,导致速度下降(图4e)。处于折叠状态的微型机器人可以在潮湿的环境中滚入水中(图4f i)。微型机器人可以通过滚动运动穿过胃折叠,并以平折叠滚动(图4f ii、iv、v)。图4f iii、vi显示,微型机器人可以依靠磁力在水下快速平移。使用磁性连续体机器人的导管取出微型机器人的过程如图4g所示。
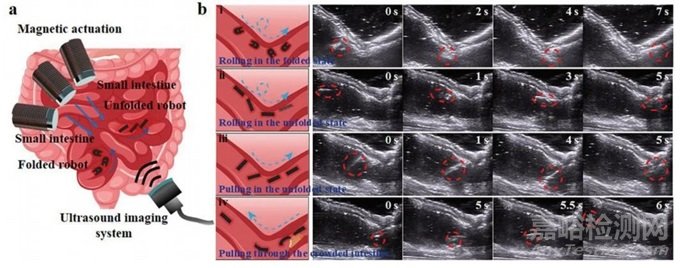
磁力微型机器人在体外证实了其在猪肠道内的生物可操作性(图5a)。该微型机器人最初被放置在猪小肠左端,图5b i显示一个折叠的微型机器人在一个滚动的磁场下沿着小肠壁滚动,穿过小肠的转折点。随着胶囊壳的膨胀,微型机器人自行折叠,但它仍然可以沿着肠壁自由地向前滚动(图5b ii)。微型机器人在磁场的作用下平移,以一定角度旋转后改变平移方向通过转弯(图5b iii)。虽然肠道被食物碎片等物体充血,但由于身体灵活而薄,微型机器人仍然可以在大磁场的作用下通过肠道(图5b iv)。结合实时临床成像设备,可以观察到微型机器人在体内的运动,这是微型机器人在体内医学应用的基本前提。
图6 该微型机器人的体外实验及高效的靶向药物释放应用
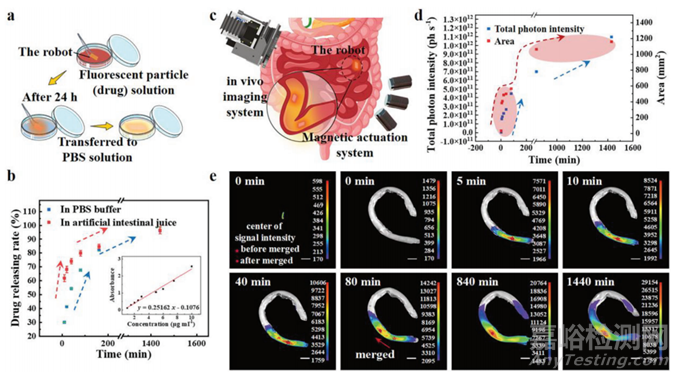
使用罗丹明荧光纳米珠作为标记物来可视化药物扩散的状态(图6a)。使用紫外-可见近红外分光光度计校准药物浓度和吸光度之间的关系,并测量释放药物的浓度(图6b)。使用体内成像系统获得荧光图像和亮场照片(图6c)。荧光粒子的总光子强度和可检测扩散面积如图6d所示。图6e显示,可以检测到装入微型机器人药物的荧光信号。因此,微型机器人与临床成像设备结合,在体内医疗应用方面具有相当大的潜力。
综上所述,本研究提出了一种新的微型机器人设计,以靶向、长期的药物释放在体内。将粘合剂材料和结构的优点应用到机器人技术领域,解决了在临床实践中应用医学微型机器人时不可忽视的关键问题。在这项研究中设计了一个软磁性机器人,它可以通过导管输送到人体,并被操纵锚定到组织的目标区域,用于医疗应用。该机器人由贻贝启发的水凝胶层和磁性吸盘结构层组成,因此它具有不同粘附机制的双层粘附表面。本研究利用该粘合剂水凝胶在空气和水下的可变粘附强度,使微型机器人能够通过导管实现快速、无损伤的输送。空气中强大的粘附防止输送过程中分离,而水中较弱的粘附强度确保控制、无损的释放。磁吸盘结构层使机器人能够在外部磁场下以各种运动模式进行内部导航,机器人在负压展开后也能粘附在组织表面。本研究模拟了猪肠道内的生物环境,并利用US成像证明机器人内部操作的可行性。此外,结合体内成像系统验证了该微型机器人在体内的靶向性和药物释放能力。为了设计更多治疗场景的机器人,可生物降解材料无疑是首选。未来对机器人结构和材料的改进可以实现更有效的运动模式和增强的降解性。
文章来源:https://doi.org/10.1002/smll.202306510