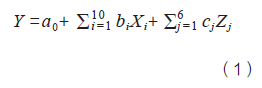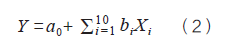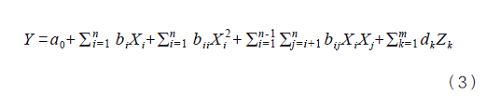摘 要 / Abstract
目的:针对中药制药过程参数控制中存在的共性关键问题,提出一种中药制药过程质量控制方法。方法:以三七总皂苷生产制造为例,在简述物料传递流程基础上,对原料药材属性参数、产品质量标准以及生产流程各单元工艺环节物料属性参数进行检测,辨识关键物料质控参数及其合理限度;设计预置过程参数并用10批次以上原料考察制药过程,根据实验结果辨识出关键过程参数,进而择优确定关键过程参数的取值范围。结果与结论:工业生产实践表明,上述方法能确保三七总皂苷产品质量,并适宜推广应用。
Objective: A quality control method for the manufacturing process of traditional Chinese medicine is proposed for tackling the common key problems in the control of manufacturing parameters. Methods: A case study was done on the manufacturing of Notoginseng Total Saponins(NTS). Based on the brief description of the material transfer steps, tests were taken in terms of the indices of medicinal materials, the quality standards of finished products, and material property parameters of each unit during the production process, so as to identify the key material quality control parameters and their reasonable ranges. Process parameters were preset and the pharmaceutical process was investigated with more than 10batches of medicinal materials. Critical process parameters(CPPs) were identified according to the experimental results. Then the ranges of CPPs were optimized. Results and Conclusion: The industrial practice verifies that the proposed method can ensure the product quality of NTS and the proposed method is suitable for popularization and application.
中成药化学组成十分复杂,其质量检验不仅技术难度大,而且检测成本很高[1]。中药制药过程质量控制对于确保中药安全性、有效性及质量一致性具有重要的现实意义[2]。尽管《中国药典》在“制法”项中规定了单元工艺先后顺序以及必要的工艺参数取值等,但仍然不够缜密,需进一步完善。放眼国际,美国等发达国家的药品监管部门均倡导在深入研究并认知制药过程规律的基础上,加强制药过程质量控制[3]。
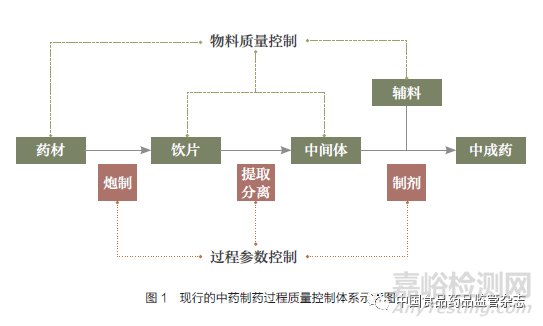
先进的制药过程质量控制系统能够适时检测关键物料质量参数和过程状态参数,及时调整关键过程参数,保障所产药品质量与原定的药品质量概貌一致,从而“免检”实时放行药品[3]。因此,科学构建中药制药过程质量控制体系是解决中药工业领域当今“最紧急、最紧迫”问题的关键技术路径。现行的中药制药过程质量控制体系如图1所示,一般包括物料质量控制及过程参数控制。
中药生产物料包括药材、饮片、辅料和中间体等,《中国药典》一部规定了药材、饮片和部分提取物的质量标准,而四部规定了辅料的质量标准。由于在中药生产制造中涉及相当多的过程参数,且往往存在关键过程参数不明确、与产品质量相关参数的优选值不清楚等情况,会出现符合法定标准的药材及物料难以生产出质量可靠的中药产品等问题。此外,中药生产制造一般通过检测单个物理量(如温度、压力、密度、pH值等)判断制药过程状态,造成产品质量风险难以防控,但若要检测更多化学或生物活性指标,就存在设备价格高、分析结果不直观等问题。
本文以三七总皂苷生产制造为例,提出一种中药制药过程质量控制方法,其技术步骤为:①研究量值传递规律,在此基础上完善药材的质量检测指标,解决药材应该“测什么”的问题。②根据制药过程参数对物料量值传递的影响,设置药材质检指标的内控标准,解决药材“怎么控”的问题。③联合考察多个单元工艺并考虑原料批次间质量变化情况,筛选关键过程参数,解决生产过程“控什么”的问题。④考虑原料批次间质量变化情形,提出过程参数的优值范围,解决过程参数“如何控”的问题。
1、三七总皂苷制药过程质量控制方法研究
1.1 根据量值传递规律设定原料内控指标
量值传递一般是指中药生产规程中物料平衡的递次量传以及关键物料质控参数的量测值在制药全流程各环节的逐级传递。这里可以采用单位质量药材为基准的指标性成分含量、大类成分含量以及总固体的产量等指标定量表征相关物质在中药生产规程中的传递。
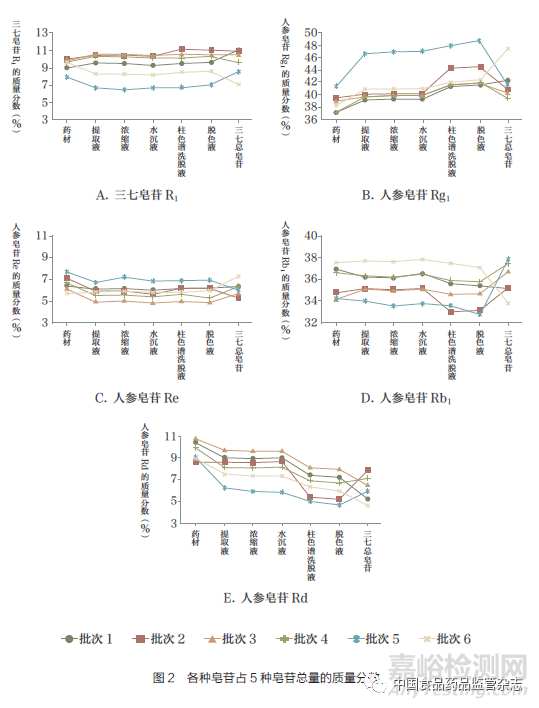
根据国家药典委员会相关规定,三七总皂苷是采用三七药材,经过粉碎、醇提、水沉、柱色谱、脱色、精制、浓缩和干燥等一系列单元工艺制得。笔者曾考察了不同批次三七生产三七总皂苷过程中的量值传递情况[4]。分别检测了6批次三七药材、提取液、浓缩液、水沉液、柱色谱洗脱液、脱色液以及三七总皂苷产品中三七皂苷R1、人参皂苷Rg1、人参皂苷Re、人参皂苷Rb1和人参皂苷Rd 5种皂苷含量。计算了各个物料中每种皂苷在这5种皂苷总量中的质量分数,具体结果如图2所示。
从图2中可知,在提取过程中人参皂苷Rg1的质量分数略有增加,而人参皂苷Rd的质量分数略有下降,但改变量大多在3%以下。提取后的各单元工艺处理后,除人参皂苷Rd的质量分数稍有下降外,其他皂苷的质量分数总体变化不大。这意味着,最终所得三七总皂苷确实主要是从药材提取分离“传递”而来,而非化学反应“转化”而来。那么,作为原料的三七质控指标应该考虑控制上述5种皂苷的含量。
《中国药典》2020年版规定三七药材中含人参皂苷Rg1、人参皂苷Rb1、三七皂苷R1的总量不得少于5.0%,没有规定人参皂苷Re和人参皂苷Rd的含量要求。根据量值传递研究结果,人参皂苷Re和人参皂苷Rd主要是从药材中提取分离而来。因此,如果是作为工业生产三七总皂苷的原料,三七药材内控标准中应考虑将人参皂苷Re和人参皂苷Rd含量作为质量参数,每批进行检测。
《中国药典》2020年版规定了三七总皂苷中5种皂苷的含量下限,实际上对原料药材中这些皂苷的含量提出了要求。例如,5种皂苷中含量最低的是人参皂苷Re,假设三七药材中人参皂苷Re含量为0.1%,并且提取分离过程中人参皂苷Re无损失(转移率为100%),为了达到三七总皂苷中2.5%人参皂苷Re的最低标准,那么5种皂苷的总得率只能是低于4.0%。这意味着合格三七药材中很多皂苷都未能充分利用。因此,如果希望5种皂苷的总得率不低于8.0%,那么三七药材中人参皂苷Re含量就不宜低于0.2%。类似地,人参皂苷Rd、三七皂苷R1、人参皂苷Rg1和人参皂苷Rb1的含量分别不宜低于0.4%、0.4%、2.0%和2.4%。
若考虑提取分离过程中5种皂苷存在一定损失,那么采购三七药材时上述5种皂苷的含量下限还需要进一步提高。比如,PAN等[5]的研究结果显示,人参皂苷Re、人参皂苷Rd、三七皂苷R1、人参皂苷Rg1和人参皂苷Rb1从药材传递到三七总皂苷的转移率约为82.3%、69.9%、79.0%、80.7%和77.8%。以上述转移率进行估算,药材中人参皂苷Re、人参皂苷Rd、三七皂苷R1、人参皂苷Rg1和人参皂苷Rb1的含量下限分别为0.243%、0.572%、0.506%、2.48%、3.08%。
从上面的分析可以看到,工业生产中所用三七的内控标准会比药典标准更高,不仅需要检测更多皂苷成分,且对各皂苷含量下限有要求。目前已有文献报道了三七药材中5种皂苷含量的液相色谱检测方法[6-7],可参考这些方法进行检测。检测后可以考虑进一步采用混批调配的方法降低原料质量波动。
1.2 辨析关键过程参数
中药制药过程参数的类型较多,通常包括工艺参数、物料属性参数、状态参数、设备参数和环境参数等[8]。其中,工艺参数通常是指在国家药品标准的制法项或工艺规程中规定的参数(比如,工艺规程中调p H值的目标范围就是工艺参数);物料属性参数是用来表征中药生产原辅料或中间体特性的参数,包括物理、化学或生物特性参数,影响药品质量的物料属性参数称为物料质量参数;质控参数是指用于确保药品质量而进行控制的过程参数;状态参数是反映制药过程状态的参数,其可能不用数字变量而用语言变量(比如,用“未沸腾”或“沸腾”描述中药煎煮过程状态,又如,用“未达终点”或“达终点”描述渗漉提取过程状态);设备参数通常指制药相关设备的参数(比如,计量泵的电机转速);表征制药流程所处环境的参数一般称为环境参数,常见的有环境温度、湿度、压力、洁净度等。
目前,对已上市中成药可根据生产数据、检验数据和文献报道等,采用风险评估等可行方法直接确定关键过程参数。常用的风险评估方法包括风险排序及过滤、失效模式及效应分析、故障树分析等。如果有实验研究数据或者工业生产数据,可采用适当统计学方法确定关键过程参数,如多元线性回归法[9]、逐步回归法[9]、标准偏回归系数法[9]、加权决定系数法[10]等。
笔者曾采用确定性筛选设计(definitive screening design)安排了32个实验用于研究提取、浓缩、水沉和柱色谱4个步骤中的10个参数,并且在实验中随机搭配了16个不同批次的三七药材[5]。测定了每种药材中以特定提取条件提取的5种皂苷量和总固体量作为药材属性参数。得到柱色谱洗脱液后,测定了5种皂苷的纯度、总固体产量、总皂苷产量作为过程评价指标(Y)。以逐步回归法精简公式(1)获得关键过程参数为提取所用乙醇浓度、洗脱液乙醇浓度、洗脱时间。
式中,X为实验中考察的过程参数,Z为药材属性参数,a0为拟合所得常数项,bi和cj均为拟合所得偏回归系数。
上述工作与多数参数筛选工作的区别点在于:筛选关键过程参数时考虑了药材属性参数的变化,获得关键过程参数时也确定了药材质量参数。此外,还对比了不考虑药材属性参数变化的情况,即采用逐步回归法精简公式(2)获得关键过程参数。
对比结果见表1。从中可知:考虑三七属性参数变化筛选所得关键过程参数与不考虑时不同。考虑三七属性参数所得模型的决定系数数值更高,说明部分三七属性参数确实对过程评价指标有影响。因为工业生产中三七药材批次间质量差异总是存在,考虑三七属性参数变化所得关键过程参数应该更为可靠。
1.3 确定参数操作范围
ICH Q8《药物开发》(Pharmaceutical Development)要求构建设计空间(design space)以保障制药过程质量。构建设计空间的本质是优化制药过程参数到合适的范围,而非一个操作点,以便为生产提供更大灵活性,减少不必要的监管。制药过程中过程参数数量很多,优化其中关键过程参数的操作范围是构建设计空间最核心的内容。
设计空间的概念中提示优化过程参数取值范围时应将物料质量参数考虑在内。因此笔者采用公式(3)建立了关键过程参数和工艺评价指标之间的定量模型[5]。
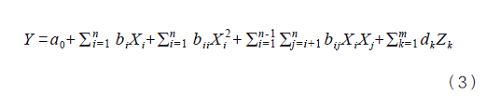
式中,Z为物料质量参数,n为除物料质量参数以外的关键过程参数个数,m为物料质量参数个数,i、j、k用于区别不同的偏回归系数。建立数学模型后计算获得设计空间。设计空间以列表的形式给出。验证后发现模型预测结果准确,设计空间范围可靠。
除关键过程参数外,其他过程参数也应有操作范围。选择其他参数具体运行值时,应考虑节能、降耗、增效等原则。例如,在确保树脂充分吸附三七皂苷的前提下,可以适当增加上样速度以提高生产效率;在确保洗涤除去杂质的前提下,洗涤水用量应尽量少些;在确保树脂再生效果的前提下,酸碱液洗涤的用量应尽量少些。
2、研究结果与讨论
2.1 基于量值传递规律判断关键工艺
确定制药过程关键工艺环节的意义在于明确实施制药过程质量控制的重点,缩小关键过程参数的搜索范围。根据量值传递研究结果可以确定关键单元工艺。
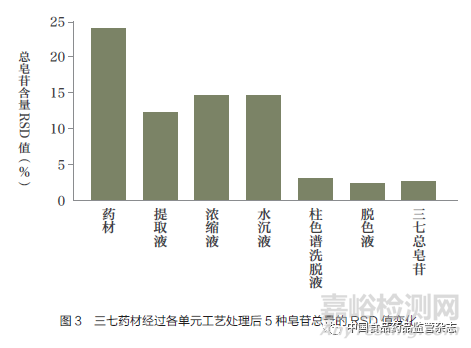
笔者测定了各单元工艺处理后6批次三七5种皂苷总量的相对标准偏差(RSD)[4],如图3所示。该数值体现了三七5种皂苷总量在生产过程中精密度的变化,体现了各单元工艺对提升三七总皂苷批次间一致性的贡献大小。从图3可知,药材中5种皂苷总量相差较大,RSD超过20%。经过提取工艺后,RSD下降到15%以下。经过柱色谱工艺后,RSD更是下降到5%以下。这说明当处理多批次三七时,柱色谱工艺对提升产品质量一致性贡献最大,是影响其精密制造的关键工艺,提取工艺的贡献次之。
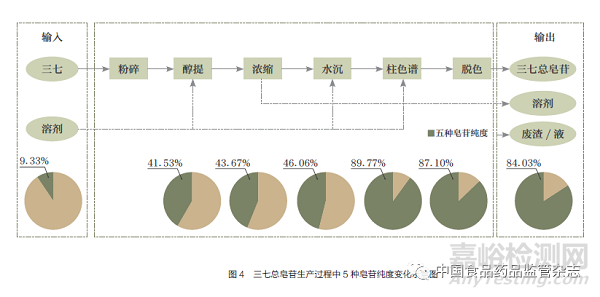
研究中也发现提取工艺和柱色谱工艺都较大程度地改变了体系中化学成分组成,具体体现为5种皂苷占总固体的质量分数大幅上升,即纯度明显提高。提取后5种皂苷纯度从不足10%提升到约40%,柱色谱后纯度从不足50%提升到超过80%,如图4所示。柱色谱工艺后所得药液的抗凝血酶活性也有较大变化。因此,柱色谱工艺是三七总皂苷生产的首要关键单元工艺,提取工艺是次要关键单元工艺。
2.2 关键过程参数辨析策略的选择
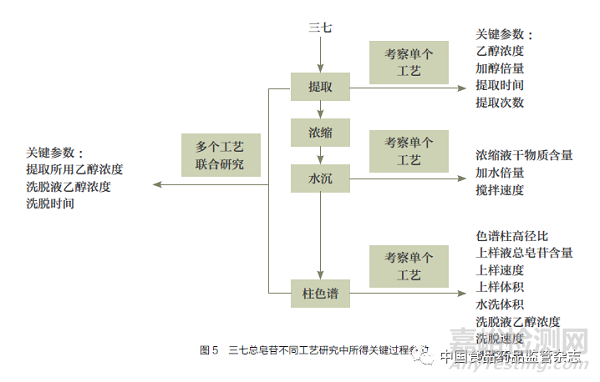
目前多数研究都是针对某个具体单元工艺,实验研究后辨析关键过程参数。需要注意的是,逐个考察单元工艺所得关键过程参数数量往往会多于联合考察多个单元工艺。图5列出了这2种研究策略所得参数的差别。
逐个研究提取、水沉和柱色谱工艺时共找到关键过程参数15个。但联合研究提取、浓缩、水沉、柱色谱4个单元工艺时,关键过程参数只有提取所用乙醇浓度、洗脱液乙醇浓度、洗脱时间3个。所得关键过程参数均集中于提取和柱色谱工艺,也证实2.1节基于量值传递研究所得关键工艺是准确的。因此,联合研究多个单元工艺不仅效率较高,且能从更接近全局的视角中获得制药过程真正的关键过程参数。联合研究多个单元工艺需要同时考察较多过程参数,建议采用足够分辨率的筛选试验设计以减少实验次数。
2.3 实验设计方法的选择
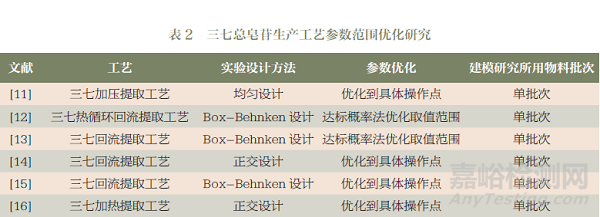
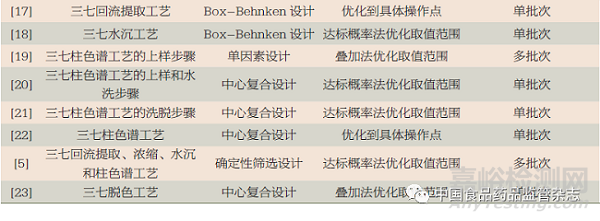
表2中列出了三七总皂苷生产工艺相关文献报道中的实验设计方法。实验设计方法包括:中心复合设计、Box-Behnken设计、确定性筛选设计、单因素设计、正交设计和均匀设计。实验设计方法的选择和待研究参数个数及后续建模方法有关。若考虑采用二阶多项式建模,用前3个实验设计方法较好。当所研究的参数超过5个时,中心复合设计和Box-Behnken设计的实验次数都较多,建议采用确定性筛选设计。
2.4 优化方式的选择
表2中列出了三七总皂苷生产工艺研究中的参数优化工作。虽然很多研究者将参数优化到最优点,但将参数优化到特定范围会更有利于提升制药过程的稳健性。目前不少研究工作在优化时都计算了达标概率,以达标概率定量表示在优化范围内运行参数时制药过程质量能得到的保障。达标概率计算时可以考虑过程参数、实验结果或模型预测结果的不确定度,所得参数优化范围会更为可靠。MODDE或Matlab等软件均可用于计算获得基于达标概率的较优参数范围。
另一种参数优化思路是前馈控制,即根据三七药材质量参数变化针对性地调整参数。应用该思路调整参数要注意合规。JIANG等[24]用Yoon-Nelson模型关联了三七水沉后上样液中皂苷浓度、上样液流速和柱色谱穿透曲线,能根据每次柱色谱上样液中皂苷含量高低灵活调整柱色谱上样时间。王晓宇等[25]建立了三七药材近红外光谱主成分、提取过程参数及指标成分提取量的定量模型,通过扫描药材快速获得光谱信息,然后针对性地调整提取过程参数,可以减少三七质量差异造成的提取液质量波动。
采用适当的制药过程检测技术确定状态参数,然后针对性地调整后续过程参数则是反馈控制的思路。JIANG等[26]将在线近红外光谱和紫外光谱所得数据相融合,建立了三七柱色谱上样流出液中三七皂苷浓度的定量模型,可用于实时监测流出液皂苷浓度;若观察到流出液皂苷浓度过高,则考虑停止上样。蒋程[27]采集三七柱色谱过程在线紫外光谱数据,以多变量统计过程控制的方法评价过程批次一致性,能检测出药液中皂苷浓度和流速的异常;进一步可根据异常情况确定处理方案。
2.5 中间体和其他物料的内控标准设定
中药生产中往往会有多个中间体,针对关键中间体设置内控标准有利于保障后续制药过程质量和药品质量。设置关键中间体内控标准的原则:放行符合内控标准的中间体后,后续加工应能得到合格药品。
确定关键中间体时需要考虑上游的控制情况,取样是否方便、检测工作量大小等。比如,三七饮片由药材粉碎制得,如果药材已按照1.1节中5种皂苷含量内控标准进行了放行控制,那么饮片可不作为关键物料。三七提取液在工业生产中往往存放于多个储罐,各储罐中提取液浓度不同,取样检测工作量大,不适合作为关键物料。三七提取液浓缩所得的浓缩液通常放置在同一储罐中,体系均匀性好,取样和检测都较方便,更适合作为关键中间体。确定关键中间体的质量参数及其范围可以采用类似于1.1节的方法。也可以先建立中间体质量参数和后续制药过程评价指标之间的定量模型,再根据评价指标的要求反算出中间体质量参数的控制标准。类似思路已用于设置丹参水提液[28]、黄芪浓缩液[29]等中间体质量标准。
除了原料药材和关键中间体,其他物料也需要有其内控标准。例如,三七柱色谱工艺中使用的树脂,应保证每次使用前都洗净上个生产周期中吸附的成分。又如,采用三七醇提液或者柱色谱洗脱液的回收乙醇用于下一批生产,应保证不产生批次间交叉污染。因此,这些物料也需要有合适的内控标准判断其品质是否合格。
2.6 制药过程设备和设施管理的重要性
制药设备性能与运行状态对药品质量及生产效率均有较大影响,因此需要科学管理中成药生产制造所涉及的设备和设施。国际制药工程协会(International Society for Pharmaceutical Engineering,ISPE)发布了《良好工程管理规范》(Good Engineering Practice,GEP),其中一项重要的内容是“操作与维护”,其目标是将设备和设施维持在较优状态。
生产中除了采集物料和参数数据,还应采集设备相关数据,以反映设备当前运行状态。建议对关键单元工艺对应的设备增加故障预警预报模块,定期检测其运行状态,并实施科学干预,确保设备长期稳定工作,促使生产处于受控状态。
2.7 制药过程质量控制持续改进的重要性
在整个药品生命周期内,都应不断积累中药产品和制药过程的知识,采用风险管理方法,持续完善中成药质量标准和提升过程质量控制水平。具体的,如果获得三七总皂苷制剂的临床数据,建议结合制剂质检数据和临床反馈信息等进行回顾分析,根据分析结果调整三七总皂苷的质量参数及其控制要求。在此基础上,重新分析确定关键过程参数及其控制范围、关键物料及其质量参数控制范围。如果采集了工业大数据,可以进一步采用合适方法,依靠数据驱动预判产品质量风险,提升整体管理水平。
3、结 论
本文针对当前中药制药过程质量控制技术方面的难点问题,以三七总皂苷生产为例,提出了一种中药制药过程质量控制方法并用于工业生产,可有效提高三七总皂苷产品合格率。