您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-08-12 22:07
中药材灭菌如何在降低微生物限度的同时确保中药材疗效并选用适宜的灭菌方法?本文探索研究了一种中药材灭菌的新技术,对高温瞬时灭菌新设备进行了智能化设计,对其高温瞬时灭菌效果进行了性能确认。试验结果证明该技术能在保留中药黄芩有效成分的同时有效除去药材中的微生物,为中药材灭菌提供了一种新手段。
制造业是国民经济的主体。如今,工业4.0智能化时代、“互联网+”时代即将到来,“互联网+制造业”将成为全球制造业发展的新趋势。《中国制造2025》提出要加快推动新一代信息技术与制造技术融合发展[1-4],《药品生产质量管理规范(2010年修订)》及其附录“计算机化系统”、《药品数据管理规范(征求意见稿)》《药品记录与数据管理要求(试行)》《中华人民共和国电子签名法》等制药行业法规及标准也均对智能制造与权限管理提出了明确要求[5-10]。根据以上法规要求,本文采用西门子博途v15.1自动化编程软件对中药材高温瞬时灭菌设备进行了智能化的设计建造,为论证其智能化设计各项控制功能的有效性,考察其灭菌效果,对中药材高温瞬时灭菌新设备进行了性能确认。
Part1高温瞬时灭菌智能化设计
1灭菌新方法概述
本次试验采用的高温瞬时灭菌新设备经中国中药协会中药新技术专业委员会认定为中药新技术产品、江苏省重点推广应用新技术新产品,拥有瞬时对药品、食品粉末进行灭菌的系统等8项发明专利和一体框架隔离式管道流通粉末灭菌系统等11项实用新型专利[11-12]。其工作原理为:中药材按照定量给料系统设定的进料速度、搅拌旋转速度,在蒸汽桨中进行旋转,同时灭菌介质纯净过热蒸汽被送入灭菌系统,搅拌桨带动物料旋转,使物料悬浮于高速流动的过热蒸汽中,从而达到杀死微生物、实现高温瞬时灭菌的目的。在该灭菌过程中,物料受热均匀;在灭菌后,汽料分离冷却系统会将物料分离并进行急骤冷却,保证物料成分不受破坏;最后,物料会经出料阀控制送至无菌储料罐,高温瞬时灭菌工艺流程如图1所示。该高温瞬间灭菌的温度为135℃~210℃,灭菌时间为2~20 s,具有生产效率高,杀菌效果好,可连续生产,灭菌后的中药材无结块呈粉状,无需进行二次烘干、粉碎等优点[13],可更好地保留有效成分。而且配备的计算机系统具有数据存储、实时打印等功能,可保证灭菌数据的完整性和可追溯性。另外,也配置了CIP(原位清洗)/SIP(原位消毒)、臭氧消毒(浓度≥1000 ppm)功能,可彻底防止多产品共线可能引起的污染、交叉污染等质量风险[14]。
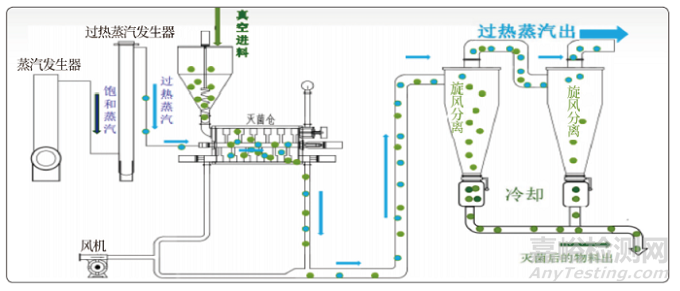
图1 高温瞬时灭菌工艺流程图
2智能化设计与计算机化系统权限分级设计
本试验运用信息技术与制造技术,采用西门子博途v15.1自动化编程软件对高温瞬时灭菌新设备进行了智能化设计,计算机化系统采用三级权限设计(Ⅲ级为操作员OP、Ⅱ级为工艺员User、Ⅰ级为管理员Admin),可使高温瞬时灭菌升温、进料、灭菌、气粉分离冷却等灭菌过程达到生产操作程序化、参数执行标准化、产品质量均一化的设计目标。
3计算机化系统三级权限
管理员Ⅰ级权限
输入用户名(Admin)及登录密码,即可进入管理员操作界面,在这里可进行人员、账户的分配设置,权限的修改、变更、禁用和删除,设置用户名和登录密码等操作,进行计算机化系统的系统时间锁定、解除、校准设置以及系统软件数据的恢复、备份和重新安装等权限管理。
工艺员Ⅱ级权限
输入用户名(User)及登录密码,即可进入工艺员操作界面,在这里可进行定量进料速度、搅拌旋转速度、蒸汽压力、灭菌压力、灭菌温度、灭菌时间、物料出口温度等关键工艺参数的设置,进行系统输入信息的复核以及系统软件数据的备份、修改、删除、历史数据的查阅等权限管理。
操作员Ⅲ级权限
输入用户名(OP)及登录密码,即可进入操作员操作界面,在这里可以通过计算机化系统监控生产运行,可进行计算机化系统的具体操作,高温瞬时灭菌生产运行状态如图2所示。
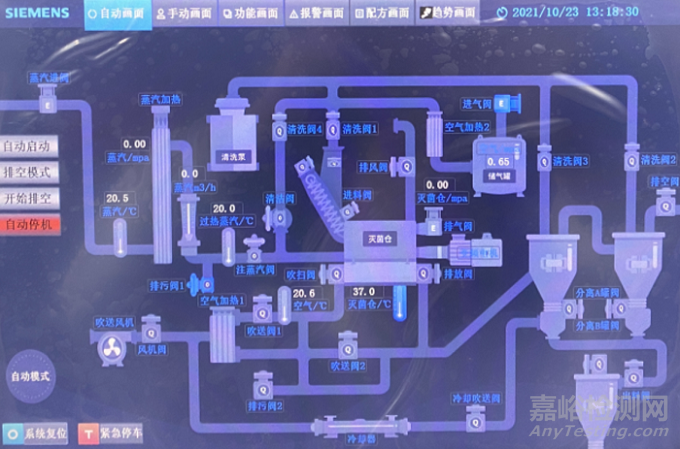
图2 高温瞬时灭菌生产运行状态
Part2灭菌效果性能确认
1性能确认方法
每次取中药黄芩粉10 kg,工艺员设定定量进料速度为50 kg/h、灭菌温度为160℃,灭菌时间为8 s,物料出口温度为30℃;管理员对设定参数、运行参数的一致性进行复核;操作员进行设备进料、灭菌生产过程监控、出料等具体操作。对中药黄芩粉进行连续3次的高温瞬时灭菌,通过对灭菌前与灭菌后的需氧菌、霉菌等微生物限度,水分、总灰分、浸出物等参数进行比较,并进行薄层鉴别,确认高温瞬时灭菌设备自动化控制功能的有效性,确认中药黄芩粉高温瞬时灭菌设备的灭菌效果。
2微生物、水分、总灰分、浸出物检查
检查方法
按《中华人民共和国药典(2020年版)》对中药黄芩粉高温瞬时灭菌前、灭菌后微生物、水分、总灰分、浸出物进行对比检查。
2.2.2合格标准
微生物限度:需氧菌总数<1000 CFU/g;霉菌和酵母菌总数<100 CFU/g;水分:不得超过12.0%;总灰分:不得超过6.0%;浸出物:不得少于40.0%。
检查结果
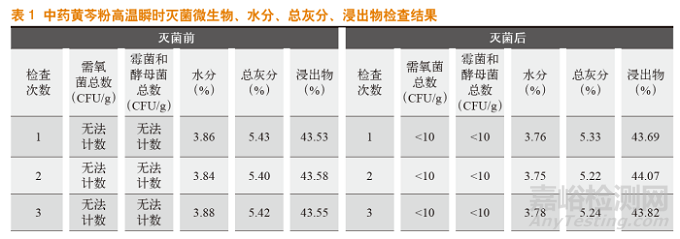
微生物、水分、总灰分、浸出物检查结果详见表1。
结果分析
通过表1的数据可以得出:需氧菌总数、霉菌和酵母菌总数在灭菌前均无法计数,灭菌后均小于10 CFU/g;灭菌前药材所含水分高于灭菌后,说明高温瞬时灭菌不会增加物料水分;总灰分的数值在灭菌前、灭菌后无变化;浸出物在灭菌前、灭菌后无变化;各项检查均符合标准要求,且检查数据重现性良好。
3薄层鉴别检查
检查方法
按《中华人民共和国药典(2020年版)》对中药黄芩粉进行高温瞬时灭菌前与灭菌后的薄层鉴别对比检查。
合格标准
薄层鉴别:供试品色谱中,在与对照药材色谱相应的位置上,显相同颜色的斑点;在与对照品色谱相应的位置上,显三个相同的暗色斑点。
检查结果
高温瞬时灭菌前薄层鉴别结果如图3所示,高温瞬时灭菌后薄层鉴别结果如图4所示。
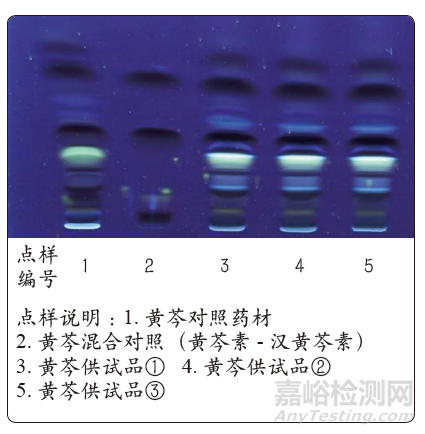
图3 中药黄芩粉高温瞬时灭菌前薄层鉴别色谱
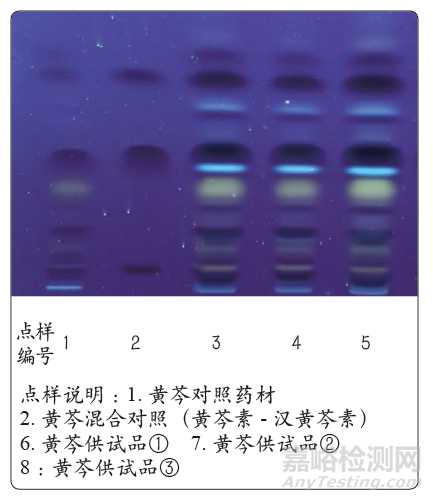
图4 中药黄芩粉高温瞬时灭菌后薄层鉴别色谱
结果分析
由图3、图4可以得出:灭菌前、灭菌后,供试品色谱中,在与对照药材色谱相应的位置上,均显相同颜色的斑点;在与对照品色谱相应的位置上,均显三个相同的暗色斑点;鉴别结果均符合检验标准要求,黄芩薄层鉴别无变化,说明高温瞬时灭菌对黄芩有效成分无影响,且检查数据重现性好。
4黄芩苷含量测定检查
检查方法
按《中华人民共和国药典(2020年版)》对黄芩粉高温瞬时灭菌前、灭菌后的黄芩苷含量进行对比检查。
合格标准
含量测定:含黄芩苷(C21H18O11)不得少于6.0%。
检查结果
灭菌前对照品色谱如图5所示,供试品色谱如图6所示;灭菌后对照品色谱如图7所示,供试品色谱如图8所示。根据色谱图可计算黄芩苷含量,黄芩苷含量测定检查结果详见表2。
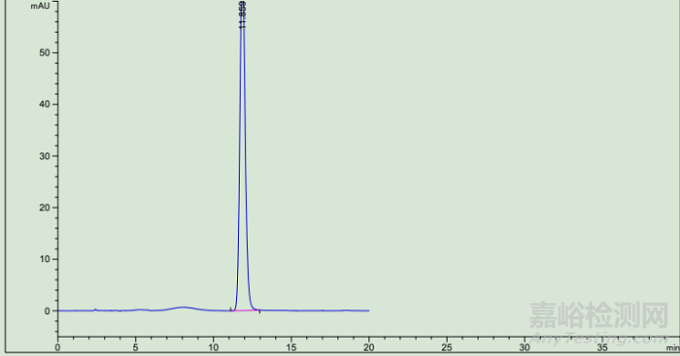
图5 中药黄芩粉高温瞬时灭菌前对照品高效液相色谱图
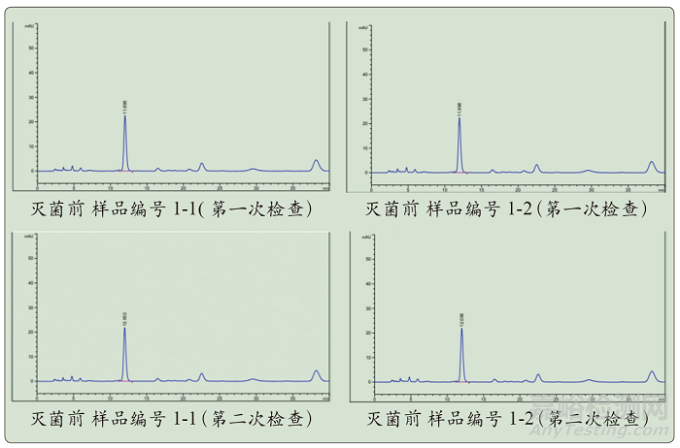
图6 中药黄芩粉高温瞬时灭菌前供试品高效液相色谱图
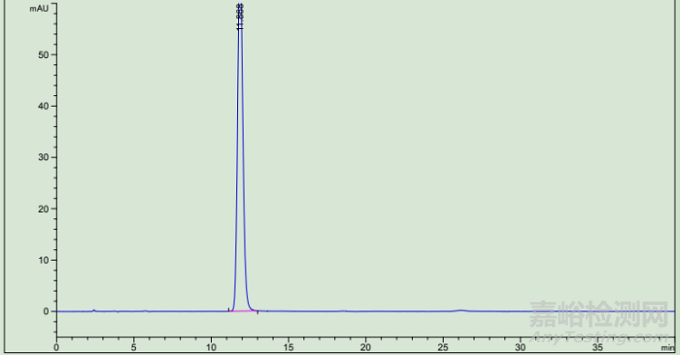
图7 中药黄芩粉高温瞬时灭菌后对照品高效液相色谱图
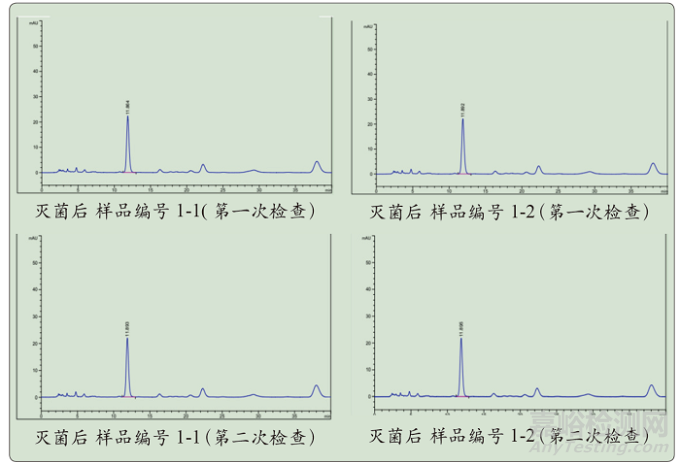
图8 中药黄芩粉高温瞬时灭菌后供试品高效液相色谱图
结果分析
在试验中,对照品高效液相色谱图、品峰面积,供试品高效液相色谱图、峰面积,黄芩苷含量测定等检验过程,均符合检验标准要求。由表2数据可以得出黄芩苷含量无变化,说明高温瞬时灭菌对黄芩有效成分黄芩苷无影响,且检查数据重现性好。
Part3结论
经过对高温瞬时灭菌设备的性能确认,得出中药材黄岑的需氧菌总数、霉菌和酵母菌总数在灭菌后均小于10 CFU/g,符合标准要求;峰面积在灭菌后与灭菌前相比基本无变化,也符合质量标准要求。在试验中,设备的计算机化系统权限管理、参数设定、操作运行等智能化设计各项控制功能的有效性良好,实验数据重现性好,符合中药灭菌智能化生产的设计目标,实现了中药材高温瞬时灭菌的智能化生产操作,且符合制药行业相关法规对权限管理的要求。该项新技术填补了国内空白,提供了一种新的灭菌方法,能在确保中药材有效成分不降解的同时有效去除微生物。本文中的试验为推进高温瞬时灭菌新设备、新技术、新方法在我国中药、食品行业的应用,提供了原始的参考依据和数据支持。
【参考文献】
[1]李玉梅,兰文飞,苗圩.中国制造2025:建设制造强国的行动纲领[J].军工文化,2015(10):12-15.
[2]苗圩.中国制造2025:建设制造强国的行动纲领[J].理论参考,2015(07):4-18.
[3]刘伟,杨营.工业4.0新形势下的机械制造及设备制造[J].装备维修技术,2022(05):0248-0248.
[4]王彦文.工业4.0新形势下的机械制造及设备制造[J].山东工业技术,2018(12):25-25.
[5]中华人民共和国卫生部.药品生产质量管理规范(2010年修订)[EB/OL].2011-01-17.https://www.nmpa.gov.cn/xxgk/fgwj/bm gzh/20110117120001434.html.
[6]国家食品药品监督管理总局.药品生产质量管理规范(2010年修订)附录:计算机化系统[EB/OL].2015-05-26.https://www.nmp a.gov.cn/xxgk/ggtg/qtggtg/20150526120001509.html.
[7]食品药品审核查验中心.药品数据管理规范(征求意见稿)[EB/OL].2016-10-10.https://www.nmpa.gov.cn/xxgk/zhqyj/zhqyjyp /20161010091001218.html.
[8]国家药品监督管理总局.药品记录与数据管理要求(试行)[EB/OL].2020-06-24.https://www.nmpa.gov.cn/xxgk/ggtg/qtggtg /20200701110301645.html.
[9]全国人民代表大会常务委员会.中华人民共和国电子签名法(2019年修正).[EB/OL].2019-04-23.https://wap.miit.gov.cn/zwgk /zcwj/flfg/art/2022/art_4ed0e4a46946479c90a9e0f2c76a11ef.html.
[10]国家药品监督管理局.中华人民共和国药品管理法(2019年修正)[EB/OL].2019-08-27.https://www.nmpa.gov.cn/xxgk/fgwj/ flxzhfg/20190827083801685.html.
[11]陶海涛.瞬时对药品食品粉末进行灭菌的系统[P].中国专利:CN106110346B,2021-08-20.
[12]陶海涛.一体框架隔离式管道流通粉末灭菌系统[P].中国专利:CN207626491U,2018-07-20.
[13]尚海宾.压力蒸汽灭菌法在中药制剂生产中的应用[J].机电信息,2013(26):33-38+51.
[14]尚海宾,邢俊加.小容量注射剂CIP在线清洗系统的概念设计[J].流程工业,2018(12):34-34,36,38-40.
[15]孟祥飞,尚海宾.混合系统的数据完整性[J].流程工业,2021(04):16-19.
[16]尚海宾.小容量注射剂干燥及包装生产质量风险管理[J].流程工业,2016(19):48-50.

来源:制药业


