您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-04-06 11:20
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
上海挚盟激动剂上Ⅰ期临床。挚盟医药自主研发的小分子口服TLR8激动剂CB06,在美国健康受试者中开展的Ⅰ期临床完成首例受试者给药。CB06是该公司管线中第2款进入临床的创新候选药物,拟用于慢性乙肝的治疗。CB06已在临床前研究中显示出良好的肝靶向特征,并通过在人外周血单核细胞中诱导细胞因子,以达到多种免疫介质去激活抗病毒功能。
国内药讯
1.恒瑞卡瑞利珠单抗肺癌Ⅲ期临床积极。恒瑞医药在2022 ELCC大会上公布其卡瑞利珠单抗联合卡铂和紫杉醇一线治疗ⅢB~Ⅳ期鳞状非小细胞肺癌的Ⅲ期临床最新结果。与化疗组相比,卡瑞利珠单抗联合化疗组中位OS延长接近1年(27.4个月vs15.5个月),死亡风险显著降低43%;2年和3年生存率均高出单纯化疗组约20%(53.4%vs35.0%,42.8%vs23.7%)。临床中未观察到新的安全性信号。
2.腾盛博药RNAi疗法Ⅱ期乙肝临床积极。腾盛博药siRNA候选疗法BRII-835(VIR-2218)在APASL2022会议上公布用于治疗慢性乙型肝炎病毒(HBV)感染患者的中国Ⅱ期临床最新数据。在16例达到病毒学抑制的非肝硬化慢性HBV感染患者中,两针皮下注射12周时,患者的HBV表面抗原(HBsAg)水平呈剂量依赖性降低,HBeAg阴性患者降幅为1.02 log10 IU/mL和1.22 log10 IU/mL,HBeAg阳性患者降幅为0.70 log10 IU/mL和1.15 log10 IU/mL。BRII-835总体耐受性良好。研究数据与之前用于其他人种/种族中的研究结果一致。
3.阿斯利康/第一三共ADC拟纳入突破性疗法认定。阿斯利康与第一三共开发的HER2-ADC新药Trastuzumab deruxtecan (T-DXd,Enhertu)用于治疗既往接受过一种或一种以上抗HER2药物治疗的不可切除或转移性HER2阳性乳腺癌的适应症获CDE拟纳入突破性治疗品种。这是该产品获CDE突破性疗法资格的第2项适应症,2020年12月,T-DXd单药用于既往接受过一种或一种以上治疗方案的HER2阳性局部晚期或转移性胃或食管胃结合部(GEJ)腺癌的适应症已被CDE授予突破性疗法资格。
4.歌礼第2款FASN抑制剂获批临床。歌礼制药1类新药ASC60片获批在国内开展临床试验,拟用于治疗晚期实体瘤。2019年2月,歌礼从Sagimet Biosciences公司引进两款FASN抑制剂(ASC40和ASC60)的大中华区独家授权,目前ASC40已在美国开展的ASC40联合贝伐珠单抗治疗高级别星形细胞瘤首次复发患者的II期临床中取得积极结果。在临床前小鼠肿瘤模型中,ASC60显示出可有效抑制肿瘤生长并加强mPD-1抗体的抑瘤效果。
5.徐诺RAF抑制剂获批国际临床。徐诺药业新一代广谱RAF抑制剂XP-102获FDA临床默示许可。这是一项国际Ⅰ/Ⅱa期临床,将主要在美国和中国评估XP-102用于治疗结直肠癌、非小细胞肺癌、恶性黑色素瘤和甲状腺肿瘤的安全性、耐受性及有效性。多项临床前研究显示,XP-102可能恢复耐药肿瘤的药物敏感性,有望为肿瘤耐药患者提供新的治疗方案。
6.辉瑞FIC肾病新药在华报IND。辉瑞1类生物制品注射用PF-06730512的临床试验申请获CDE受理。PF-06730512是一款基于ROBO2配体陷阱(ligand trap)的创新生物药,能够改善肾脏足细胞的功能,有望开发用于治疗多种和足细胞相关的蛋白尿性肾小球疾病。在一项用于治疗局灶节段性肾小球硬化(FSGS)的Ⅱa期临床中,PF-06730512显著降低患者尿蛋白肌酐比值,而且总体耐受性良好,没有观察到明显的安全性信号。
国际药讯
1.Novavax新冠疫苗申请用于青少年。Novavax公司重组蛋白新冠疫苗Nuvaxovid(NVX-CoV2373)向欧盟提交有条件上市许可申请(CMA),用于12-17岁青少年接种预防由SARS-CoV-2引起的COVID-19。在一项Ⅲ期PREVENT-19儿科扩展研究中,NVX-CoV2373达到主要终点,对Delta总体疗效达到80%;并且该疫苗总体耐受性良好。去年12月,Nuvaxovid已获欧盟委员会批准有条件上市,用于主动免疫预防18岁及以上个体由SARS-CoV-2引起的COVID-19。
2.吉利德CAR-T获批扩展适用范围。FDA批准吉利德旗下Kite Pharma开发的CD19-CAR-T疗法Yescarta(axicabtagene ciloleucel)扩展适用范围,用于二线治疗大B细胞淋巴瘤(LBCL)成人患者。在一项开放标签临床ZUMA-7中,Yescarta显著延长患者的无事件生存期EFS(HR=0.40,95% CI:0.31,0.51;p<0.0001),预估的EFS达到8.3个月(vs2.0个月)。Yescarta是FDA批准的第二款CAR-T,此前已获批用于治疗曾接受至少两次其他治疗未缓解或疾病出现复发的LBCL患者。
3.gMG皮下注射疗法Ⅲ期临床成功。Argenx公司开发的FcRn拮抗剂efgartigimod的皮下注射制剂,在治疗全身型重症肌无力(gMG)的Ⅲ期临床达到主要终点。与该药获批静脉输注(IV)制剂Vyvgart(efgartigimod alfa-fcab)相比,皮下注射制剂组第29天的平均总IgG水平相对基线降低达到非劣效性标准,两组IgG水平相对基线分别降低66.4%和62.2%。argenx计划今年年底向FDA提交皮下注射制剂的生物制品许可申请(BLA)。
4.PARP抑制剂维持治疗卵巢癌Ⅲ期临床成功。Clovis Oncology公司口服小分子PARP抑制剂Rubraca(rucaparib),在用于一线维持治疗晚期卵巢癌的Ⅲ期临床获积极结果。与安慰剂相比,Rubraca一线维持治疗显著提高研究者评估的无进展生存期(PFS)(20.2个月vs9.2个月,p<0.0001),而且PFS的改善不依赖于患者的生物标志物特征。该公司预计今年第二和第三季度向美国和欧盟的监管机构递交上市申请。
5.FIC帕金森病新药Ⅱ期临床积极。Cerevance公司选择性多巴胺D2受体靶向口服药CVN424治疗帕金森病的Ⅱ期临床结果积极。在左旋多巴或其它帕金森病药物的治疗背景下,与安慰剂相比,CVN424治疗4周后使患者“OFF”期改善1.3个小时(p=0.042);增加了患者无运动障碍的“ON”时间;并且还降低患者的白天嗜睡指标。临床中,CVN424总体安全性良好。
6.FIC止痛疗法两项Ⅱ期临床积极。Vertex公司选择性NaV1.8抑制剂VX-548,在治疗腹部整形手术或拇囊炎切除术后急性疼痛的两项概念验证Ⅱ期临床获积极结果。与安慰剂相比,高剂量VX-548治疗显著提高患者的痛觉评分SPID48(SPID48评分越高表明止痛效果越好),达到主要终点指标。在两项临床中,VX-548耐受性良好,无与VX-548相关的严重不良事件。
医药热点
1.北京完善肿瘤诊疗服务体系。北京市卫健委印发《2022—2024年北京市肿瘤诊疗质量提升行动方案》提出,完善肿瘤诊疗服务体系,明确综合医院、肿瘤专科医院、中医医院、安宁疗护机构等的功能定位,建立完善覆盖肿瘤诊疗全周期、全过程的医疗服务体系。《方案》还指出,医疗机构和医务人员要转变医学模式,关心患者心理变化,提供心理支持。
2.新冠核酸检测单人单检不高于28元。国家医保局、国务院应对新冠疫情联防联控机制医疗救治组发布关于降低新冠病毒核酸检测价格和费用的通知。通知提出,下调公立医疗机构新冠病毒核酸检测的政府指导价。各省份要将单人单检降至不高于每人份28元;多人混检统一降至每人份不高于8元。实行检测价格和试剂价格分开计价收费的省份,要按照不高于上述水平设置封顶标准。
3.我国新冠疫苗支出在医保承受范围。国家医保局日前就新冠疫苗价格情况、采购疫苗对医保基金的影响等社会热点问题做出回复。据介绍,我国自2021年2月正式启动居民免费接种新冠病毒疫苗,疫苗采购和接种费用主要由医保基金和财政共同负担;截至目前,我国已经接种32亿剂次疫苗,疫苗费用1200余亿元,疫苗支出费用在医保基金可承受范围内。
4.台湾出现首例感染XE变异毒株病例。据台媒报道,台湾指挥中心医疗应变组副组长罗一钧2日证实,台湾地区出现1例新冠XE变异毒株病例。该病例是一名3月18日从捷克入境的女性,经过落地采检发现阳性,属于无症状个案。XE(Stealth Omicron)是Omicron BA.1和BA.2的重组体,由于该毒株刚被发现,台媒表示目前尚未得知XE毒株的传播率是否较高。
评审动态
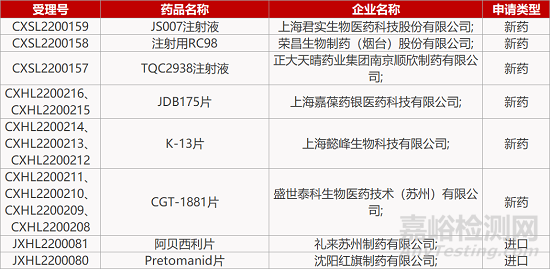
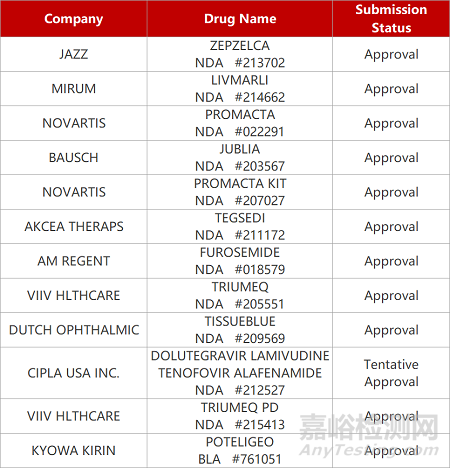

来源:药研发


