您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-01-23 08:46
近来随着人们对环保、安全、可持续发展越来越重视,壳聚糖作为天然高分子材料,逐步进入人们的视野,也引来了大批的研究者的关注研究,由于其具有生物降解性、生物相容性、可持续性、无毒、抑菌等多种优势特点,已广泛应用于食品、纺织、农业、环保、化妆品等各个行业。本文主要讲述了壳聚糖的特性及其在各种给药系统中的最新研究进展。
1. 前言
近年来随着新药研发技术的进步,许多药物活性化合物已被发现。然而,将药效物质传递到靶向目标是治疗疾病的关键。合适的给药系统(DDSs)可以增强这些新型药物的药代动力学和药效学特性,增强其细胞/组织和生物相容性。因此,研究高效、可靠、安全的给药系统成为了研究学者们的香饽饽。
新型给药制剂在过去的四十年里快速发展,与传统制剂相比有很多优势,如增强吸收速率和生物相容性,保护药物避免被酶解,精准给药至细胞和组织,调控体内的药物浓度。尽管这些优点很有吸引力,但也存在一些缺陷,比如毒性、降解副产品和不可生物降解,这仍然是我们面临的问题。因此可降解的生物相容性聚合物受到高度重视,天然高分子材料,如多糖、多肽或磷脂通常被用作载体。其中,壳聚糖是一种阳离子多糖,其卓越的物理特性和生物特性在给药系统中获得越来越多的认可。
2. 来源
壳聚糖是甲壳素(如图2a)衍生物,通常是通过甲壳素的碱性脱乙酰化获得的。如果甲壳素的来源是真菌,则需进行酶提取得到甲壳素,然后将甲壳素部分脱乙酰以获得壳聚糖。螃蟹和虾壳至今仍然是甲壳素的主要来源。图1说明了提取来源和从该来源加工甲壳素和壳聚糖的方法。
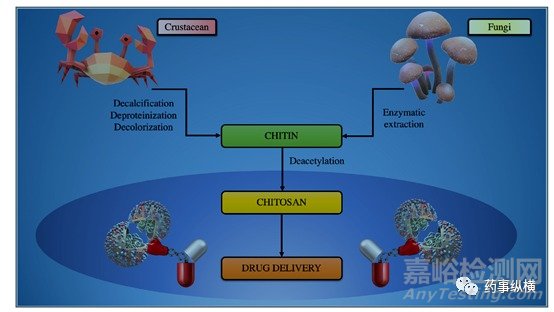
图1壳聚糖的来源和提取方法
壳聚糖是一种无毒,半结晶,可生物降解,具有生物相容性的线性多糖,由随机分布的N-乙酰氨基葡萄糖和β1-4相连的氨基葡萄糖单元组成(如图2b)。
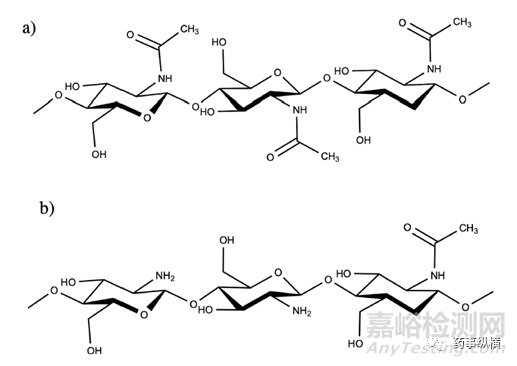
图2甲壳素和壳聚糖的化学结构图(a.甲壳素、b.壳聚糖)
壳聚糖由于含伯氨基,带正电荷,具有良好的粘接特性,能增强粘膜黏附,增加药物渗透作用的时间。壳聚糖具有较高的肾脏清除率,可以被酸和酶降解,降解产物可以通过肾脏清除。壳聚糖在生物系统中的生物降解速度和程度取决于脱乙酰度(DD),降解率随DD的增加而降低。壳聚糖的抗氧化特性也吸引了科学家的注意。AbhijeetB Muley等指出具有较低分子量(Mw)的壳聚糖具有比具有更高Mw的壳聚糖具有更高的抗氧化性能。壳聚糖可以有效地加工成各种功能形态,包括凝胶,纳米纤维,微珠,膜,支架,纳米原纤维,纳米颗粒,微粒和海绵状结构。因此,壳聚糖由于其卓越性能和各种形态被广泛应用于各种给药系统中。
3. 壳聚糖在给药系统中的研究进展
在过去几十年里大量的药品被发现,其中有些具有极佳的疗效,然而,它们的生物利用度和药代动力学非常差,导致全身不良反应。因此,给药系统研究成为了关键,如利用水凝胶,微珠、微球、纳米颗粒、纳米纤维、脂质体等来提高疗效。这些给药系统的制备方法有很多,如乳化交联、凝聚/沉淀、喷雾干燥、聚合法、离子凝胶法、反胶束法、筛分法。以下是以壳聚糖为载体的制剂通过不同的给药途径,使药物到达所需部位,发挥疗效的应用。
3.1 粘膜给药
为了避免首过效应,出现了粘膜给药系统,壳聚糖由于其粘附性和高渗透性是最理想的粘膜给药载体之一。胶束具有分子可修饰性,生物相容性,载药性,生物降解性,被应用于该给药系统中。研究人员合成了磷酸化的壳聚糖-硬脂酸共轭物(CSSAP),随后将其转化为ζ电势变化的胶束。最初,带负电荷的区域使胶束跨粘液层扩散,随后的正电荷改善药物与细胞膜和粘液的接触,从而避免向后扩散的效果(见图3)。CSSAP胶束显示出较高的粘液渗透和细胞缔合(HEK-293细胞)性,因此可用于疏水性药物和大分子药物的粘膜给药。
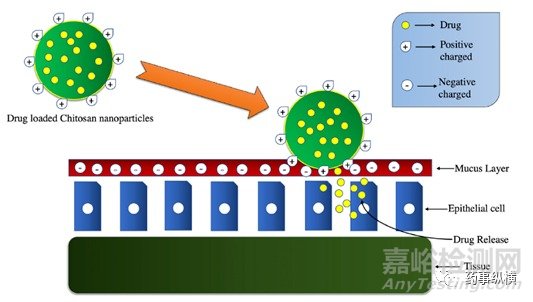
图3.壳聚糖纳米颗粒(CS-NP)的结构及其与黏液层的关系示意图。
(从左边开始的CS-NP,当它到达黏液层时,在静电吸引的帮助下与带负电荷的黏液层结合,并随着时间释放药物)
癌症研究仍然是所有研究人员喜欢的内容。但是,设计对人体内部新陈代谢状态有反应的输送系统仍然很麻烦。在各种刺激类型的系统中,pH响应系统是用于设计敏感纳米制剂来进行抗癌治疗最常用的方法。梁毅等利用席夫碱反应,制备了一种多功能的黏膜粘附和pH响应的壳聚糖二氢咖啡酸(CS-DA)和氧化支链淀粉(OP)注射用水凝胶,包载阿霉素(DOX)来治愈结肠癌。他们制备的水凝胶显示出优异的可注射性,体外pH依赖性和流变性,在不同pH条件下的释放性极好,可有效破坏结肠肿瘤细胞(HCT116细胞),可注射的pH响应型水凝胶主要用于粘膜粘附或结肠癌的药物给药。
处方药依卡贝钠具有抗黏膜性,为了克服这一缺点,J.Y.Kim等制备了依卡贝钠壳聚糖蔗糖电解质复合物(ChEs)。在药物释放实验中,与依卡贝钠悬浮液相比,ChEs在12小时内显示出高达80%的持续释放。C.N.Cheaburu-Yilmaz等制备并表征了伏立康唑交联N异丙基丙烯酰胺(PNIPAAm)和聚乙烯醇(PVA)(CS-g-PNIPAAm/ PVA)冷冻凝胶。伏立康唑的载药量为70%。该药物的体外释放曲线显示出符合Fickian扩散,8小时内释放38%,稳定研究表明,储存两个月后冷冻凝胶制剂仍然稳定。此外,HK-2细胞培养实验表明PNIPAAm/ PVA冷冻凝胶无毒。该复合材料是合适的粘膜给药材料。
最近的壳聚糖制剂研究,如3D打印的木糖醇和双氯芬酸钠壳聚糖/PVA,曲安奈德儿茶酚共轭壳聚糖,强力霉素琥珀酸酯和吡哆醇盐酸盐戊二醛/壳聚糖,奥沙利铂壳聚糖混悬液,西替利嗪壳聚糖,阿霉素壳聚糖和阿霉素的季铵盐衍生物壳聚糖等均应用于促进粘膜给药。
3.2 眼用制剂
传统的眼科制剂如滴眼剂通常是用于治疗眼前部疾病。由于眼中的结构,如泪膜(鼻泪引流,催泪,泪液周转,泪液稀释),角膜(对扩散的抵抗力高),结膜(对扩散的抵抗力,全身性的吸收),使眼用制剂达到治疗眼底疾病所需的治疗浓度是一项艰巨的任务。为了促进局部眼部治疗给药,科学家主要强调了两种方法:(1)利用粘度增强剂,粘膜粘附剂,颗粒和/或原位胶凝系统来延长角膜滞留时间,(2)利用渗透促进剂,胶体载体(例如纳米颗粒和脂质体)。壳聚糖及其衍生物由于其粘膜黏附特性和可降解性,被用作眼部制剂控制释放的载体。此外,壳聚糖制剂在角膜表面的保留时间比传统眼用制剂更长。
影响眼底病以令人震惊的速度增长(占眼部疾病总数的55%)。胶体药物载体(例如聚合物纳米胶束)的最新发展为药物输送到眼后部的途径打开了一个窗口。如今,研究人员正在研究用于眼底疾病的纳米胶束,使药物浓度达到治疗水平。例如,X.Xu等开发了基于地塞米松(Dex)的壳聚糖寡糖-缬氨酸-缬氨酸-硬脂酸(CSOVV-SA)纳米胶束,增强眼后部药物生物利用度,该胶束被证明对增强粘膜粘附性,生物相容性和穿透性以及持续释放药物非常有用。
右旋糖酐(Dex)是用于治疗不同炎症的最大甾体活性物质之一,像其他传统的眼药水一样,Dex眼药水给药后也迅速通过眼泪或鼻泪引流除去,以及角膜上皮层的不渗透性导致生物利用度低。因此,市售的Dex滴眼液通常疗效低下,需重复给药以维持药物治疗所需浓度。为了克服这些缺陷,研究人员一直专注于一些如角膜前药物保留,持续释放药物,及扩大角膜通透性的研究。A.Yu等设计了共轭地塞米松-乙二醇壳聚糖(Dex-GCS)纳米颗粒(粒径-277-289nm)水溶液。以磷酸盐缓冲液(PBS,pH= 7.4)为释放介质的体外释放实验显示Dex逐渐释放,释放时长可达48小时。该Dex-GCS无细胞毒性,可以治疗不同眼部炎症疾病。
为了克服眼部用药的缺陷,研究者们还研究了一种原位胶凝制剂,该制剂注入眼睛时,呈液体形式,但到达眼睛的结膜囊部位后变成粘弹性凝胶,随后药物持续释放,可降低给药频率。H.Shi等人合成了基于己酰二醇壳聚糖(HGCS)的热敏水凝胶(原位凝胶),以增强左氧氟沙星的眼生物利用度,研究结果表明HGCS可以延长角膜前药物的保留时间,体外细胞毒性研究表明无细胞毒性。体内药代动力学研究表明,载有左氧氟沙星的H-GCS水凝胶相比左氧氟沙星的水溶液可提供较高的Cmax和AUC0–12h(曲线下的面积),增强生物利用度。因此, H-GCS水凝胶可以用作局部眼用给药的有利载体。
研究学者们设计了不同的壳聚糖用于改善眼部给药的制剂。例如,酒石酸溴莫尼定壳聚糖,氟比洛芬壳聚糖,京尼平壳聚糖/明胶,噻吗洛尔壳聚糖/明胶,盐酸倍他洛尔MTT/壳聚糖,左氧氟沙星壳聚糖,槲皮素京尼平壳聚糖,香豆素壳聚糖,这些是最近的具有改善的眼部用药的壳聚糖制剂。
3.3 经皮给药
经皮给药被认为是最受青睐的替代口服和静脉给药的途径,因为其具有明显优势,即各种药物载体均可以通过透皮途径直接进入全身循环,避免肝脏代谢,并且不受胃中酸性介质,酶以及可变血浆浓度的影响。可将药物以无创方式,如喷雾、贴剂或凝胶形式通过皮肤给药。该给药系统需要具备无毒、无刺激的材料,同时该材料不应与治疗药物反应。但是上市经皮给药产品很少能透过皮肤角质层障碍,为了克服这一缺陷,必须提高药物制剂的细胞渗透性。J.Radwan-Prag等以乙酰水杨酸为模型药物,采用化学交联法,制备了壳聚糖氧化锌纳米水凝胶,小鼠成纤维细胞L929毒性试验表明该制剂无毒,药物释放试验研究表明,新型水凝胶按一级动力学模型释放,可有效控制药物的释放。
卵磷脂/壳聚糖纳米颗粒(LCNs)已受到全世界的关注。LCN是通过静电相互作用通过自组装带正电荷的壳聚糖和带负电荷的卵磷脂而合成的。由于壳聚糖和卵磷脂均具有增强的渗透性和粘膜粘附性,可以扩大药物在不同生物屏障上的渗透,可以通过口腔,粘膜,透皮和眼的生物屏障,具有广阔的应用前景。黄芩素是一种天然的类黄酮,具有抗菌和消炎作用,是治疗皮肤病的理想药物。但是,由于其不良的亲脂性和亲水性,其药用受到限制。为了增强黄芩素的稳定性,药物渗透性和延长药物保留时间,J.Ye等制备了黄芩素卵磷脂/壳聚糖纳米颗粒,包封率高达84.5%,具有良好的渗透性和较长的药物保留时间,无皮肤刺激性。
一种有效的阿片类药物拮抗剂纳曲酮(NTX)盐酸盐可以肌内或口服给药。这两种给药途径都有明显的缺点。口服NTX会通过肝脏代谢,导致胃肠道不适及血浆浓度波动。肌内注射NTX成本高昂,需要医学专业知识,并且注射会引起局部疼痛。NTX的透皮给药可以克服肌肉和口服给药的缺点。然而,NTX的亲水性限制了其在透皮吸收中的应用。近年来,微针(MN)透皮给药已被发现可用于NTX的透皮给药,可增强药物向皮肤深层的渗透。A.T.Ogunjimi等将壳聚糖-NTX微球与微针给药相结合,可使NTX通过皮肤屏障。采用喷雾干燥法将NTX包封到壳聚糖微球中,包封率为70%~87%,壳聚糖-NTX微球经过微针注射NTX的通量为11.6±2.2μg/cm2∙h,远大于NTX皮肤直接给药量,壳聚糖-NTX微针可增强患者的依从性,并改善NTX在皮肤上的持续给药。
为了克服肌肉和口服药物给药的缺陷和提高患者顺应性,研究人员设计了许多新型透皮给药制剂,如吲哚菁绿壳聚糖包衣脂质体、玫瑰红B水溶性壳聚糖、盐酸西替利嗪壳聚糖、吡非尼酮壳聚糖海藻酸钠、利多卡因壳聚糖等,这些制剂均可以促进透皮给药吸收。
3.4 口服给药
口服给药由于可以大规模生产,患者顺从性较好,通常为首选给药方式,但是要实现有效的口服治疗,必须克服几个障碍,例如,pH值可变(胃是高酸性的),酶的存在,肝脏中的首过代谢以及肠吸收障碍。上述问题限制了活性物质进入全身循环,因此降低了口服药物生物利用度。喜树碱(CPT)被认为是一种功能强大的有效活性物质,在不同的癌细胞系中具有广泛的细胞毒性。但CPT容易水解为羧酸盐和水溶性差限制了其功效。水凝胶作为载体,可为增加药物溶解度。其次,其三维结构主要由抗肿瘤药物组成,可控制CPT在作用部位的释放,延长作用时间。研究人员通过壳聚糖的胺基和THPC的羟甲基之间的共价键合制备了CPT壳聚糖水凝胶,提高了CPT的溶解性,可保护肠粘膜,以及延长给药部位的CPT浓度(持续释药48小时),较好的生物相容性和低毒性。
大黄酸(RH,1–8二羟基-3-羧基蒽醌),具有保护肾脏、抗炎、抗肿瘤、抗菌等药理作用,已引起了全世界的关注。然而由于RH水溶性较小,生物利用度低,使其在生物医学领域的应用受到阻碍。L.Jingwen等采用酰胺化法制备大黄酸壳聚糖(RH-LMWC),研究结果表明RH-LMWC共轭体系可提高稳定性,可帮助延长RH的半衰期,增加了溶解性。
虾青素(ASTX)是治疗肝纤维化的药物,由于其水溶性差和生物利用度低,用药受到限制。Q.Hu等将ASTX掺入硬脂酸共轭物中制备壳聚糖-酪蛋白酸钠-葡聚糖三元复合物(SA-CS/ NaCas /Odex)。这项研究为开发纳米粒子基于通过口服提供亲脂性药物来治疗肝纤维化提供了一种新颖的方法。另外,Q.Hu和他的团队利用戊二醛(GA)和氧化葡聚糖作为交联剂制备姜黄素壳聚糖纳米颗粒(SA-CS/ NaCs)。该纳米颗粒被证明在进食状态和禁食胃肠道条件下均具有良好的控释特性,在中性环境下表面电荷呈正电荷,这表明其有望作为疏水性药物的口服缓释载体。在另一项研究中,M.Motiei等人通过水包油乳液/离子胶凝方法制备的两亲性壳聚糖NP促进了疏水性药物来曲唑(LTZ)的吸收体外实验证明起初,LTZ突然释放,随后是缓慢释放。
4 、结语
除上述给药系统以外,壳聚糖在肺部给药、阴道给药、鼻腔给药等等,均有应用,如布地奈德壳聚糖纳米颗粒、妥布霉素海藻酸盐/壳聚糖颗粒、头孢克肟的壳聚糖-海藻酸盐微球、克霉唑包裹在壳聚糖/PLGA纳米颗粒、布洛芬壳聚糖、马来酸氯苯那敏壳聚糖等等。这篇综述讲述了利用壳聚糖制备成不同给药途径的药用剂型,壳聚糖及其衍生物在药物制剂给药系统方面具有巨大的应用前景。
原文来源:
B S P A , C V S . Connecting the dots in drug delivery: A tour d'horizon of chitosan-based nanocarriers system[J]. International Journal of Biological Macromolecules, 2020. https://www.sciencedirect.com/science/article/abs/pii/S0141813020352491?via%3Dihub

来源:Internet


