您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2020-03-16 10:16
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
「本文共:16条资讯,阅读时长约:3分钟 」
今日头条
O药在华获批治疗晚期胃癌。百时美施贵宝PD-1抑制剂欧狄沃(纳武利尤单抗注射液)获国家药监局批准,用于治疗既往接受过两种或两种以上全身性治疗方案的晚期/复发性胃或胃食管连接部腺癌患者。这是继非小细胞肺癌、头颈部鳞状细胞癌之后,欧狄沃在中国获批的第三个适应症。在一项全球Ⅲ期临床ATTRACTION-2中,欧狄沃可使患者死亡风险降低38%,一年生存率翻倍,达27.3%;而且中国台湾人群亚组中数据与整体人群结果一致;临床中欧狄沃的安全性与既往实体瘤临床试验报道一致。
国内药讯
1.花园药业硫辛酸注射液获批生产。花园药业的硫辛酸注射液仿制6类上市申请获国家药监局批准生产。硫辛酸注射液为糖尿病用药,用于糖尿病周围神经病变引起的感觉异常及其他氧化应激所致疾病。原研药是德国史达德的奥力宝。2018年中国公立医疗机构终端硫辛酸注射剂销售额为17.60亿元。目前拥有硫辛酸注射液批文的国内企业有12家,注射用硫辛酸有2家。该品种尚未有企业通过一致性评价。
2.国家药监局已批准17款新冠检测试剂盒。3月12日,国家药监局应急审批通过明德生物新型冠状病毒2019-nCoV核酸检测试剂盒(荧光PCR法)。该产品采用多重PCR-荧光探针检测方法,结合一步法RT-PCR技术,对新型冠状病毒2019-nCoV感染的肺炎疑似病例、疑似聚集性病例患者、其他需要进行新型冠状病毒感染诊断或鉴别诊断者的口咽拭子、鼻咽拭子和痰液样本中新型冠状病毒(2019-nCoV)ORF1ab基因、N基因进行检测。截至目前,国家药品监督管理局共批准新冠病毒核酸检测试剂11个,抗体检测试剂6个。
3.豪森氟维司群注射液申报上市。3月13日,豪森4类仿制药氟维司群注射液上市申请获CDE承办,成为继正大天晴之后该品种第二家国产仿制药报产的企业。氟维司群为雌激素受体(ER)下调剂,原研厂家为阿斯利康,于2002年4月获FDA批准上市,用于抗雌激素药物(如他莫昔芬)治疗后病情仍趋恶化的绝经后乳腺癌患者,2019年该药的全球销售额8.92亿美元,目前该药已获批进口中国。
4.杨森FGFR抑制剂在华获批临床。杨森FGFR抑制剂erdafitinib片获国家药监局三项临床试验默示许可,适应症为接受卡介苗治疗后复发、且携带FGFR突变或融合的高危非肌层浸润性膀胱癌。Erdafitinib是一款first-in-class疗法,已于2019年4月在美国加速获批上市,是FDA批准的首款针对转移性膀胱癌的靶向疗法,这些患者携带特定FGFR基因突变。截止日前,erdafitinib片在中国已获6项临床试验默示许可,共涉及两种适应症。
5.复宏汉霖RANKL单抗临床申请获受理。复宏汉霖自主研制的重组抗RANKL全人单抗注射液HLX14的临床申请获国家药监局受理,拟开发适应症为高危骨折风险的女性绝经后骨质疏松症。HLX14是Denosumab (Prolia®)的生物类似药。Denosumab已先后在美国和欧盟获批上市,主要用于预防多发性骨髓瘤患者和实体瘤骨转移患者的骨骼相关事件、骨巨细胞瘤、高骨折风险的骨质疏松症的治疗等适应症,可增加患者骨密度、降低患者骨折的风险。目前,Prolia®已获批进口中国。
国际药讯
1.艾伯维Venclyxto非化疗联合方案获欧盟批准。艾伯维宣布其Venclyxto®(venetoclax)与Gazyvaro(obinutuzumab)联合用药方案已获欧盟委员会批准,用于一线治疗慢性淋巴细胞白血病(CLL)成人患者。Venclyxto是艾伯维与罗氏共同开发的一种全球首创的选择性靶向b细胞淋巴瘤-2(BCL-2)蛋白的药物。在一项代号为CLL14的Ⅲ期临床中,在40个月的治疗后时,与Gazyvaro+苯丁酸氮芥相比, Gazyvaro+ Venclyxto显著降低了患者的疾病进展风险,Gazyvaro+ Venclyxto组未达到中位PFS,Gazyvaro+苯丁酸氮芥组的中位PFS为35.6个月。Venclyxto+Gazyvaro组估计的36个月无进展生存率为81.9%,Gazyvaro+苯丁酸氮芥组为49.5%。
2.FDA批准罗氏COVID-19测试新方法。FDA紧急批准罗氏开发的一种可以在全自动设备上大规模进行的SARS-CoV-2测试新方法上市,以用于检测筛查引发全球COVID-19大流行的新冠病毒。据悉,该检测方法将在欧洲CE认证的市场上推出,在罗氏广泛使用的cobas 6800/8800系统上运行,可以在3.5小时内提供检测结果。最大的机器可以在24小时内提供多达4128项测试的结果。
3.Engage创新癫痫吸入式疗法达Ⅱb期临床终点。Engage公司口腔吸入式疗法Staccato alprazolam在治疗癫痫的Ⅱb期临床StATES中达主要终点,与安慰剂组相比,治疗组患者接受治疗后在两分钟内停止癫痫,且在两小时内未复发的患者比例显著提高。Staccato alprazolam是一款小型手持口腔吸入式癫痫发作急救疗法,由已获FDA批准的Staccato递送技术和上市药物阿普唑仑(alprazolam)构成,具快速起效特点,平均只需要30秒就可以终止患者的癫痫发作。
4.恩格列净新适应症获FDA快速通道资格。勃林格殷格翰和礼来联合宣布,FDA授予其SGLT2抑制剂恩格列净(empagliflozin,Jardiance)快速通道资格,以降低慢性肾病成人患者的肾病进展和心血管死亡风险。在一项临床研究EMPA-REGOUTCOME中,恩格列净将2型糖尿病患者的肾病和心血管疾病发生和进展风险降低了39%。2016年,恩格列净已获FDA批准用于降低患有心血管疾病的2型糖尿病患者的血糖,以及他们因心血管疾病死亡的风险。
5.Lynparza联合VEGFR抑制剂卵巢癌Ⅲ期临床失败。阿斯利康和默沙东宣布,Lynparza(奥拉帕利)与cediranib(西地布尼)联用对比铂类化疗用于铂敏感的复发性卵巢癌患者的Ⅲ期临床试验GY004未达到主要终点。在意向性治疗(ITT)人群中,西地布尼+奥拉帕尼与化疗相比使得患者无进展生存期(PFS)没有取得统计学上的显著改善。GY004研究观察到的安全性和耐受性概况与每种药物已知的情况相一致。详细结果将在未来的医学会议上展示。奥拉帕尼是阿斯利康开发的“first-in-class”聚ADP核糖基聚合酶(PARP)抑制剂,目前已获批的适应症覆盖卵巢癌、乳腺癌、前列腺癌等。
6.Kymera完成C轮融资。致力于使用靶向蛋白质降解疗法为患者创造突破性药物的生物技术公司Kymera Therapeutics公司完成1.02亿美元C轮融资,这些资金将用于推进其多款在研疗法进入临床开发阶段。Kymera专有的Pegasus靶向蛋白降解平台利用人体的天然蛋白回收机制降解引起疾病的蛋白,它能够使用基于小分子药物的方法,去针对那些无法被传统小分子药物所抑制的蛋白。Kymera开发的主要靶点是IRAK4。IRAK4是一种在toll样受体和IL-1受体介导的炎症中起重要作用的蛋白。Kymera正计划在多种自身炎症,自身免疫性疾病,以及肿瘤疗法适应症中推进IRAK4降解疗法。
医药热点
1.全球医药领域企业市值TOP50榜单。Endpoints News发布了最新的全球生物制药领域的企业市值TOP50排行榜(市值结算时间为2020年3月5日)。在名单中,有6家中国企业上榜,包括恒瑞医药(第22名)、豪森药业(第29名)、中国生物制药(第36名)、石药集团(第41名)、百济神州(第47名)5家药企,以及全球领先的开放式、一体化生物制药能力和技术赋能平台药明生物(第33名)。
2.英国或将于下周开始禁止大型聚集活动。据英媒报道,英国政府正在制定进一步防控新冠病毒传播措施,其中有可能最早于下周开始禁止大型聚集活动。3月12日,苏格兰地区政府已经采取措施,禁止举行500人以上的聚集性活动。此前,英国政府就应对新冠病毒传播第三次召开“眼镜蛇”会议后,并没有采取停课、取消公众聚集活动等措施,从而饱受民间争议。截至到当地时间3月14日早9点,英国累计确诊达到1140人,累计死亡21人。
3.美国进入“国家紧急状态”。据媒体报道,美国3月13日下午宣布进入“国家紧急状态”,以释放更多资金与资源应对新冠肺炎疫情。美国国会众议院14日凌晨表决通过旨在援助国民应对疫情的“家庭优先冠状病毒应对法案”。据悉,进入“国家紧急状态”,可为美国联邦和地方政府提供额外500亿美元应对疫情资金。特朗普还公布一系列行政措施,包括以公私合作方式扩大在便利场所检测新冠病毒、减轻学生贷款负担和赋予医疗专业人士在治疗患者时额外“灵活性”。
4.江苏14名援鄂医护直升高级职称。江苏省人社厅近日发布消息,经江苏省高层次和急需紧缺人才高级职称考核认定委员会认定,该省14名被授予“全国卫生健康系统新冠肺炎疫情防控工作先进个人”的医护人员直接认定卫生系列高级职称,其中认定主任医师5名、主任护师5名、副主任护师4人。此次职称考核认定体现了突出抗疫表现、引导广大医护人员把论文写在临床一线、把研究成果应用到疫情防控一线的鲜明评价导向。
股市资讯
【华海药业】公司的"硫酸苯丙胺片"的新药简略申请获得美国FDA审评批准,该药用于治疗发作性睡病、脑炎后遗症、麻醉药或其它中枢神经抑制药中毒。
【亚太药业】1)2019年度实现营业收入7.09亿元(-45.84%);归母净利润-20.69亿元(-1,095.57%);扣非归母净利润-20.88亿元(-1,150.41%)。2)Wind一致增速无。3)公司及其子公司亚太房地产所持有的公司股份2,000.00万股(公司总股本的3.73%)被司法冻结。4)鉴于公司2019年度亏损,公司2019年度拟不派发现金红利,不送红股,不以资本公积金转增股本。
【凯普生物】公司提交的《创业板上市公司非公开发行新股核准》申请材料符合法定形式,中国证监会对该行政许可申请予以受理,收文编号为200417。
审评动向
1. CDE最新受理情况(3月15日)
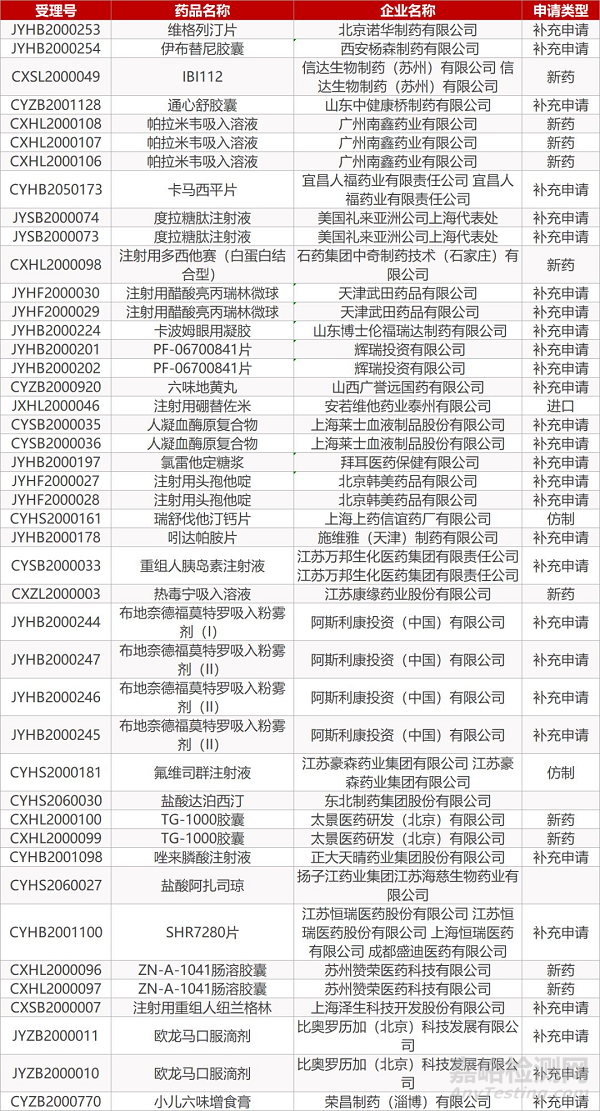
2. FDA最新获批情况(北美3月12日)
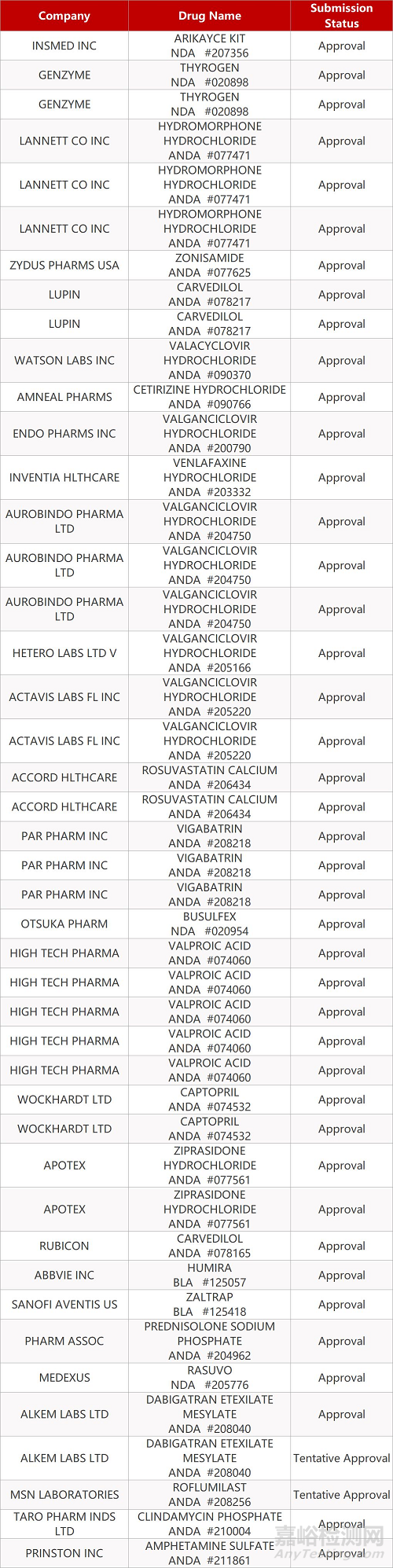
- The End -

来源:药研发


