您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2019-10-31 10:36
作者:王丽婵 , 晁哲 , 吴燕 , 骆鹏 , 卫辰 , 马霄
中国食品药品检定研究院, 国家卫生健康委员会生物技术产品检定方法及其标准化重点实验室, 北京 102629
摘要:
目的:比较不同类型无细胞百日咳疫苗免疫小鼠后诱导的抗体应答及其持久性。
方法:将来自于3家企业,采用2种不同工艺生产的无细胞百日咳疫苗(组分苗和共纯化苗)按一定比例稀释后分别给3组小鼠皮下接种,0.5 mL/只,于第4周加强免疫,剂量与初免疫相同。于免疫后第4周、第5周、第8周、第12周、第17周、第30周、第40周、第50周和第65周取血,分离血清,检测小鼠血清中抗百日咳抗体IgG水平(抗-PT和抗-FHA)和PT的中和抗体水平,并对其结果进行分析比较。结果:两类疫苗组检测结果比较,在免疫后第30周之前,两组之间抗-PT和抗-FHA水平无显著性差异;但在30周之后,两组之间抗-PT和抗-FHA水平有显著性差异(P < 0.05),组分苗组抗体水平高于共纯化苗组。中和抗体方面,组分苗组中和抗体水平高于共纯化苗组,两组比较有显著性差异(P < 0.05)。
结论:两种类型的百日咳疫苗免疫小鼠后均能诱导产生体液免疫应答,组分苗组的抗体持久性(包括百日咳抗体IgG和百日咳PT中和抗体)强于共纯化苗组;且百日咳IgG抗体与中和抗体之间具有一定的相关性。
关键词:无细胞百日咳疫苗 抗体 中和抗体 免疫持久性
百日咳疫苗包括全细胞百日咳疫苗(Whole Cell Pertussis Vaccine,WPV)和无细胞百日咳疫苗(Acellular Pertussis Vaccine,APV)两种,其中,无细胞百日咳疫苗根据百日咳工艺的不同又分为共纯化无细胞百日咳疫苗和组分无细胞百日咳疫苗。共纯化无细胞百日咳疫苗(以下简称共纯苗)采用共纯化技术自发酵产物中提取百日咳抗原,主要抗原成分为百日咳毒素(Pertussis Toxin,PT)和丝状血凝素(Filamentous Haemagglutinin,FHA)。组分无细胞百日咳疫苗(以下简称组分苗),采用的是柱层析分别纯化工艺自发酵产物中提取有效抗原,主要抗原包括PT、FHA和百日咳粘着素(Pertactin,PRN)三种成分,有效抗原成分明确且精确定量,质量稳定可控。目前,通过分别纯化工艺生产的已经上市的组分百日咳疫苗主要来自于进口,国内组分百日咳疫苗尚处于新药注册阶段。目前,国内大部分人群使用的是我国自主生产的共纯化无细胞百日咳疫苗。
百日咳血清学效力检测方法(Pertussis Serological Potency Test,PSPT),即百日咳疫苗免疫小鼠后,检测其百日咳特异性抗体IgG水平作为评价标准,此方法主要评价的是体液免疫效果。百日咳毒素CHO中和抗体法,主要检测的是疫苗主要成分PT免疫后产生的功能性抗体,与PSPT法检测的PT结合抗体不同,可以更确切地反映疫苗保护效果。意大利Von Hunolstein和美国Sutherland等人均认为此方法可辅助PSPT的检测[1-3]。本文主要观察这两类百日咳疫苗免疫小鼠后,采用PSPT法和CHO中和抗体法检测的百日咳抗体水平,并对其免疫效果进行为期65周的动态监测。
1 材料与方法
1.1 样品
共纯化无细胞百日咳疫苗、组分无细胞百日咳疫苗由中国食品药品检定研究院提供。
1.2 实验动物
BALb/C小鼠、雌性、6~8周、SPF级,由中国食品药品检定研究院实验动物中心提供,实验动物生产许可证号:SCXK(京)2014-0013。饲养于中国食品药品检定研究院动物实验室。
1.3 主要试剂及仪器
PT、FHA标准抗原和CHO-K1细胞由中国食品药品检定研究院百白破疫苗与毒素室提供;WHO鼠源抗百日咳血清标准品97/642和WHO百日咳毒素标准品JNIH-5,簇集活性每支10000 IU,购自英国生物标准与检定研究所(NIBSC);抗小鼠辣根过氧化物酶标记抗体为美国Life Technologies公司产品;培养基DMEM/F12(Cat. No. 21127-022)、胎牛血清(Cat. No. 10099-141)购自美国Gbico公司;其他化学试剂均为国产分析纯。酶标仪Spectra Max Plus购自美国Molecular Devices公司;EVOS成像显微镜购自美国AMG公司;细胞培养箱购自美国THERMO公司。
1.4 动物实验
将实验小鼠随机分为4组(Lot1到Lot3试验组和PBS组,其中Lot1为进口组分APV,Lot2为国内处于新药注册阶段组分APV,Lot3为国产共纯化APV),每组10只,腹部皮下注射经过5倍稀释的样品,0.5 mL/只,于免疫第28天进行加强免疫,剂量同上。于免疫后第4周、第5周、第8周、第12周、第17周、第30周、第40周、第50周和第65周取血,采集后的小鼠血液离心后收集血清,-20℃冰箱保存待用。
1.5 百日咳特异性抗体IgG水平检测
检测小鼠血清中抗-PT和抗-FHA的含量,采用常规间接ELISA法进行检测,以WHO鼠源抗百日咳血清标准品97/642作为标准(含抗PT-IgG 17 IU/支,抗FHA-IgG 143 IU/支)来计算血清中的抗体含量。PT、FHA包被抗原浓度均为3 μg·mL-1,置4 ℃冰箱过夜;洗板后按照实验方案设计格式分别加入经过稀释后的待检小鼠血清及标准品97/642,进行2倍系列倍比稀释直至酶标板最后一排,之后按常规ELISA方法步骤检测。终止显色反应后,使用SoftMax pro软件,酶标仪读板,以WHO标准品97/642的数据为标准,应用双平行线分析方法对待检样品进行统计分析,确定各种抗小鼠百日咳抗体的含量。
1.6 CHO细胞中和抗体滴度检测
采用CHO细胞簇集试验[4]。将待测样品和WHO鼠源抗百日咳血清参考品97/642(作为阳性对照)进行2倍系列稀释,加入稀释至0.4 IU·mL-1的PT毒素标准品JNIH-5进行毒素中和,置37℃结合2 h;将中和完成的毒素样品混合物加入到预先准备好的CHO细胞培养板中(细胞浓度3000个/孔),置5% CO2孵箱中培养48 h。同时,设置只有PT毒素和CHO细胞的毒素对照、培养基对照和CHO细胞对照。样品血清孔以显示<50%的细胞聚集的最高稀释度为中和抗体的最后滴度。抗血清阳性对照应有中和抗体滴度;毒素对照灵敏度应小于0.03 IU·mL-1;培养基和细胞对照应不簇集。
1.7 统计学分析
采用IBM SPSS Statistics 20软件对抗体检测数据和CHO细胞中和抗体滴度数据进行统计学分析。组间比较采用单因素方差分析,以P<0.05表示差异具有统计学意义;Spearman相关系数分析ELISA法P T抗体结果和C H O细胞中和抗体结果的相关性。
2 结果
2.1 抗体水平IgG检测
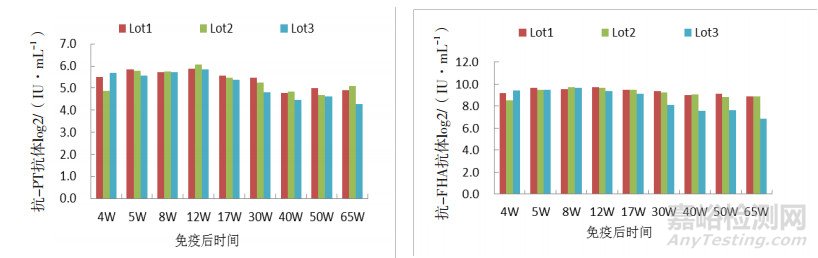
将每组百日咳抗体检测结果取平均值,转化为对数Log2后,进行比较分析。如图 1所示,免疫后第4周抗-PT和抗-FHA IgG水平均已升高,Lot1、Lot2组分APV组升高水平不及Lot3共纯化APV组明显;但是加强免疫后一周检测,即第5周检测结果显示,Lot1、Lot2组升高明显,Lot3组反而没有显著变化,说明Lot3组初次免疫后抗体水平就已明显升高。3组疫苗在免疫后第12周抗体水平达到峰值,之后有所下降,组分APV组从第40周开始、共纯化APV组从第30周开始抗体水平有显著性下降(P<0.05)。Lot1组和Lot2组的抗体水平比较,二者之间没有显著性差异;Lot1、Lot2组与Lot3组抗体水平比较,从第30周开始,无论是抗-PT,还是抗-FHA IgG水平,Lot3组均显著低于Lot1、Lot2组,均有显著性差异(P<0.05)。以上结果表明,国产共纯化APV疫苗免疫后抗体水平升高早,但是下降快,免疫持久性相对于组分APV疫苗组差。
图 1 小鼠免疫后第4周到第65周百日咳抗体检测结果
2.2 中和抗体检测
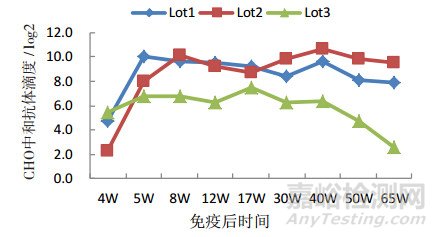
将3个试验组2 7次试验的C H O中和抗体和ELISA PT抗体的检测结果取平均值,转化为对数Log2后作图,见图 2。结果显示,虽然在免疫后第5周到第12周,3个试验组的抗-PT IgG水平没有显著性差别,见图 1;但是,Lot3组的CHO中和抗体水平在免疫后第4周,即加强免疫前并不比Lot1、Lot2组差,而加强免疫后,却显著低于Lot1和Lot2组(P<0.05)。随着免疫后时间的延长,Lot3组的中和抗体水平下降趋势更加明显。
图 2 小鼠免疫后第4周到第65周百日咳毒素CHO中和抗体检测结果
2.3 相关性分析
分别将各试验组的ELISA法PT抗体结果和CHO细胞中和抗体结果取对数后进行Spearman相关性分析,结果分别为Lot1组相关系数r=0.131,Lot2组相关系数r=0.200,Lot3组相关系数r=0.603,前两组为低度相关,Lot3组为显著相关。总体来说,ELISA法检测的抗-PT IgG水平与CHO中和试验检测的PT中和抗体水平之间具有一定的相关性。
3 讨论
无细胞百日咳疫苗有效性评价主要有两种方法,即小鼠血清学效力方法和改良脑腔攻击法(Modified Intracerebral Challenge Assay,MICA)。我国一直采用MICA法用于百日咳疫苗效力试验的放行。小鼠血清学效力法主要是应用ELISA法检测疫苗中各百日咳抗原组分在免疫小鼠后的抗体免疫反应,该方法在欧美国家已广泛用于评价疫苗的有效性[5-6]。CHO细胞中和抗体法,主要检测的是百日咳主要抗原PT诱导产生的中和抗体,而通过ELISA技术检测到的抗体为结合抗体,中和抗体肯定具有结合抗体的性质,但结合抗体不一定具有中和活性。
本实验中,采用ELISA法和CHO中和抗体法检测疫苗免疫后诱导产生的抗体应答,并连续监测至免疫后第65周,评价组分APV和共纯化APV在小鼠体内的抗体应答和免疫持久性。结果显示,ELISA法检测的结合抗体,组分APV与共纯化APV相比,在免疫后早期,到第30周,二者之间的抗体水平差异不显著,随后,虽然百日咳抗体水平都有下降趋势,但共纯化APV组下降更加明显,显著低于组分APV组。CHO细胞法检测的PT中和抗体,在免疫后第4周,此时尚未加强免疫,共纯化APV组的中和抗体水平与组分APV组的Lot1组没有显著差异,且高于Lot2组;但在加强免疫后,组分APV组的中和抗体水平远远高于共纯化APV组(P <0.05)。统计学Spearman相关性分析显示,两种方法的检测结果具有一定的相关性,Lot1、Lot2组为低度相关,Lot3组为显著相关。虽然此次试验选取的样本数量有限,但总体来说,ELISA法检测的抗-PT IgG水平与CHO中和试验检测的PT中和抗体水平之间具有一定的相关性,表明两种检测方法结合使用可更加全面反映抗原的免疫原性[7]。此外,PT中和抗体检测方法及其质量控制研究一直是本实验室正在研究项目的重点之一,最终目标是以这种相对简单、快捷、符合动物使用3R原则的质量评价方法,替代目前我国使用的MICA法。MICA法试验周期长,使用动物数量大,影响因素多。中和抗体的检测在后续研究中将进一步细化以积累更多数据。
综上所述,无论哪种工艺生产的无细胞百日咳疫苗,免疫小鼠后均能诱导产生抗体反应。在诱导抗体产生能力上,两种类型的百日咳疫苗在免疫后前期,ELISA法检测的抗体水平没有显著性差异,但随着监测时间的延长,共纯化苗组的抗体水平下降趋势较组分苗组显著。中和抗体检测结果显示,共纯化苗组显著低于组分苗组。
参考文献
[1] Von HunolsteinC, Gomez Miguel MJ, Pezzella C, et al. Evaluation of Two Serological Methods for Potency Testing of Whole Cell Pertussis Vaccines[J]. Pharmeuropa Bio, 2008(1): 7-18.
[2] Sutherland JN, MaynardA JA. Characterization of a Key Neutralizing Epitope on Pertussis Toxin Recognized by Monoclonal Antibody 1B7[J]. Biochemistry, 2009, 48(50): 11982-1193. DOI:10.1021/bi901532z
[3] Sutherland JN, Chang C, Yoder SM, et al. Antibodies Recognizing Protective Pertussis Toxin Epitopes Are Preferentially Elicited by Natural Infection Versus Acellular Immunization[J]. Clin Vaccine Immunol, 2011, 18(6): 954-962. DOI:10.1128/CVI.00561-10
[4] Hewlett EL, Sauer KT, Myers GA, et al. Induction of a Novel Morphological Response in Chinese Hamster Ovary Cells by Pertussis Toxin[J]. Infect Immun, 1983, 40(3): 1198-1203.
[5] Gaines DR, Horiuchi Y, Zhang SM, et al. Modified Intracerebral Challenge Assay for Acellular Pertussis Vaccines:Comparisons Among Whole Cell and Acellular Vaccines[J]. Vaccine, 2009, 27(49): 6824-6832. DOI:10.1016/j.vaccine.2009.09.014
[6] Van Der Ark A, Von Straaten-van, De Kappelle I, Hendriksen CF, et al. Pertussis Serological Potency Test as an Alternative to the Intracerebral Mouse Protection Test:Development, Evaluation and Validation[J]. ALTEX, 1998, 15(5): 33-36.
[7] Dalby T, Sorensen C, Petersen JW, et al. Pertussis Serology:Assessment of IgG Anti-PT ELISA for Replacement of the CHO Cell Assay[J]. APMIS, 2010, 118(12): 968-972. DOI:10.1111/j.1600-0463.2010.02664.x

来源:中国药事


