摘要:药用气雾剂是一种特别的药物剂型,在治疗支气管哮喘、慢性阻塞性肺病等呼吸系统疾病方面具有其他剂型不可替代的优势;抛射剂是药用气雾剂中药液雾化的动力,也是溶解或分散药物的介质,作为药用气雾剂中的重要辅料,抛射剂的质量直接影响到药品的安全性和有效性。现对几类常见的药用气雾剂辅料抛射剂国内外质量标准进行概括比较,为我国药用气雾剂辅料抛射剂质量标准的制修订工作提供参考。
药用气雾剂系指原料药或原料药和附加剂与适宜的拋射剂共同封装于具有特制阀门系统的耐压容器中,使用时借助抛射剂的压力将内容物呈雾状物喷出,用于肺部吸入或直接喷至腔道黏膜、皮肤的制剂。按用药途径可分为吸入气雾剂、非吸入气雾剂;按处方组成可分为二相气雾剂(气相与液相)和三相气雾剂(气相、液相、固相或液相);按给药定量与否,可分为定量气雾剂和非定量气雾剂[1]。药用气雾剂具有便携、易使用、药物稳定性高、给药剂量准确、对创面刺激性小等优点,直接进入肺部的吸入气雾剂还可避免肝脏首过效应和减少对胃肠道的副作用。由于气雾剂中的药物可以直接雾化到作用部位或吸收部位,具有十分明显的速效作用与定位作用,因此,其在治疗支气管哮喘、慢性阻塞性肺病等呼吸系统疾病方面具有其他剂型不可替代的优势,但也正是由于气雾剂给药后药物的活性强,尤其是吸入气雾剂,直接作用于肺部并有全身吸收,吸收速度快,不亚于静脉注射,因此,与其他剂型的药物相比,气雾剂的安全性要求更高。
气雾剂中药液能以雾状喷射的动力来源是抛射剂,抛射剂是气雾剂必不可少的关键组成之一,同时,也是溶解或分散药物的介质。由于不同的抛射剂会引起气雾剂处方工艺和产品质量的变化[2],也会影响药物在呼吸道不同部位的分布和吸收[3],因此,抛射剂的质量会直接影响到药品的安全性和有效性。理想的抛射剂应无毒、无致敏性和刺激性;应无色、无臭、无味;应性质稳定,不易燃易爆,不与药物、容器发生相互作用;应廉价易得。在常温下的蒸汽压大于大气压,但在实际应用中,多数抛射剂的生产工艺流程复杂,最终产品中不可避免地含有生产过程中残留的水分、酸碱性物质、高沸点残渣、多种杂质等,而抛射剂中杂质的种类和含量更是会直接影响气雾剂的安全性。2016年,眼用全氟丙烷气体可疑严重不良事件的发生原因,即是全氟丙烷气体的含量不达标,杂质成分不明确[4]。因此,为保证药用气雾剂的安全性,对其辅料抛射剂进行必要的质量控制是非常重要的。
本文对几类常见的药用气雾剂辅料抛射剂的国内外质量标准进行概括比较,并归纳其异同点。
1 药用气雾剂辅料抛射剂种类
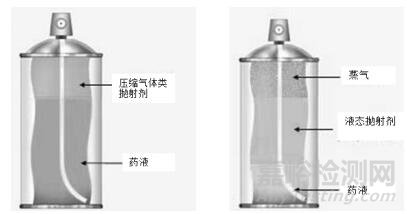
根据物理特性的不同,抛射剂可分为液化气体类和压缩气体类[5]。液化气体类抛射剂在常压下沸点低于室温,蒸汽压高,可均匀分散在气雾剂产品中,保持恒定的压力和喷雾模式,填充量一般为85%;根据分子结构其又可分为全氯氟烃类〔CFCs:三氯氟甲烷(CFC11)、二氟二氯甲烷(CFC12)和二氯四氟乙烷(CFC114)〕、碳氢化合物类(丙烷、正丁烷和异丁烷)、氢氟烷烃类〔HFCs:1, 1, 1, 2-四氟乙烷(HFA-134a)、七氟丙烷(HFA-227ea)〕和含氧化合物类(二甲醚)。压缩气体类抛射剂包括二氧化碳、氧化亚氮、氮气、压缩空气等;填充压缩气体类抛射剂的气雾剂、抛射剂只在气雾剂顶部空间,如图 1所示,使用时压力下降,导致喷出的颗粒粗糙,填充量只能达到50%~70%。
注:压缩气体类抛射剂在气雾剂使用过程中压力变小,其他类抛射剂能保持恒定压力。
图 1 压缩气体类抛射剂与液化气体类抛射剂在气雾剂产品中的区别
各国药典对药用气雾剂中抛射剂的使用类别限定基本一致:美国药典[6]中列出的抛射剂有丙烷、正丁烷、异丁烷、二氧化碳、氧化亚氮、氮气、CFC11、CFC12和CFC114,欧洲药典[7]中建议的抛射剂有氢氟烷烃、小分子烃类(丙烷、丁烷)、压缩气体类(二氧化碳、氮气、氧化亚氮);《中华人民共和国药典》(以下简称《中国药典》)对可以使用的抛射剂未作明确规定。
2 药用气雾剂辅料抛射剂质量标准
抛射剂的质量对气雾剂产品的质量和安全性起到相当关键的作用,自气雾剂发明以来,各国对抛射剂的质量、安全性及环境影响的研究从未停止,下面介绍各国药典收载的抛射剂质量标准情况。
2.1 液化气体类
2.1.1 全氯氟烃类
全氯氟烃类物质又称氟利昂(CFCs:CFC11、CFC12和CFC114),无毒、不易燃,具有合适的沸点、密度以及可接受的气味等优点,曾经作为药用气雾剂辅料抛射剂被广泛使用;但氟利昂对大气臭氧层有严重的破坏作用,而且是产生温室效应的重要物质之一;目前,在全球范围内已基本被淘汰。1985年,联合国环境规划署协调各国制定了《保护臭氧层的维也纳公约》;1987年,又签署了《蒙特利尔议定书》;提出要控制包括CFC11、CFC12和CFC114在内的8种CFCs类物质,随后,欧美日等发达国家相继制定了药用气雾剂CFCs分类淘汰政策并陆续完成了淘汰[8]。我国积极响应国际号召,自2007年起先后启动了“中国药用非吸入/吸入气雾剂CFCs消耗分步淘汰行业计划”,其中,由中国食品药品检定研究院包装材料与药用辅料检定所担任国内执行机构的“中国药用非吸入气雾剂CFCs消耗分步淘汰行业计划”已于2013年按时圆满完成;《关于禁止使用全氯氟烃类物质生产药用非吸入气雾剂的公告》 [9]在2013年正式发布,圆满实现了国家履约。“中国药用吸入气雾剂CFCs消耗分步淘汰行业计划”目前正在进行中,预计于2019年完成。
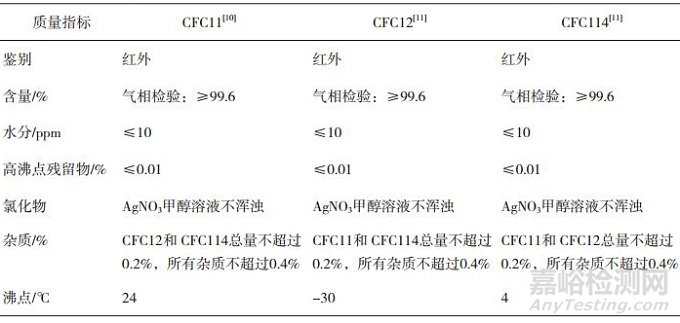
全氯氟烃类物质的质量标准仅在美国药典(USP40-NF35)中有过收载,在USP41-NF36版中删除了CFC12和CFC114,保留了CFC11,表 1列出了美国药典收载的CFC11、CFC12和CFC114质量标准检测项目,3种物质的检测项目、方法、限度均相同。由于其应用较早,相比于其他抛射剂,CFCs质量标准的项目和限度均较为宽松。
表 1 美国药典中全氯氟烃类抛射剂的质量标准
2.1.2 碳氢化合物类
丙烷、丁烷、异丁烷等碳氢化合物类抛射剂性质稳定,不会消耗臭氧层,也不会产生温室效应,毒性低,具有较好的溶解性且来源广泛,价格低廉,普遍用于非吸入气雾剂中。例如美国FDA橙皮书中收载的17种非吸入气雾剂在市新药(Newdrug application,NDA)中有16种使用的是丙烷、丁烷、异丁烷或其混合物(如表 2所示),但由于其是挥发性有机物质且易燃易爆,生产或使用中存在较大的危险,在欧洲一些国家被禁止用于气雾剂中。
表 2 美国FDA橙皮书收载的在市NDA新药所用抛射剂类型[12]
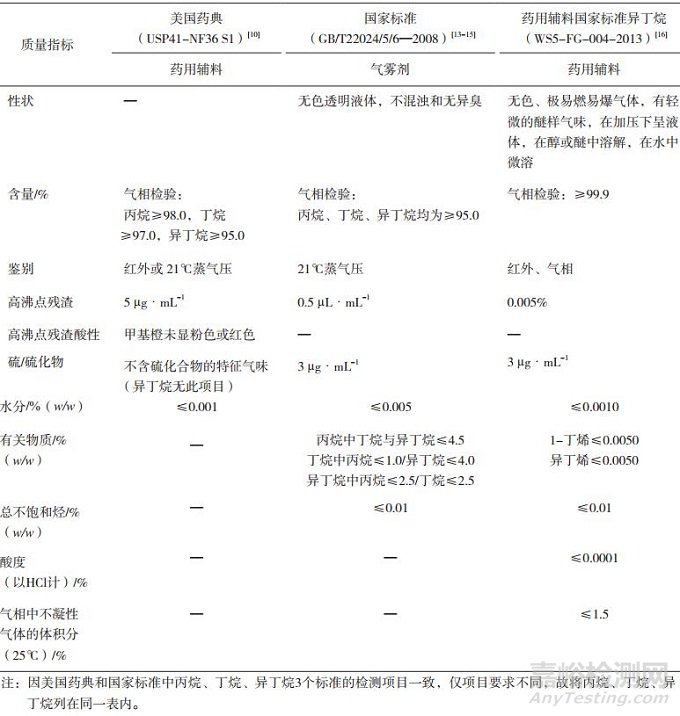
丙烷、丁烷、异丁烷的质量标准在美国药典(USP41-NF36 S1)、欧洲药典(EP 9.6)、英国药典(2018)中均有收载,但在欧洲药典、英国药典中仅规定了含量(99.0%V/V),没有对其他指标进行限定,日本药典、《中国药典》未收载。我国有药用辅料国家标准异丁烷(外用气雾剂用抛射剂,标准号:WS5-FG-004-2013);此外,还有国家标准:气雾剂级丙烷(A-108,标准号:GB/T22026—2008)、正丁烷(A-17,标准号:GB/T22024—2008)、异丁烷(A-31,标准号:GB/T22025—2008),《国家药用辅料标准手册》(2006年)也收录有丙烷、丁烷、异丁烷,引用的是美国药典标准,各标准对比情况见表 3。可见我国仅有药用级异丁烷的标准,而气雾剂级丙烷、丁烷的国家标准要求均低于美国药典标准,在中国药用非吸入气雾剂CFCs淘汰行业计划实施时,有部分气雾剂生产企业使用的是丙烷、丁烷、异丁烷作为CFCs的替代物且已成功替代,因此,为加强相关药品质量的监督管理、保障用药安全有效,需要进一步制定丙烷、丁烷的药用级标准。
表 3 碳氢化合物类抛射剂的国内外标准指标对比表
2.1.3 氢氟烷烃类
由于氢氟烷烃类抛射剂与传统医用气雾剂抛射剂CFCs具有相类似的热力学和物理性质,但是不含氯,臭氧消耗潜能值(ODP)为零,是一种化学惰性的氢氟烃,对大气平流层没有破坏作用,是非易燃品,因此是公认的CFCs替代物之一,在美国多用于吸入气雾剂,是我国CFCs淘汰后药用气雾剂中主要使用的抛射剂。
对于HFA-134a(Norflurane),欧洲药典(EP9.0版)、英国药典(BP2018版)均有收载,《药用辅料手册》(第六版)中也有收载,美国药典没有收载,但在计量吸入器(MDI)和干粉吸入器(DPI)产品——质量考量行业指南草案[Guidance for Industry-Metered Dose Inhaler(MDI)and Dry Powder Inhaler(DPI)Products]中对MDI和DPI产品用HFC-134a的杂质含量进行了规定。国内标准主要有药用辅料国家标准四氟乙烷(外用气雾剂用抛射剂,标准号:WS5-FG-003-2013)和浙江衢化氟化学有限公司、中化近代环保化工(西安)有限公司等生产企业的内控标准,其中,浙江衢化氟化学有限公司进一步制定了吸入气雾剂用HFA-134a的内控标准,与国家标准四氟乙烷(外用气雾剂用抛射剂,标准号:WS5- FG-003-2013)相比,对纯度、有关物质、高沸点残留物等项目的要求更加严格。
对于HFA-227ea(Apaflurane),公开的质量标准多为灭火剂、制冷剂用产品标准,公开的药用级HFA-227ea质量标准只有药用辅料国家标准七氟丙烷(外用气雾剂用抛射剂,标准号:WS5-FG-002-2013),2018年4月,美国FDA关于MDI和DPI产品-质量考量行业指南中提出了对HFA-227ea的质量要求。
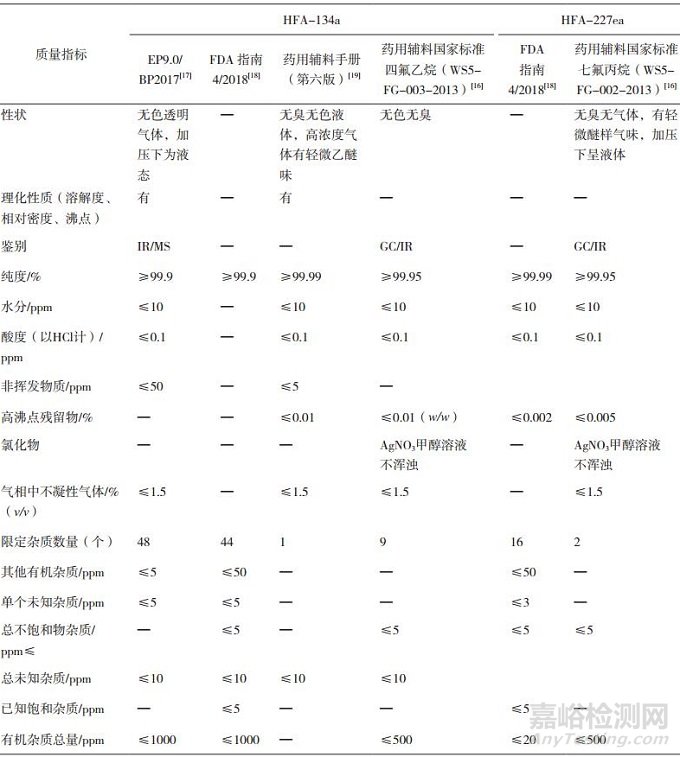
HFA-134a和HFA-227ea的各标准对比情况见表 4,我国发布的外用气雾剂用国家药用辅料标准对杂质的种类和限度较国外药典要求比较宽泛,而吸入气雾剂直接吸入肺部,因此,对抛射剂的水分、酸度和杂质的控制较外用气雾剂比均应更加严格。
表 4 氢氟烷烃类抛射剂的国内外标准指标对比表
2.1.4 含氧化合物类
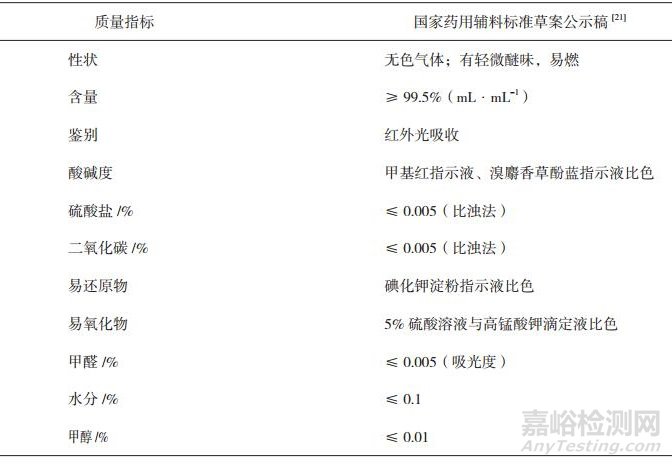
含氧化合物类抛射剂主要指二甲醚,最初在20世纪70年代开始使用,由于其压力适宜,低毒,可与水混溶,对极性和非极性物质均有较好的溶解性,对臭氧破坏值为零,不污染环境,广泛应用于香水、精油等行业相关的气雾剂中。在药用气雾剂领域,李雪梅等[20]用二甲醚成功替代了利多卡因氯己定气雾剂抛射剂。关于二甲醚的药用质量标准,目前仅有国家药典委员会发布的二甲醚国家药用辅料标准草案公示稿[21](见表 5),欧洲药典、英国药典、日本药典、美国药典均未收录该品种,马丁代尔大药典[22]有收载,但仅列出了分子式、CAS号、类别等信息,没有检测方法和限度的描述。
表 5 国家药典委员会发布的二甲醚国家药用辅料标准草案
2.2 压缩气体类
压缩气体类抛射剂有二氧化碳、氧化亚氮、氮气,其优点是易获得,价格便宜,不像挥发性烃类那样易燃易爆,但由于其压力太高,且使用时气雾剂罐内压力会随着气雾剂的使用逐渐变小,因此,目前使用很少。
二氧化碳在美国药典(USP41版)、欧洲药典(EP9.0版)、英国药典(BP2018版)、日本药典(JP ⅩⅦ)中均有收载,但未明确作为气雾剂抛射剂,《中国药典》(2015年版)中明确了类别为气雾剂抛射剂,但未对水分、NO、NO2、SO2进行限定,而抛射剂中这些物质的存在或可使药物的粒度、晶型发生变化,或可影响药物的存储,或可刺激粘膜,因此,应严格控制其含量。
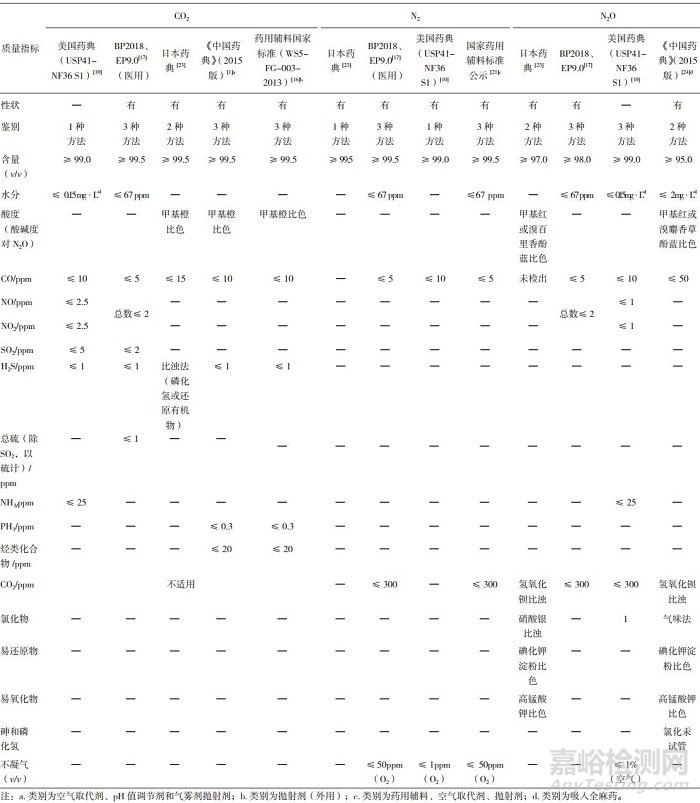
压缩气体类抛射剂的标准对比情况见表 6。N2和N2O在美国药典(USP41版)、欧洲药典(EP9.0版)、英国药典(BP2018版)、日本药典、(JP ⅩⅦ)中也均有收载,但均未明确品类为气雾剂抛射剂。2019年1月,国家药典委员会发布了“关于氮气和二甲醚国家药用辅料标准草案的公示(第二次)” [21],明确品类为药用辅料,空气取代剂,抛射剂,检查项目与限度均与欧洲药典一致。
表 6 压缩气体类抛射剂的国内外标准指标对比表
《中国药典》(2015年版)中收载的N2O为吸入全麻药,而非气雾剂抛射剂。
3 药用气雾剂辅料抛射剂质量标准的异同点
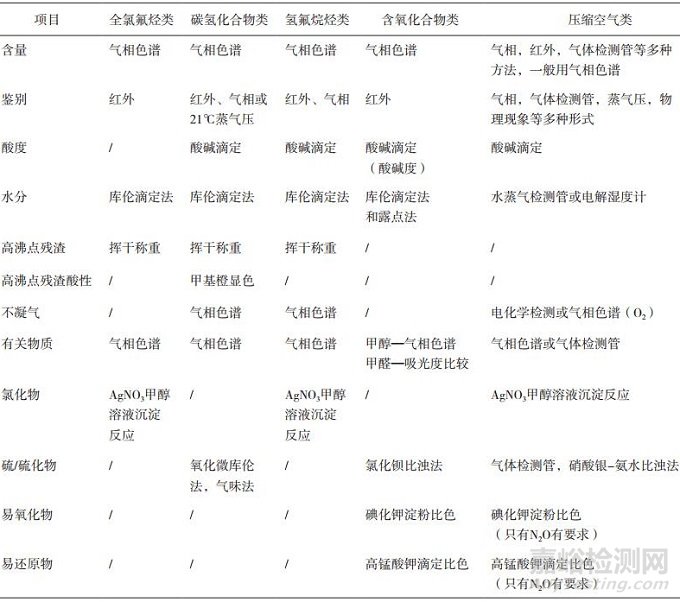
药用气雾剂辅料抛射剂在常温常压下均为气体,其质量标准限定项目有一定相似,水分、酸度、杂质种类及含量、不凝气几乎在所有抛射剂标准中均有涉及,一是由于这些指标同时也是气雾剂产品要求的指标,如水分、杂质[20],二是因为这些成分的存在会影响气雾剂生产工艺及产品的质量,如过多的水分会导致储存罐和传输管道的锈蚀[25],会引起混悬型MDIs中的药物微粒粒径增加,或微粒粒径分布、絮凝、喷雾模式、释药剂量和体内沉积部位等的改变,甚至可能会导致阀门的堵塞[26]; 过量的酸会引发产品安全性风险,如使皮肤失去对细菌的抑制作用,引发痤疮、毛囊炎等感染性皮肤病,使呼吸道黏膜受损,引发咳嗽和呼吸困难,导致肺炎、哮喘等疾病[27],杂质的含量会影响抛射剂主成分的含量,会引发产品的不稳定性,一些未知杂质的毒性无法评估。这些项目所用到的检测方法也基本类似,如表 7所示,含量和有关物质的检测一般用气相色谱法,水分检测一般用库仑滴定法,酸度检测一般用酸碱滴定法。
表 7 几类药用气雾剂辅料抛射剂质量标准的检测项目及方法
各类抛射剂质量标准的不同点主要是项目的限度要求不同,这一般是根据各类物质的理化特性和生产工艺决定的,如氢氟烷烃类抛射剂生产工艺较为复杂,生产过程中会产生较多的杂质,因此,对有关物质的种类和含量限定较挥发性烃类和压缩性气体类多且严格;压缩性气体类抛射剂吸湿性较弱,因此,对水分的限定较挥发性烃类和氢氟烷烃类抛射剂宽松。
4 结语与展望
我国药用气雾剂工业起步较晚,对抛射剂的质量研究也没有欧美等发达国家深入,如美国药典对抛射剂检测项目及方法均设有单独的指导原则[10],而我国药典对抛射剂种类及检测方法均未涉及。虽然近年来在中国药用非吸入和吸入气雾剂CFCs淘汰行业计划的推动下,药用气雾剂用抛射剂的标准制修订工作取得了突破性进展,2013年8月,用于药用非吸入气雾剂的CFCs替代辅料二氧化碳、异丁烷、七氟丙烷、四氟乙烷国家标准发布,为国内药用非吸入气雾剂的CFCs替代产品提供了技术支撑,保证了CFCs向HFCs转换过程中的“有药可用”和替换后的“用药安全”;用于吸入气雾剂的HFA-134a国家标准,目前也正在制定中,但是,仍然存在标准制定相对滞后,一些产品标准缺失、限度较为宽泛的问题。随着近年来哮喘和慢性阻塞性肺病患者的增加,药用气雾剂的用量也在逐年增加,为保证药用气雾剂的安全性和有效性,应尽快制定相关抛射剂的质量标准和抛射剂类辅料的指导原则。
此外,在国际环境保护形势的推动下,绿色抛射剂的开发一直在进行中,碳氢化合物类抛射剂由于属于挥发性有机物(VOC),且易燃易爆被一些国家禁止使用,压缩气体类抛射剂由于不能产生恒定的压力而应用受限。2005年生效的《京都议定书》将二氧化碳、甲烷、氧化亚氮、氢氟烷烃类物质、全氟化碳、六氟化硫列为需要控制的6种温室气体;欧盟、美国已经通过颁布规定和法令限制氢氟烷烃类物质的使用,并倡导推广环境友好的自然制剂的应用,《蒙特利尔议定书》也已启动了氢氟烷烃类物质管控的谈判进程,这意味着曾经广泛替代CFCs的氢氟烷烃类物质(HFA-134a和HFA-227ea)将面临绿色贸易壁垒和再次替代的命运[28]。目前,一些新型的抛射剂如1, 3, 3, 3-四氟丙烯(HFO-1234ze)、二氟乙烷(HFC-152a)等在药用气雾剂中的应用正在研究中,为在国际谈判中争取主动地位,我们应该关注国内外新型抛射剂的开发,根据我国国情适当推广并及时开展其质量标准的制修订工作,相信随着国内药用气雾剂行业的发展,我国在药用气雾剂辅料抛射剂的质量标准研究方面也会更加全面、更加深入。
参考文献
[1] 中华人民共和国药典: 四部[S]. 2015: 17-18, 256-257.
[2] 国家食品药品监督管理局.国食药监注[2011]185号国家食品药品监督管理局关于印发已上市吸入气雾剂变更抛射剂研究技术要求的通知[S]. 2011.
[3] 翁琳琳, 唐黎明, 陈桂良. 吸入给药制剂的质量控制及其安全性研究进展[J]. 药物分析杂志, 2013, 33(6): 724-727.
[4] 国家食品药品监督管理总局.食药监总局回应问题眼用气体: 不符合标准已停产[EB/OL]. (2016-4-14)[2018-12-27]. http://samr.cfda.gov.cn/WS01/CL1747/151409.html.
[5] 龙晓英. 药剂学笔记[M]. 北京: 科学出版社, 2010: 156.
[6] First Supplement to USP 41-NF 36[S]. 2018: Excipients 8481.
[7] EUROPEAN PHARMACOPOEIA 9.6[S]. 2018: 5914.
[8] 金方, 侯曙光, 魏农农. 氟利昂替代后吸入气雾剂(MDIs)的研究要求和进展Ⅰ:欧美抛射剂替代研发和质量控制[J]. 中国医药工业杂志, 2009, 40(7): 543-548. DOI:10.3969/j.issn.1001-8255.2009.07.020
[9] 国家食品药品监督管理总局, 中华人民共和国环境保护部. 2013年第9号关于禁止使用全氯氟烃类物质生产药用非吸入气雾剂的公告[EB/OL].(2013-04-26)[2018-11-6]. http://samr.cfda.gov.cn/WS01/CL0087/80445.html.
[10] USP 41-NF 36[S]. 2018: 705-706, 2960-2961, 5228, 5401, 5537, 5462, 5643, 6356-6354.
[11] USP 40-NF 35[S]. 2017: 7636-7637.
[12] U.S. Food and Drug Administration. Orange Book: Approved Drug Products with Therapeutic Equivalence Evaluations[EB/OL].[2018-06-12]. https://www.accessdata.fda.gov/scripts/cder/ob/search_product.cfm.
[13] 中国国家标准化管理委员会. GB/T 22026-2008气雾剂级丙烷(A-108)[EB/OL].(2008-06-19)[2018-11-09]. http://c.gb688.cn/bzgk/gb/showGb?type=online&hcno=F02A7912341B74B2F4B7E7C06299F5A5.
[14] 中国国家标准化管理委员会. GB/T 22024-2008气雾剂级正丁烷(A-17)[EB/OL].(2008-06-19)[2018-11-09]. http://c.gb688.cn/bzgk/gb/showGb?type=online&hcno=44E5539A7E65332C9AB735E3EE288E0F.
[15] 中国国家标准化管理委员会. GB/T 22025-2008气雾剂级异丁烷(A-31)[EB/OL].(2008-06-19)[2018-11-09]. http://c.gb688.cn/bzgk/gb/showGb?type=online&hcno=29978E32EC1722620FC5565AB6EB0E55.
[16] 国家食品药品监督管理总局.国家药品标准制定件: 批件号FGB2013-001-004[S]. 2013.
[17] EUROPEAN PHARMACOPOEIA 9.0[S]. 2016: 1951-1952, 3179-3183, 3165, 3166-3167.
[18] U.S. Food and Drug Administration. Metered Dose Inhaler (MDI)and Dry Powder Inhaler(DPI)Products-Quality Considerations Guidance for Industry(DRAFT GUIDANCE)[EB/OL]. (2018-04)[2018-06-12]. https://www.fda.gov/downloads/drugs/guidances/ucm070573.pdf.
[19] Handbook of Pharmaceutical Excipients[M]. 6th Edition. London: pharaceutical press, 2009: 733-734.
[20] 李雪梅, 周雪, 侯甲福, 等. 利多卡因氯己定气雾剂抛射剂替代实验[J]. 医药导报, 2010, 11(29): 1477-1478.
[21] 国家药典委员会.关于氮气和二甲醚国家药用辅料标准草案的公示(第二次)[EB/OL].(2019-01-25)[2019-01-31]. http://www.chp.org.cn/view/ff808081687eba33016882d0c5d608d5?a=BZFULIAO.
[22] 马丁代尔大药典: 39版英文版[S]. 2016: 1832.
[23] JAPAN PHARMACOPOEIA: JP ⅩⅦ[S]. 2016: 580, 1316-1319.
[24] 中华人民共和国药典: 二部[S]. 2015: 1134-1135.
[25] 靳贵英. 烷烃类抛射剂质量研究[J]. 中国医药科学, 2016, 6(5): 50-53.
[26] 侯曙光, 魏农农, 金方. 氟利昂替代后吸入气雾剂(MDIs)的研究要求和进展Ⅱ:抛射剂替代的MDIs的技术挑战和工业化生产[J]. 中国医药工业杂志, 2009, 40(8): 622-626. DOI:10.3969/j.issn.1001-8255.2009.08.017
[27] 关皓月, 闫中天, 孙会敏. 1, 1, 1, 2-四氟乙烷国内外质量比对研究[J]. 中国新药杂志, 2015, 24(18): 2153-2156.
[28] 肖学智, 含氢氯氟烃HCFCs替代技术指南[S]. 2016: 29-30.