您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2025-06-09 08:40
一、 泰国医疗器械监管介绍
1. 监管部门
在泰国,医疗器械由泰国食品和药物管理局 (Thai Food and Drug Administration, TFDA) 下属的医疗器械控制司(Medical Device Control Division, MDCD) 监管。
2. 监管法规
Medical Device Act B.E. 2551 (2008)
Medical Device Act (No. 2) B.E. 2562 (2019)
3. 产品风险分类
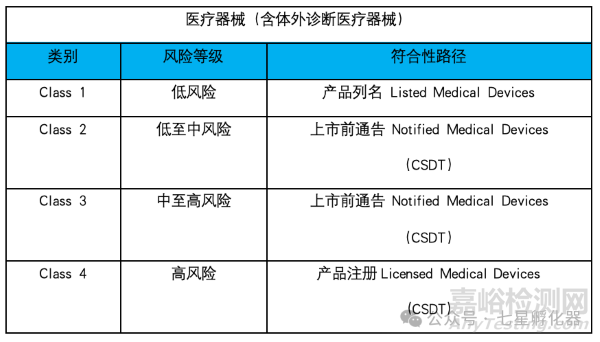
泰国医疗器械风险等级分类严格遵守东盟医疗器械指令AMDD附录3,医疗器械(Non -IVD)和体外诊断(IVD)医疗器械分为两大类:
医疗器械(Non -IVD)按风险由低到高分为四个类别:Class 1, Class 2, Class 3, Class 4
体外诊断(IVD)医疗器械按风险由低到高分为四个类别:Class 1, Class 2, Class 3, Class 4
二、 产品注册介绍
1. 注册路径
在泰国, 根据产品的注册历史,可以有三种注册路径进行选择。
第一种:Full evaluation全面评估
该路径允许无任何国家的注册历史。
第二种:Concise pathway简明路径
该路径旨在加快注册进程并降低评估费用,需要满足的条件为:
(1)风险等级为Class 2~4的医疗器械;
(2)医疗器械必须在参考监管机构:欧盟(EU NB)、加拿大(HC)、日本(MHLW)、澳大利亚(TGA)、美国(FDA)、WHO组织,其中1个监管机构获得注册认证(通过全面评估)并上市一年以上,无任何严重不良事件。
(3)通过该路径提交的医疗器械的商品名称、型号、产品编号、预期用途、适应症、标签,说明书、包装、制造商的名称和地址必须与参考监管机构批准的保持一致。
第三种:Reliance program信赖计划
该路径依赖于新加坡HSA(Health Science Authority)的批准,同样旨在加快注册进程并降低评估费用,需要满足的条件为:
(1)风险等级为Class 2~4的医疗器械;
(2)已经被新加坡HSA批准;
(3)通过该路径提交的医疗器械的商品名称、型号、产品编号、预期用途、适应症、标签,说明书、包装、制造商的名称和地址必须与新加坡HSA批准的保持一致。
2. 注册流程
· 确定产品是否属于泰国法规规定的医疗器械,确定产品风险分类及注册路径
· 指定泰国当地代理人
· 准备注册文件
· 提交注册文件;由医疗器械控制司(MDCD)录入至数据库并进行审核
· 审核通过后获取医疗器械批准证书后,合法进入泰国市场销售
3. 注册文件
1类产品列名文件清单如下:
· 制造或进口医疗器械产品的经营许可证(Establishment Licensing);
· 制造商出具的授权信LoA,授权进口商的注册提交;
· 医疗器械名称和产品描述、标签、规格和制造商或产品所有人信息以及产品说明书;
· 国外注册记录;
· 需要灭菌的产品,应提供灭菌证明;
· 生产或进口具有测量功能的医疗器械,说明检测或校准检测情况的文件;
· 制造商或产品所有人签发的合格声明;
· 产品所有人出具的进口商授权书Power of attorney;
2类、3类和4类器械需要按照东盟 CSDT 格式提交技术档案,文件清单如下:
· 制造或进口医疗器械的经营许可证(Establishment Licensing);
· 制造商出具的授权信LoA,授权进口商的注册提交;
· 医疗器械名称和产品描述、标签、产品说明书、执行摘要和制造商或产品所有人信息;
· 医疗器械安全和性能基本原则总结;
· 设计开发和验证总结;
· 风险分析报告;
· 说明产品使用后废弃物的销毁、拆除或处置方法的文件;
· 质量体系证书 (如ISO 13485)
· 制造商或产品所有人提供的关于产品预期用途、标识、包装、标签和说明书的声明信;
· 符合性声明;
· 产品上市情况描述;
· 安全有效声明文件;
· TFDA认可的国外注册证明
· 产品所有人出具的进口商授权书Power of attorney;
4. 注册文件语言要求
【供专业人士使用】:英语
【供非专业人士使用】:标签、说明书,提供英文和泰语版;除标签、说明书之外的其他资料,可以提供英文版。
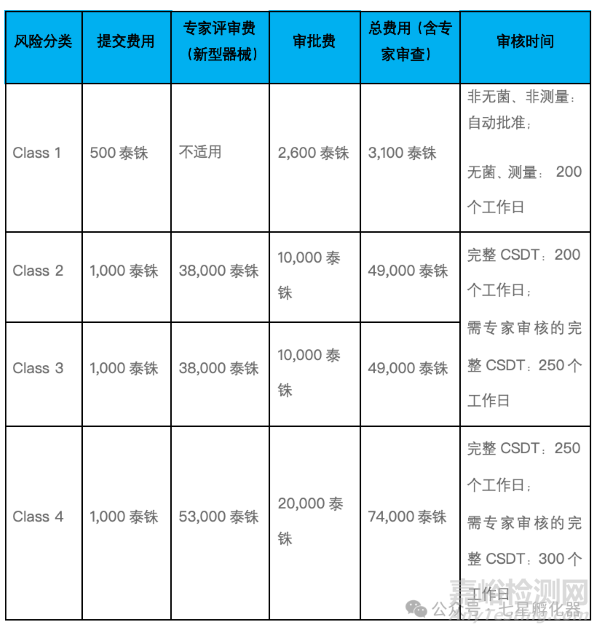
5. 注册费用和审核周期
三、 问答
Q:是否需要原产国批准?
A: 不需要。
Q:是否需要ISO 13485证书?
A: 2-4 类器械都需要 ISO 13485 证书。
Q:是否需要当地代表?
A:进入泰国市场需要有当地代表。当地代表持证并且必须 参与进口过程。

来源:七星孵化器


