您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2024-05-18 21:27
近日,美敦力Medtronic(NYSE:MDT)全新一代 IN.PACT™ Admiral™ XL 药物涂层球囊(长球囊:200mm 和 250mm) 获国家药品监督管理局(NMPA)批准国内上市。
该产品为双腔药物涂层外周球囊扩张导管适用于对股浅动脉(SFA)和腘动脉近端(PPA)的外周动脉阻塞性疾病进行经皮腔内血管成形术(PTA)治疗。
200mm 和 250mm 的药物涂层球囊 IN.PACT Admiral 在 2018 年 5 月获得 FDA 批准。它是第一个获得美国 FDA 批准的 DCB,用于治疗支架内再狭窄和长达 360 毫米的病变,并于2021年获得 CE 批准。
IN.PACT Admiral 药物涂层球囊

▲源自公司官网
IN.PACT Admiral 适用于外周动脉阻塞性疾病进行经皮腔内血管成形术(PTA)治疗,包括支架内再狭窄(ISR),以及天然或动静脉透析瘘的阻塞性病变。
IN.PACT Admiral 具有多达7种不同长度的球囊(从40mm到250mm),使其能够适用于不同类型的外周动脉阻塞性疾病。
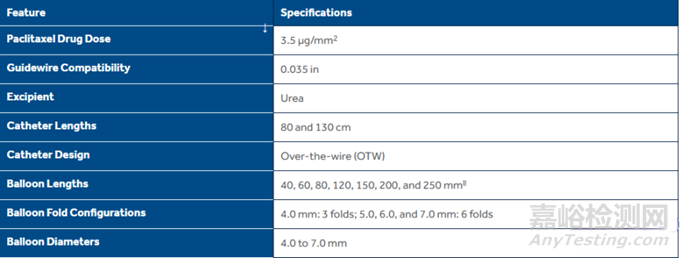
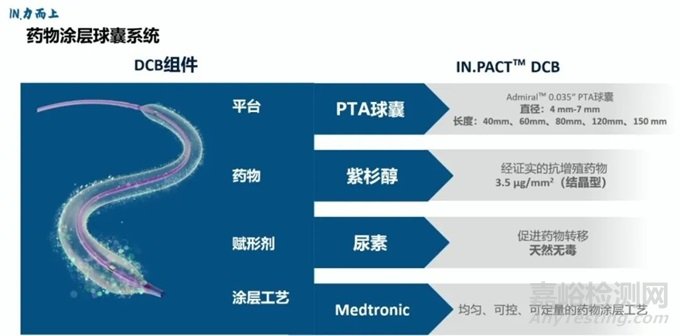
IN.PACT Admira之所拥有领先于对手的药物释放技术,是由于其采用Admiral 0.035 PTA 球囊作为平台,药物浓度为 3.5ug/mm² 的结晶型紫杉醇,赋形剂为亲水性的尿素,涂层工艺为美敦力均匀、可控、可定量的药物涂层工艺。
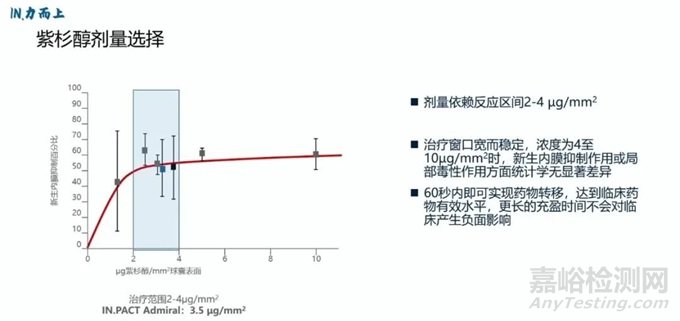
紫杉醇能够抑制血管平滑肌细胞增殖、迁移和表型转换,通常其使用剂量越大,对内膜增生的抑制作用越显著。但是动物试验证明,紫杉醇浓度在 2-4ug/mm² 时对内膜增生的抑制效果最为理想,浓度过低时治疗效果不显著,浓度超过 4ug/mm² 时抑制内膜增生效果与 2-4ug/mm² 无异。因此,美敦力通过科学方式确定紫杉醇浓度为3.5ug/mm²。
IN.PACT Admira 采用尿素作为赋形剂,使其具有多种优势:
(1)尿素为亲水性,有利于药物在病变区域的释放,比疏水性的赋形剂组织浓度更高;
(2)尿素较其他亲水涂层在输送过程中丢失率更低,在组织中转运效率更高;
(3)尿素为人体的天然分子,毒性低,无过敏反应,且球囊表面最大尿素剂量仅为人体一天产生量的1/20000,剂量极小,从而保证 IN.PACT Admiral 药物持续释放长达180天。
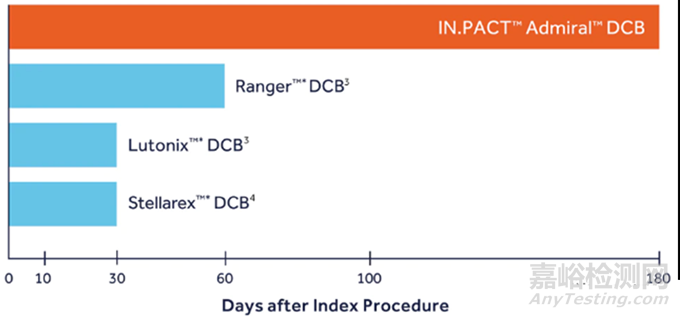
临床试验结果
IN.PACT Admiral 已经在多个临床研究中证明其维持血管的长期通畅性和安全性。超过3500名患者参与了21项临床研究,在全球治疗了50多万名患者。
在一项 IN. PACT SFA 研究(来自欧美多中心的前瞻性、随机、单盲研究)中,对受试者继续进行长达5年的随访,从而获得DCB安全性与有效性的实际情况。
DCB 组与 PTA 组,3年一期通畅率分别为 69.5% 和 45.1% ,5年无靶病变血运重建(CD-TLR)分别为74.5% 和 65.3%,首次 CD-TLR 天数分别为 807.5±433.9 天和 474.9±484.3 天。可见 DCB 组在疗效上的优势。
安全性方面,两组患者全因死亡率、血栓形成和目标肢体大截肢等方面都无显著差异。
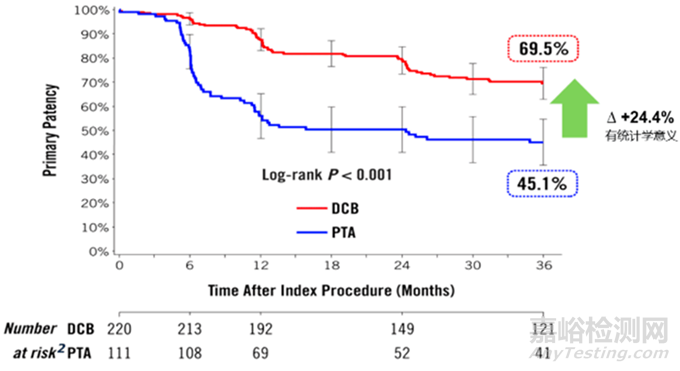
▲三年一期通畅率
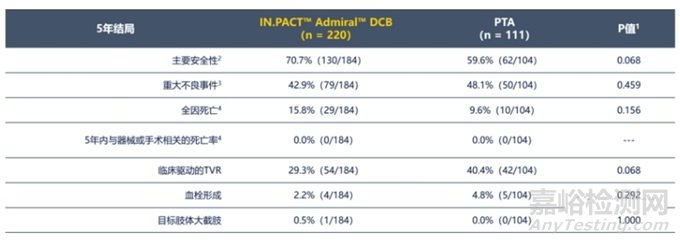
▲5年安全性结局
药物涂层球囊市场概况
裸金属支架(BMS)的出现在一定程度上解决了球囊扩张后可能会面临的血管壁夹层、血管急性闭塞和血管弹性回缩等问题,但却带来了另一个严峻的挑战,即支架内再狭窄。金属支架对血管内膜的持续性刺激,可导致血管内膜增生过度,引起支架内再狭窄(ISR),发生率可达30%。
药物涂层球囊扩张术使药物作用于血管内壁,维持血管通畅效果更佳且不留异物在血管内,在血管内再狭窄ISR、小血管、分叉病变有明显优势,原发病变的扩展也不断探索验证。
随着近年来“介入无植入”理念的推广,药物涂层球囊使用量快速增长。根据弗若斯特沙利文预测数据,药物涂层球囊首次在中国获批用于冠状动脉疾病的治疗后,使用量从 2016 年的 7500 个大幅增长至 2021 年的 29.0 万个。预计 2025 年市场规模将进一步攀升至 100.0 万个,2030 年预计将达到 204.2 万个。
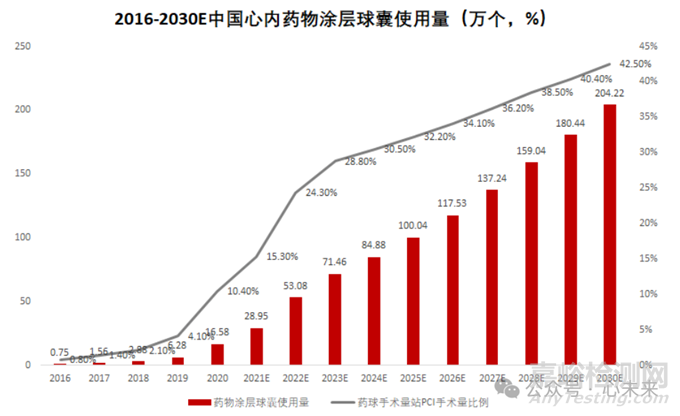
▲源于弗若斯特沙利文
根据弗若斯特沙利文预测数据,国内冠脉药物涂层球囊的市场规模从 2016 年的 1.35 亿元大幅增长至 2021 年的 20.09 亿元,预计 2025 年市场规模将进一步攀升至 43.86 亿元,2030 年预计将达到 59.33 亿元。
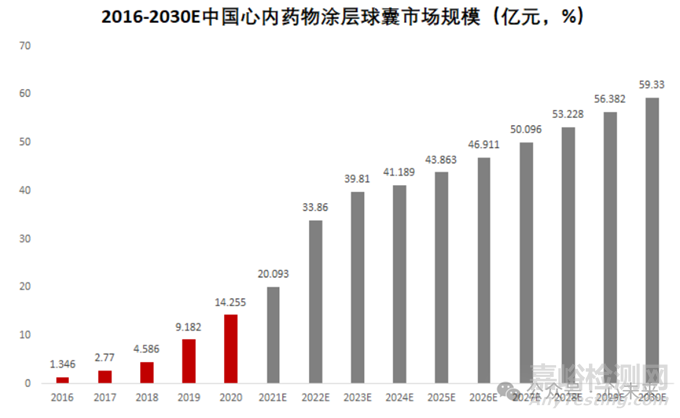
▲源于弗若斯特沙利文
冠脉药物涂层球囊是高端第三类医疗器械,产品具有高精密技术,进入壁垒较高的特点。我国药物球囊行业发展起步较晚,发展时间较短,国内市场由数家公司主导,仍有较大的进步空间。
德国贝朗的 SeQuent Please 是我国最早上市的药物涂层球囊,其适应症为冠状动脉支架内再狭窄治疗。垠艺生物的轻舟®药物洗脱球囊于 2017 年获原国家食品药品监督管理总局(CFDA)优先审批上市,是国际首个适用于原发冠脉分叉病变的产品,也是国内首个取得注册证的产品。
随着临床应用研究逐步开展,参与者陆续取得冠脉药物球囊产品注册证,如上海申淇、乐普医疗、凯德诺(远大医药)、赢生医疗、巴泰医疗、鼎科医疗。未来随着更多竞争对手和竞品进入市场,市场竞争将加剧,但竞品的进入也将进一步加强行业的国内市场教育,促进产品市场渗透率提高。
其中,垠艺生物的轻舟®药物洗脱球囊具有出色的通过性及输送性、优异的药物涂层品质,已在多家知名心血管医院及国内逾千家医院进行临床应用,上市后销量增长较快,打破了德国贝朗的市场垄断。
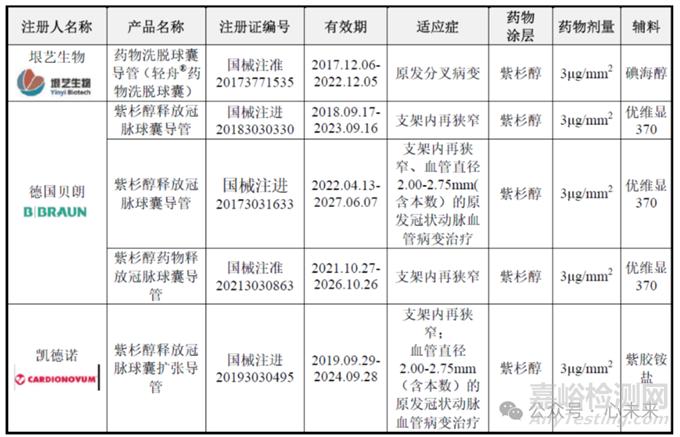
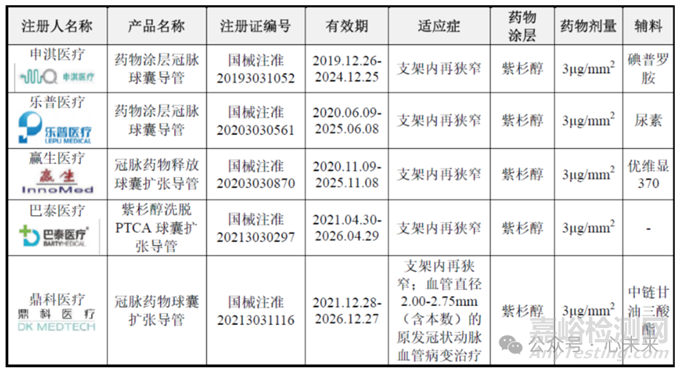
▲冠脉药物球囊竞品信息对比(源于垠艺生物招股说明书)
关于美敦力

美敦力 (Medtronic,NYSE:MDT) 成立于1949年,总部位于美国明尼苏达州明尼阿波利斯市,是全球领先的医疗科技公司,拥有超过95000名员工。
美敦力的创新解决方案已拓展至70余种重点疾病领域,致力于为慢性疾病患者提供终身的治疗方案,每一秒钟,全球就有2位患者受益于美敦力的医疗技术或疗法。
美敦力主要业务有心血管、医疗外科、神经科学和糖尿病业务四块,其中心血管占比最高。美敦力卖什么?心血管产品线超全盘点
以2023年财报为例,公司整体收入312.27亿美元,在全球医疗器械企业营收中排名第一。其中心血管业务营收115.73亿美元,占比37.06%,包括心脏节律和心力衰竭(CRHF)、结构性心脏和主动脉(SHA)以及冠状动脉和外周血管(CPV)三个部门。
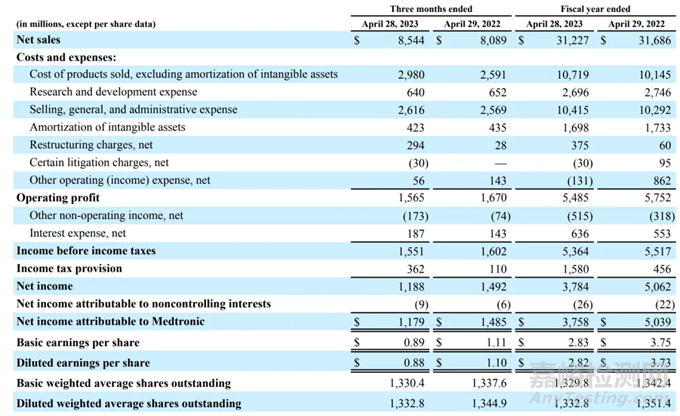
▲2023年财报(源自公司官网)

来源:心未来


