今日头条
上海标新分子胶降解剂获批临床。上科大孵化企业标新生物开发的1类化药GT919胶囊获国家药监局临床试验默示许可。GT919是标新生物的首个分子胶降解剂产品,拟开发用于恶性血液肿瘤的治疗,旨在解决目前临床上来那度胺类药物的耐药性及安全性问题。标新生物于2020年成立,并与上科大签订超亿元合同金额的专利独家许可协议。此次也是上科大成果转化项目获得的首个中国临床批件。
国内药讯
1.大冢「布瑞哌唑」在华报产。大冢制药5.1类新药布瑞哌唑片(brexpiprazole)的上市申请获CDE受理。Brexpiprazole是一款非典型抗精神病药物,由灵北制药和大冢制药联合开发,于2015年7月首次获FDA批准上市,商品名为Rexulti,用于治疗精神分裂症和作为抗抑郁药物的辅助疗法治疗重度抑郁症(MDD)。Rexulti目前还在治疗阿尔茨海默病患者激越的Ⅲ期临床中获得积极结果,预计即将向FDA递交补充新药申请(sNDA)。
2.信达CLDN18.2靶向ADC获批临床。信达生物靶向CLDN18.2(claudin18.2)的ADC药物IBI343获国家药监局临床默示许可,拟用于治疗晚期恶性实体瘤。IBI343可通过与表达CLDN18.2的肿瘤细胞结合后,发生CLDN18.2依赖性ADC内化,并释放毒素药物引起DNA损伤,导致肿瘤细胞凋亡。此外,IBI343也具有旁观者效应,也可通过质膜扩散并杀死相邻的肿瘤细胞。这是信达获批进入临床阶段的首款ADC。
3.石药TNFR2单抗在美获批临床。FDA批准石药集团附属公司NovaRock Biotherapeutics开发的抗肿瘤坏死因子2型受体(TNFR2)单抗药物NBL-020的新药临床试验申请,拟用于晚期实体瘤的治疗。TNFR2属于肿瘤坏死因子受体(TNFR)超家族,通过多种信号通路维持肿瘤细胞免疫抑制的微环境,直接或间接促进肿瘤进展。临床前研究显示,NBL-020单药或与PD-1抗体联用,均具有积极的抗肿瘤活性和良好的安全性。
4.德睿智药GLP-1R激动剂获批减肥临床。德睿智药宣布,FDA已批准其专有AI制药平台Molecule Pro开发的新型非竞争性GLP-1R激动剂小分子药物MDR-001临床许可,拟开展用于肥胖适应症的临床试验。在早期的糖尿病合并肥胖猴的药效模型中,长期给药结果显示MDR-001能有效降糖和降体重,还能使糖化血红蛋白(HbA1C)恢复到健康猴水平,并显示出具有治愈早期糖尿病的潜力。
5.科伦7个在研ADC项目向默沙东授权。科伦药业控股子公司科伦博泰与默沙东就前者管线中7种临床前期ADC候选药物签署独家许可和合作协议。根据协议,默沙东将获得7款ADC候选药物在全球范围内或在中国大陆、香港和澳门以外地区进行研究、开发、生产制造与商业化授权;科伦博泰将收到一次性合计1.75亿美元不可退还的首付款,预计不超过93亿美元的里程碑潜在付款,以及产品的销售分成。
国际药讯
1.吉利德长效HIV新药获FDA批准上市。FDA批准吉利德长效HIV衣壳抑制剂Sunlenca(lenacapavir)注射液和片剂上市,用于联合其他抗逆转录病毒药物治疗多重耐药人类免疫缺陷病毒(HIV)感染的成人患者。Sunlenca也是首个可为多重耐药HIV患者提供一年两次给药的HIV衣壳抑制剂。在Ⅱ/Ⅲ期临床CAPELLA中,Sunlenca联合治疗在第52周时,可使83%的患者达到病毒载量检测不到的标准(<50 拷贝/毫升)。
2.罗氏CD20/CD3双抗获FDA批准上市。罗氏旗下基因泰克开发的CD20/CD3双特异性抗体Lunsumio获FDA批准上市,用于治疗至少两线系统治疗后复发或难治性滤泡性淋巴瘤(FL)患者。在一项Ⅰ/Ⅱ期临床GO2978中,中位随访为18.3个月时,中位缓解持续时间为22.8个月,完全缓解率为60%,客观缓解率为80%。Lunsumio是全球首个CD20/CD3双抗,为这类患者提供一种无化疗、现货型的新免疫治疗选择。
3.KRAS抑制剂获突破性疗法认定。Mirati公司KRAS G12C抑制剂Krazati(adagrasib)获FDA授予突破性疗法认定,与EGFR抑制剂cetuximab联用,治疗KRAS G12C突变的晚期结直肠癌患者。在KRYSTAL-1试验中,Krazati联合cetuximab达到46%的客观缓解率(ORR,95% CI:28-66),其中位缓解持续时间(DOR)为7.6个月(95% CI:5.7-尚无法评估),中位无进展生存期(PFS)为6.9个月(95% CI:5.4-8.1)。再鼎医药拥有adagrasib在大中华区的开发权益。
4.Alnylam糖尿病领域RNAi疗法报IND。Alnylam公司靶向酮己糖激酶(KHK)的皮下给药RNAi疗法ALN-KHK,已向加拿大卫生部提交了针对2型糖尿病(T2DM)适应症的I/II期临床试验申请。研究表明KHK介导的果糖代谢有助于肝脏脂肪生成和胰岛素抵抗。Alnylam计划于明年初开始对健康超重/肥胖志愿者以及患有2型糖尿病的肥胖患者进行I/II期研究,并预计在2023年底报告首个人体数据。
5.AAK1抑制剂治疗神经痛II期临床失败。Lexicon公司口服小分子衔接子相关蛋白激酶-1(AAK1)抑制剂LX9211用于减轻带状疱疹后神经痛的II期概念性验证研究(RELIEF-PHN-1)未达到主要终点。数据显示,LX9211(200mg)组患者的ADPS(每日疼痛评分)相比基线降低2.42分,而安慰剂组则降低1.62分,不具备显著性差异(P=0.12)。临床中的不良事件(AE)与既往研究一致。Lexicon表示,研究失败的原因是剂量选择不当。
6.德国默克与Mersana联合开发新型ADC。德国默克子公司与Mersana公司达成合作和许可协议,利用后者专有的ADC开发技术平台,合作开发最多两个靶标的新型Immunosynthen ADC候选疗法。Immunosynthen ADC能在肿瘤驻留免疫细胞和抗原表达细胞中局部激活STING(干扰素基因刺激蛋白)信号,释放先天免疫刺激的抗肿瘤活性;其激活强度比游离激动剂高约40-100倍。今年,Mersana先后与杨森和GSK达成合作,总金额超23.6亿美元。
医药热点
1.牡丹江医学院将更名为牡丹江医科大学。12月23日,黑龙江省人民政府办公厅发布《黑龙江省“十四五”高等学校设置规划》。其中提出“十四五”期间,黑龙江省拟规划4个高等学校设置项目,其中更名大学项目2项,包括牡丹江医学院更名为牡丹江医科大学。更名大学,将更有利于增强区域医学科技创新能力,提升区域医疗卫生水平,推动学校事业高质量发展。
2.首个“健康上海行动院士科普基地”成立。12月23日,上海市五官科医院挂牌首批“健康上海行动院士科普基地”,上海市耳鼻喉健康促进中心成立。该中心由王正敏等院士牵头,将以构建全生命周期五官健康管理及科普教育体系,针对重点人群开展重点五官疾病的预防监测工作,大力推进五官疾病高质量医教研协同发展。
3.卫健委不再发布每日疫情信息。12月25日,国家卫健委官网发布消息,宣布从即日起,不再发布每日疫情信息,将由中国疾控中心发布相关疫情信息,供参考和研究使用。对此,南方医科大学公共卫生学院生物安全研究中心主任赵卫表示,此举不仅表示疫情信息已经失去了每日发布的必要性,同样也能让有关部门将更多精力投入到临床救治等关键环节。
评审动态
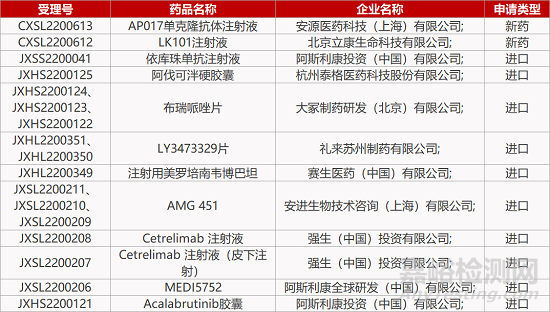
1. CDE新药受理情况(12月24日)
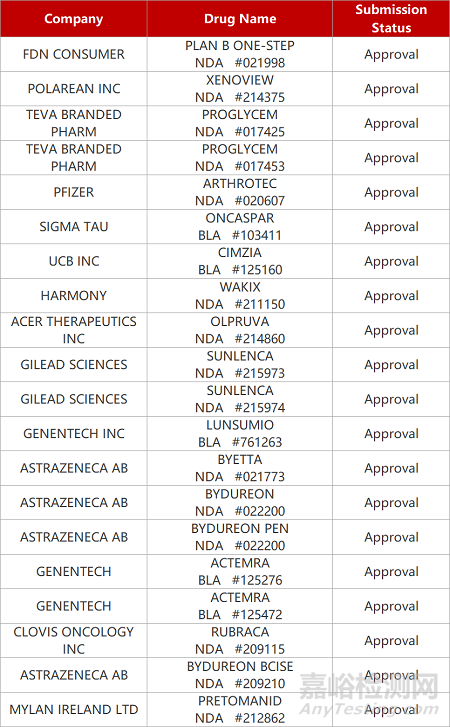
2. FDA新药获批情况(北美12月23日)