您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-05-21 10:05
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
「 本文共:15条资讯,阅读时长约:3分钟 」
今日头条
普克鲁胺治疗新冠在美获批新临床。开拓药业宣布新一代雄激素受体(AR)拮抗剂普克鲁胺用于治疗COVID-19住院患者的III期临床已获得FDA的批准。这是普克鲁胺COVID-19项目在美国获批的第二项III期临床,这项试验将同时招募男性和女性COVID-19住院患者。值得一提的是,今年4月,开拓药业在美国开展的普克鲁胺用于治疗轻中症新冠男性患者的III期临床已正式启动;目前FDA已批准在该项研究中拓展纳入女性患者。
国内药讯
1.百济神州泽布替尼在美申报新适应症。FDA受理百济神州BTK抑制剂泽布替尼用于治疗先前接受过至少一项CD20导向疗法的成年边缘区淋巴瘤(MZL)患者的新适应症上市申请,并授予其优先审评资格,PDUFA日期为2021年9月19日。一项公布于ASH2020会议上的Ⅱ期MAGNOLIA临床结果显示,泽布替尼在这类患者中达到74.2%的总缓解率以及将近90%的临床受益率。这是该公司针对MZL提交的首项上市申请。
2.恒瑞SHR0302片获批新临床。恒瑞医药1类新药SHR0302片获国家药监局两项临床试验默示许可,拟临床开发用于银屑病关节炎的治疗。SHR0302是一款小分子JAK1激酶选择性抑制剂,恒瑞正在中美同步临床开发。目前,SHR0302已在国内开展了针对类风湿性关节炎、溃疡性结肠炎、克罗恩病等多项临床研究。SHR0302用于12岁及以上青少年和成人中重度特应性皮炎适应症已获CDE纳入突破性疗法认定。
3.阿诺医药PD-L1抑制剂在美报IND。阿诺医药宣布其原创新药PD-L1抑制剂AN4005已向FDA递交了临床试验申请(IND)。临床前研究表明,AN4005具备良好的体外活性和体内抗肿瘤功效,以及良好的成药性和安全性。作为针对多种实体瘤的小分子药物,AN4005在单药治疗以及组合用药方面都有着巨大的潜力。该公司计划在美国开展评估AN4005的安全性和药代动力学特征的Ⅰ期临床。
4.Epizyme公司EZH2抑制剂品种在华报IND。Epizyme公司“first in class”新药Tazemetostat的临床试验申请获CDE受理。Tazemetostat是FDA批准的首款EZH2抑制剂,已获批用于治疗不适合完全切除的转移性/局部晚期上皮样肉瘤(ES)患者;以及既往经过至少二线系统治疗EZH2+复发或难治性(r/r)滤泡性淋巴瘤(FL)成人患者或无其他替代疗法的r/r FL成人患者。在国内,恒瑞EZH2抑制剂SHR2554目前处于I期临床阶段、上海海和公司的EZH1/EZH2抑制剂HH2853已批准临床。
5.映恩生物完成9000万美元B轮融资。映恩生物宣布完成9000万美元的B轮融资。本轮融资由礼来亚洲基金领投,楹联健康基金、华盖资本等国内知名基金参投,以及A轮战略投资者药明生物产业基金继续加持。映恩生物是一家成立于2020年1月的创新生物制药公司。该公司目前已拥有包含近10款“best-in-class”及“first-in-class”的双抗及抗体偶联药物(ADC)。本轮融资将用于该公司在全球范围内推进产品管线的临床前研究、临床开发及产品授权引进。
国际药讯
1.BTI公司右美托咪定在美报NDA。FDA受理BTI公司右美托咪定舌下膜剂BXCL501的新药申请,用于与精神分裂症及双相情感障碍I型和II型相关激越(agitation)的急性治疗。在两项分别评估BXCL501用于精神分裂症及双相情感障碍I型和II型相关激越的急性治疗的Ⅲ期研究(SERENITY I和SERENITY II)中,BXCL501耐受性良好,在120mcg和180mcg剂量下均达到主要和次要终点。该新药此前已获FDA授予突破性药物资格和快速通道资格。
2.罗氏/再生元COVID-19抗体鸡尾酒疗效积极。罗氏与再生元合作开发的抗体鸡尾酒疗法REGEN-COV(casirivimab和imdevimab)在ATS 2021上公布关键Ⅲ期试验的详细结果。与安慰剂相比,REGEN-COV将COVID-19非住院患者的住院或死亡风险显著降低70%、症状消除时间缩短4天,同时还显著降低了病毒载量。该研究中,2种剂量(1200mg和2400mg)的疗效相似。目前,FDA正在审查在紧急使用授权(EUA)中增加1200mg剂量的申请。
3.BioMarin公司血友病基因疗法长期疗效积极。BioMarin公司公布基因疗法valoctocogene roxaparvovec(valrox,BMN270)单次输注治疗重度A型血友病的Ⅰ/Ⅱ期研究最新积极结果。对6e13 vg/kg队列和4e13 vg/kg队列分别进行的5年和4年治疗后随访显示,2个队列患者均保持不使用预防性因子VIII治疗。6e13 vg/kg队列平均累积年化出血率(ABR)仍低于1,并大大低于治疗前的基线水平;与输注前相比,该队列第5年的平均ABR为0.7,5年内ABR降低95%,因子VIII使用减少96%。4e13 vg/kg队列第4年的平均ABR为1.7,与输注前相比,4年内ABR降低92%,因子VIII使用减少95%。
4.阿斯利康哮喘新药长期疗效积极。阿斯利康在ATS2021年会上公布抗炎药Fasenra治疗哮喘的Ⅲ期临床MELTEMI开放标签扩展试验积极数据。分析显示,Fasenra(benralizumab)在长达5年的时间内耐受性良好,长期安全性与之前在严重哮喘成人患者中开展的Ⅲ期试验一致。在开放标签期内,每年至少有75%接受Fasenra治疗的血液嗜酸性粒细胞水平升高的患者没有经历哮喘加重。在试验的最后一年,87%的患者没有出现哮喘加重。
5.再生元新型降脂药疗效积极。再生元(Regeneron)在ACC.2021年会上公布新型降脂药物Evkeeza(evinacumab-dgnb)用于辅助治疗重度高甘油三脂血症患者的Ⅱ期临床积极数据。数据显示,在标准降脂疗法基础上,对于脂蛋白脂肪酶(LPL)通路基因有双等位基因功能缺失突变的患者,Evkeeza治疗基本上没有益处。而在LPL通路基因中有单个突变或无突变的患者中,Evkeeza治疗将甘油三酯水平显著降低。
6.Immunocore公司创新TCR疗法上临床。Immunocore公司创新双特异性TCR疗法IMC-I109V在治疗慢性乙肝(CHB)的临床试验中完成首例患者给药。IMC-I109V通过激活T细胞,特异性消灭受到乙肝病毒(HBV)感染,表达乙肝表面抗原(HBsAg)的肝细胞,具有慢性HBV感染者的功能性治愈潜力。在临床前研究中,IMC-I109V已表现出良好的活性,能够将T细胞募集到被HBV感染的肝细胞附近,并且激活T细胞杀伤受到感染的肝细胞。
医药热点
1.英国报告近3000例新冠印度突变株感染病例。当地时间19日,英国报告最早在印度发现的变异新冠病毒感染病例数增至2967例。英国卫生大臣汉考克呼吁英国民众应尽快接种新冠疫苗。英国的大规模病毒检测将扩展至6个新的病例集中地区。这些地区将通过“一个非常敏感的生物安全监视系统”监控民众的出行方式,以及对英国70%地区的废水进行检测分析,旨在阻止变异病毒的扩散。
2.卫生健康领域拟全面实施预算绩效管理。国家卫健委、财政部、国家中医药管理局日前联合印发《卫生健康领域全面实施预算绩效管理实施方案》,提出到2022年年底,全国各级卫生健康及中医药行政部门、医疗卫生机构基本建成全方位、全过程、全覆盖的预算绩效管理体系。《方案》明确,各级各单位编制预算时要分解细化各项工作要求,设置部门和单位整体绩效目标及项目绩效目标;未按要求设定绩效目标的,不予安排预算。
3.中国加入WHO国际癌症研究机构。2021年5月17日—18日,世卫组织国际癌症研究机构(IARC)第63届理事会召开,IARC理事会一致通过中国加入国际癌症研究机构的申请。国家癌症研究中心主任赫捷院士当选IARC科学理事会成员。IARC于1965年根据世卫大会的决议成立,是世卫组织的癌症研究专门机构。中国是IARC第27个成员国。
审评动向
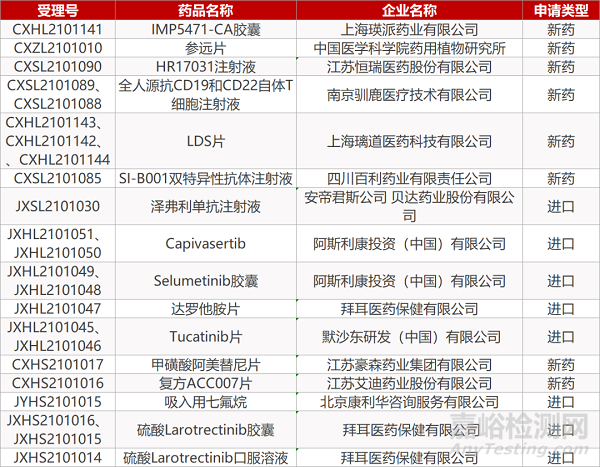
上海瑛派的IMP5471-CA胶囊、中国医学科学院药用植物研究所的参远片、江苏恒瑞的HR17031注射液、南京驯鹿的全人源抗CD19和CD22自体T细胞注射液(2个规格)、上海璃道医药的LDS片(3个规格)、四川百利的SI-B001双特异性抗体注射液、安帝君斯公司/贝达药业的泽弗利单抗注射液、阿斯利康的Capivasertib(2个规格)和Selumetinib胶囊(2个规格)、 拜耳的达罗他胺片、 默沙东的Tucatinib片(2个规格)。
2. FDA新药获批情况(北美05月19日)
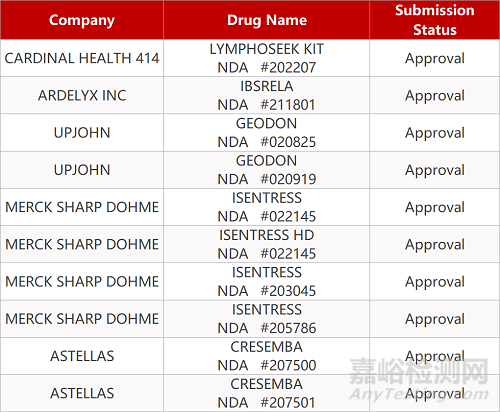

来源:药研发


