您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2021-03-15 07:57
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
正大天晴拿到第二个创新药临床许可。正大天晴「吸入用TQC3721混悬液」的新药临床试验申请获CDE批准,拟临床开发用于治疗哮喘和慢性阻塞性肺病(COPD)。根据公开信息,TQC3721是该公司第2款自主研发的呼吸领域1类新药,其拟用于哮喘、过敏性鼻炎和特应性鼻炎治疗的另一款新药TQC3564目前已完成了Ⅰ期临床。
国内药讯
1.海思科「阿伐那非片」即将获批上市。海思科阿伐那非片3类仿制上市申请已处于“在审批”阶段,有望近期获得NMPA批准上市,成为该品种首仿。阿伐那非片是一种PDE-5抑制剂,最初是由田边三菱制药授权Vivus公司开发,于2012年4月获FDA批准上市,用于治疗男性勃起功能障碍,商品名为Stendra。该品种在国内尚无生产和进口;上海汇伦江苏药业的仿制产品也正处于上市申报阶段。
2.奥赛康「艾曲泊帕乙醇胺片」即将获批上市。奥赛康4类仿制药艾曲泊帕乙醇胺片上市申请已进入 “在审批”阶段,有望近期获批上市。艾曲泊帕乙醇胺片是诺华原研的一种TPO-R激动剂,于2008年11月获FDA批准上市,用于治疗既往对糖皮质激素、免疫球蛋白等治疗反应不佳的慢性免疫性(特发性)血小板减少症(ITP),是首个治疗ITP的口服药物。目前该品种国内仅原研上市销售,商品名为瑞弗兰。
3.大冢阿立哌唑长效注射剂在华申报上市。大冢制药阿立哌唑长效肌内注射剂的上市申请获国家药监局受理。阿立哌唑是全球首个上市的多巴胺(DA)-5羟色胺(5-HT)系统稳定剂,由大冢和灵北制药联合开发,用于精神分裂症的治疗。2013年2月,FDA批准大冢及灵北的阿立哌唑长效针剂(商品名Abilify Maintena)上市,该药也是首个获FDA批准上市的阿立哌唑长效针剂。
4.李氏大药厂抗PD-L1单抗获批Ⅲ期临床。李氏大药厂宣布,其附属公司中国肿瘤医疗有限公司(COF)PD-L1单抗socazolimab(ZKAB001)获CDE批准,拟对结合化疗一线治疗扩散期小细胞肺癌(SCLC)开展一项Ⅲ期临床试验。该项试验将由上海市胸科医院陆舜教授牵头,预期2021年第二季度开展患者招募。值得一提的是,该单抗已于今年1月获CDE纳入突破性治疗品种,拟用于接受过一线含铂方案失败或者不能耐受的复发转移性宫颈癌。
5.恒瑞PD-1联合疗法在美获批Ⅱ期临床。恒瑞医药宣布其PD-1注射用卡瑞利珠单抗与多靶点酪氨酸激酶抑制剂苹果酸法米替尼胶囊的组合疗法,已获FDA批准在美国开展一项Ⅱ期临床,用于实体瘤的治疗。根据公开信息,恒瑞医药已在国内开展多项该组合的临床研究,涉及复发转移性宫颈癌、非小细胞肺癌等适应症,其中用于复发转移性宫颈癌的临床治疗已获CDE纳入突破性疗法认定。
国际药讯
1.礼来RET抑制剂Retsevmo在英国获批。英国药品和保健品管理局批准礼来(Eli Lilly)RET抑制剂Retsevmo(Selpercatinib)有条件上市,用于治疗RET融合阳性的晚期肺癌和甲状腺癌。在一项针对700多例RET驱动型癌症的I/II期LIBRETTO-00研究中,初步分析包括105例先前接受过非小细胞肺癌(NSCLC)治疗的患者,其中64%的患者对治疗有效,平均有效期为17.5个月。在先前治疗的RET突变型MTC患者中,55例患者的初步分析有69.1%的应答率。
2.预防性HAE疗法获法国临时使用许可。法国国家医学和健康产品安全局(ANSM)授予BioCryst公司口服疗法Orladeyo(berotralstat)临时授权使用(cohort ATU)或临时使用许可(ATU),用于在12岁及以上的患者中预防遗传性血管水肿(HAE)发作。Orladeyo是一款血浆激肽释放酶抑制剂, 已在美国和日本获批上市,并正在接受欧盟和英国的监管审评,是首个也是唯一专门设计用于预防12岁及以上的患者HAE发作的口服疗法。
3.礼来阿尔茨海默病抗体疗法公布Ⅱ期详细结果。新英格兰医学(NEJM)期刊日前发布礼来Aβ抗体Donanemab治疗早期阿尔茨海默症的Ⅱ期临床详细数据。该研究达到主要终点,与对照组相比,Donanemab治疗组iADRS(阿尔茨海默病综合评分量表)在76周下降幅度减小3.20,达到统计学意义的显著改善(p=0.04)。次要终点CDR-SB、ADAS0Cog13、ADCS-iADL和MMSE均呈一定程度的改善,但均未达到统计学显著性。
4.欧洲7国禁用阿斯利康疫苗。据法国电视台France24报道,自从奥地利、意大利等国有接种某批次阿斯利康新冠疫苗发生严重凝血反应事件后,已有丹麦、挪威、奥地利等欧洲七国决定在国内部分停止或全部暂停接种阿斯利康COVID-19疫苗。欧洲药品管理局(EMA)在调查报告中表示,截至9日,在超过300万接种该批次的接种者中,出现了20起以上的凝血反应案例,但尚未有确切证据证明接种后出现凝血是否由阿斯利康疫苗造成。目前仍在调查当中。
5.GSK/Vir新冠中和抗体降低住院/死亡风险85%。Vir Biotechnology和葛兰素史克开发的中和抗体VIR-7831(GSK4182136),在治疗高风险COVID-19患者的Ⅲ期临床中获积极中期分析结果。与安慰剂组相比,VIR-7831治疗组29天后患者的住院或死亡风险降低85%(p=0.002)。独立数据监督委员会(IDMC)建议研究提前终止。两家公司计划向FDA递交紧急使用授权(EUA)申请,同时也在其它国家寻求授权。
6.托珠单抗联合瑞德西韦治疗重症COVID-19研究失败。罗氏(Roche)旗下基因泰克评估抗炎药Actemra(tocilizumab,托珠单抗)联合Veklury(remdesivir,瑞德西韦)治疗严重COVID-19患者的III期REMDACTA研究未达主要终点和关键次要终点。与安慰剂+Veklury治疗组相比,Actemra+Veklury治疗组第28天时在住院时间方面没有改善;该研究也没达到关键次要终点指标;临床中,Actemra未发现新的安全信号。全部结果将于同行评议的期刊上发表。
7.基因编辑公司Intellia完成CRISPR体内编辑骨髓细胞。诺奖得主Jennifer Doudna博士创建的基因编辑公司Intellia宣布,在临床前研究中完成了对骨髓和造血干细胞进行体内基因编辑的概念验证。该公司开发的骨髓定向脂质纳米颗粒(LNPs),能够在小鼠模型中成功对骨髓和造血干细胞和祖细胞进行体内基因编辑,而且基因编辑的水平预计能够在镰刀型细胞贫血病(SCD)患者中达到功能性治愈效果。去年11月,该公司基因疗法NTLA-2001已完成Ⅰ期临床的首例患者给药,实现了首次通过全身性给药,在人体内进行基于CRISPR/Cas9技术的基因编辑。
医药热点
1.人大代表建议赋予开业护士处方权。全国人大代表、中南大学湘雅医学院党委书记黎志宏向两会建议,应赋予经规范培训的开业护士一定的处方权,将开业护士工作岗位纳入医疗卫生机构设置标准并规范执业权限。黎志宏表示,全球已有40多个国家开展了开业护士的培养和执业,我国可以借鉴国外经验,大力培养开业护士,以弥补基本医疗卫生服务人力资源的不足。
2.骨科耗材医院采购数据开始填报。国家医保局发布关于《开展部分高值医用耗材医院采购数据填报》的通知,要求各地方医保局及药品和医用耗材集中采购机构,在前期省级平台数据采集的基础上,将部分骨科高值耗材的数据采集工作延伸至医疗机构。按照要求,参加数据填报的医疗机构包括有使用人工关节类、脊柱类、创伤类骨科高值医用耗材的全部公立医院(含军队医院),以及医保定点民营医院。
3.低风险进返京不再需核酸检测阴性证明。为进一步做好常态化疫情防控,北京市日前调整了国内低风险地区人员进返京健康管理措施。自2021年3月16日零时起,国内低风险地区人员进返京不再需要持抵京前7日内核酸检测阴性证明,抵京后不再实行14天健康监测,满7天、满14天不再进行核酸检测,持健康通行码“绿码”,在测温正常且做好个人防护的前提下可自由有序进返京。环京地区通勤人员参照以上措施执行。
4.贝达药业资深副总裁兼CMO辞职。3月12日,贝达药业发布公告,毛力先生因个人原因辞去公司董事、资深副总裁兼首席医学官职位,辞职后将不在公司担任其他职务。目前毛力先生所负责的相关工作已进行交接,该公司副总裁兼临床管理和医学事务负责人季东先生、副总裁李盈女士将分别负责临床研究和战略合作的具体业务。
审评动向
1. CDE新药受理情况(03月14日)
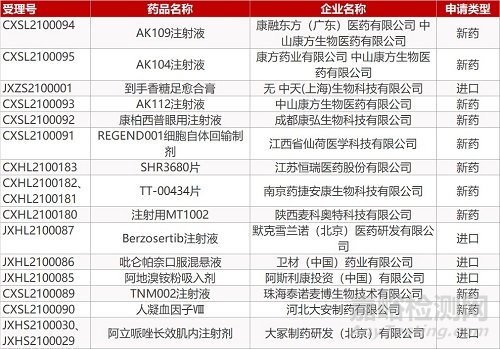
申请临床:
康融东方/中山康方的AK109注射液、康方药业的AK104注射液、中山康方的AK112注射液、成都康弘的康柏西普眼用注射液、仙荷医学科技的REGEND001细胞自体回输制剂、恒瑞医药的SHR3680片、捷安康生的TT-00434片(2个规格)、麦科奥特的注射用MT1002、默克雪兰诺的Berzosertib注射液、卫材(中国)的吡仑帕奈口服混悬液、阿斯利康的阿地溴铵粉吸入剂、泰诺麦博的TNM002注射液、大安制药的人凝血因子Ⅷ。。
申请生产:
中天(上海)生物的到手香糖足愈合膏、大冢制药的阿立哌唑长效肌内注射剂。
2. FDA新药获批情况(北美03月11日)
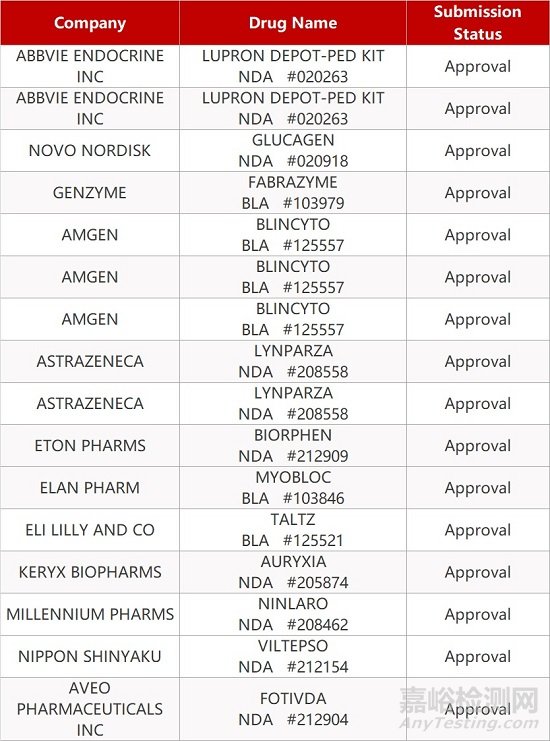
股市资讯
【亿帆医药】公司全资子公司亿帆研究院的注射用重组人生长激素-Fc融合蛋白获得药物临床试验批准通知书。
【景峰医药】控股子公司Praxgen的盐酸林可霉素注射液获得美国ANDA批准文号。
【博腾股份】公司2020年实现营收约20.72亿元,同比增长33.56%;归母净利润约3.24亿元,同比增长74.84%;扣非归母净利润约2.88亿元,同比增长77.82%。

来源:药研发


