您当前的位置:检测资讯 > 法规标准
嘉峪检测网 2020-05-25 16:50
医疗器械临床非劣效试验的研究目的是阐明试验器械不差于或非劣于对照器械,而无需考虑试验器械优于对照器械的情形。其中试验器械的有效性即使比对照器械差但在临床可接受范围内,临床最大允许值即为非劣效界值,前提是试验器械要比对照器械有其他方面的一些优势。
非劣效的结论有两层含义:试验器械的有效性优于安慰剂(间接推论试验器械的有效性);试验器械的有效性若是比对照器械差,其差值也是在临床可接受的范围内。
1.非劣效试验设计:
1.1 使用单纯的阳性对照的非劣效试验:医疗器械有广泛接受的阳性对照并且既往研究可以确定阳性对照的有效性以及稳定性;不适合使用安慰剂对照的试验以及罕见病的研究等情况下。
1.2 采用三臂非劣效试验,既有阳性对照,又有安慰剂对照:由于医疗条件的变化,无法保证阳性对照的有效性以及稳定性情况下。
2.非劣效界值的确定:ICH El0中建议非劣效界值需要在统计学和临床上共同确定且相对保守,以保证通常非劣效界值应不大于历史研究中对照器械与安慰剂的优效性试验中所观察的有效性差异。
3.统计假设
对于不同度量和指标类型,非劣效试验的原假设(H0)和备择假设(H1)的表述有所不同,见下表。其中,Δ为非劣效界值,绝对度量指标包括均值差和率差等,相对度量指标包括率比、风险比、比值比等,高优指标是其值越大表明有效性越好的指标,低优指标是其值越小表明有效性越好的指标。
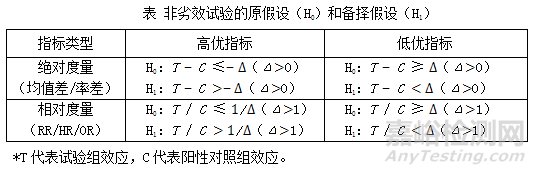
非劣效试验只需要进行一次假设检验α=0.025(单侧),即可进行统计推断。若P≤α,则拒绝H0,可推论T不劣于C;反之,则尚不能证明T不劣于C。
组间差异的置信区间法:高优指标根据T-C的双侧95%置信区间的下限大于非劣效界值-Δ,低优指标根据T-C的双侧95%的上限小于非劣效界值Δ;则可推断试验的非劣效结论成立。
根据《医疗器械临床试验设计指导原则》中的要求,对试验结果进行假设检验,建议同时采用假设检验和区间估计的方法。因此,非劣效试验需要同时满足假设检验和置信区间法。
4.非劣效与优效检验的转换
在非劣效试验方案中可以预先定义非劣效与优效检验的转换,即先进行非劣效检验,如果非劣效结论成立,可进一步进行优效检验,如果优效结论成立,则研究结论为优效;如果优效结论不成立,则研究结论为非劣效。当非劣效结论不成立时,不再进行优效检验,研究结论不支持非劣效。上述过程无需多重性调整。
需特别注意,非劣效与优效检验的转换必须事先在临床试验方案中明确定义。

来源:CIRS医疗器械监管动态


