今日头条
云顶新耀引进IgA肾病新药获批上市。云顶新耀引进的布地奈德的创新口服靶向迟释制剂耐赋康®(Nefecon)获新加坡卫生科学局批准上市,用于治疗原发性IgA肾病。Nefecon是全球首款获批的针对IgA肾病的靶向药,在临床试验(NefIgArd)中较安慰剂降低患者27%(P=0.0003)的尿蛋白肌酐比(UPCR),UPCR较基线值减少了31%(vs5%)。云顶新耀拥有该新药在大中华地区、新加坡和韩国开发以及商业化权利。
国内药讯
1.石药ADC启动头对头Ⅲ期临床。石药集团HER2 ADC新药DP303c在Clinicaltrials.gov网站上注册了一项Ⅲ期临床,拟评估DP303c对比曲妥珠单抗Emtansine治疗HER2阳性晚期乳腺癌患者的有效性和安全性,预计2025年12月初步完成。去年6月,该新药已在国内开展III期临床,评估与曲妥珠单抗对比,联合长春瑞滨/卡培他滨三线及以上治疗HER2阳性晚期乳腺癌的有效性与安全性,该项试验主要研究者为复旦大学附属肿瘤医院胡夕春博士。
2.信达眼科双抗II期临床积极。信达生物VEGF/C3补体双靶点药物Efdamrofusp alfa注射液(IBI302)治疗新生血管性年龄相关性黄斑变性(nAMD)的II期临床达到了主要终点。第40周时,IBI302(6.4mg,Q8W;8.0mg,Q12W)组患者研究眼最佳矫正视力(BCVA)较基线提高的均值分别为10.5个和11.0个ETDRS字母数,疗效非劣效于阿柏西普(2.0mg,Q8W,9.8个ETDRS字母数);中央视网膜厚度(CST)较基线改善的均值分别为-163.19 μm和-184.46 μm,vs-108.23 μm,且药物整体安全性良好。
3.华昊中天胃癌新药获孤儿药资格。华昊中天开发的埃博霉素类似物UTD2(优替德隆口服胶囊)获FDA授予孤儿药资格,用于治疗胃癌。优替德隆是一种化疗新分子,其抗肿瘤机制与紫杉醇相似,具备多药耐药和广谱抗肿瘤活性。目前,华昊中天也正在积极推进优替德隆胶囊在中国的胃癌适应症开发,将于今年下半年启动Ⅲ期临床试验。
4.思康睿奇抗耐药实体瘤新药获批IND。思康睿奇1类化药3HP-2827片获国家药监局临床许可,拟开发单药或联合用药治疗FGFR2异常的肿瘤患者。3HP-2827是一款FGFR2抑制剂,能够高特异性的抑制FGFR2磷酸化,通过抑制FGFR2信号通路以发挥抗肿瘤作用,为FGFR2异常和耐药患者带来治疗选择。去年12月,该新药已获FDA批准开展新药研究,评估治疗FGFR2突变的不可切除或转移性实体瘤的安全性和疗效。
5.德琪中美双报双抗临床前研究见刊。德琪医药PD-L1/4-1BB双特异性抗体ATG-101的临床前研究成果日前发表于Cancer Research期刊上。ATG-101仅可在PD-L1交联条件下激活4-1BB表达阳性的T细胞,这让ATG-101具有较其它4-1BB激动剂更低的肝脏毒性,并有效抑制ICI耐药肿瘤的生长。目前,该新药正在澳大利亚、中国和美国三地同步开展I期临床,评估治疗晚期/转移性实体瘤及B细胞非霍奇金淋巴瘤 (B-NHL)的安全性与有效性。
国际药讯
1.Idorsia公司新型口服降压药获批上市。Idorsia与强生联合开发的靶向双重内皮素A/B受体(ETA/ETB)的口服拮抗剂Aprocitentan(商品名Tryvio)获FDA批准上市,与其他抗高血压药物联用,治疗难治性高血压患者。Aprocitentan可有效抑制ET-1与ETA和ETB的结合,通过抑制内皮素信息通路来控制血压。在III期PRECISION研究中,aprocitentan联合用药可显著降低顽固性高血压患者的血压,且疗效维持长达48周。
2.Optinose公司鼻喷剂获批新适应症。Optinose公司基于专有EDS递送系统开发的创新药物/医疗器械组合产品Xhance(丙酸氟替卡松)鼻喷雾剂获FDA批准新适应症,用于治疗18岁以上无鼻息肉的慢性鼻窦炎患者。该产品能够将鼻部类固醇丙酸氟替卡松递送到发生炎症的部位,尤其是通过标准鼻喷雾剂难以接触的鼻窦和鼻窦引流管。临床研究显示,Xhance治疗能显著缓解患者的症状和鼻窦炎症。
3.拜耳FIC更年期新药Ⅲ期临床成功。拜耳潜在“first-in-class”双重神经激肽-1,3(NK-1,3)受体拮抗剂elinzanetant治疗更年期血管舒缩症状(潮热,VMS)的Ⅲ期临床(OASIS 3)结果积极。此前,该项试验已达到主要终点,elinzanetant治疗第12周时患者中重度VMS的频率和严重程度较安慰剂显著降低。52周数据显示,elinzanetant的长期安全性总体与之前进行的研究数据一致。拜耳计划尽快向FDA提交elinzanetant上市申请。
4.肢端肥大症激动剂Ⅲ期临床成功。Crinetics公司口服非肽类偏向性SST2激动剂paltusotine(CRN00808)治疗肢端肥大症(acromegaly)患者的Ⅲ期PATHFNDR-2临床达到了主要终点和所有次要终点。与安慰剂相比,paltusotine治疗24周后,患者达到胰岛素样生长因子1(IGF-1)水平≤正常值上限(xULN)1.0倍的比例更高(56%vs5%,p<0.0001),且paltusotine总体耐受性良好。该公司预计今年下半年递交新药申请。
5.NASH新药Ⅱ期临床达到主要终点。Inventiva公司口服泛PPAR激动剂lanifibranor联用SGLT2抑制剂恩格列净(empagliflozin)治疗代谢功能障碍相关性脂肪性肝炎(MASH)/非酒精性脂肪性肝炎(NASH)和控制不佳的2型糖尿病(T2D)患者的Ⅱ期试验LEGEND达到了主要终点。24周时,与安慰剂组相比,lanifibranor单药组和lanifibranor联用恩格列净治疗组的糖化血红蛋白(HbA1c)水平显著下降;HbA1c绝对值较基线下降>1%的应答率分别为64%和88%。此外,药物耐受性良好。
6.AZ超20亿美元收购核药公司Fusion。阿斯利康宣布将以超20亿美元款项收购放射性偶联药物(RCs)公司Fusion Pharmaceuticals,并获得该公司首发管线FPI-2265,以及其他放射偶联药物管线资产(FPI-1434、FPI-2059和FPI-2068)。FPI-2265是一种基于锕225的PSMA靶向放射偶联药物,目前正在Ⅱ期临床TATCIST中评估用于治疗转移性去势抵抗性前列腺癌(mCRPC)潜力,临床数据预计在今年4月份读出。
医药热点
1.湖南省:执业医师晋升副高级职称新规定。湖南省卫健委日前印发《湖南省卫生系列执业医师晋升副主任医师前下基层服务工作实施管理办法》。《办法》规定,执业医师在晋升副主任医师前应到基层医疗卫生机构服务一年及以上,每次连续服务不少于6个月,特殊情况按程序备案。下基层服务人员须“全脱产”在基层服务,应积极发挥专业特长,认真完成出门诊、管病床、做手术、带教学和公共卫生服务等医疗教学工作任务。
2.北京今年将建设11家老年护理中心。3月20日,在2024年北京市老龄健康工作会议上,北京市卫健委介绍,今年北京将聚力破解“老老人”长期照护难题,11家医疗机构将转型建设老年护理中心,新增床位220张。北京市卫健委鼓励有条件的基层医疗卫生机构根据需要设置和增加提供老年护理床位,引导部分二级及以下医院转型为护理院、护理中心,支持社会力量举办护理院、护理站等长期护理服务机构。同时,安宁疗护服务发展也将加快推进,年内将有8家医疗机构转型建设安宁疗护中心,新增床位280张。
3.杭州发布全国首张“七码合一”疫苗身份证。3月20日,浙江省疾控局、杭州市卫健委、杭州西湖区卫健局发布了全国首张“七码合一”疫苗身份证,“七码合一”疫苗身份证是市民在接种疫苗后,系统自动生成的一条包含了疫苗电子监管码、疫苗批号、疾控编码、门诊编码、冷链设备编码、医护编码和受种者编码等7种编码的信息,供受种者查看。
评审动态
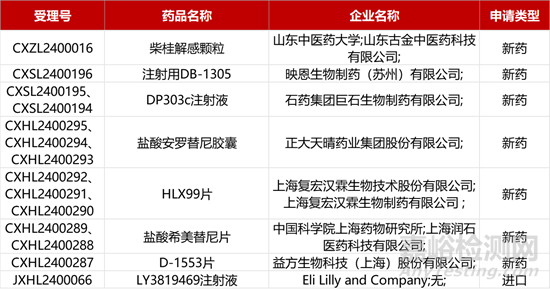
1. CDE新药受理情况(03月20日)
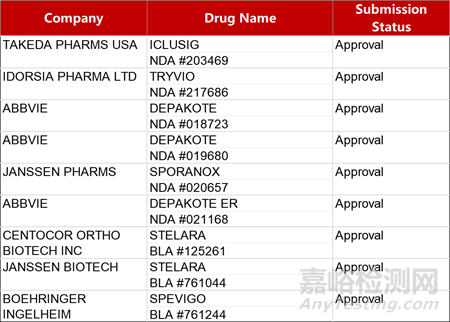
2. FDA新药获批情况(北美03月19日)