今日头条
亚虹MetAP2抑制剂膀胱癌II期临床积极。亚虹医药口服MetAP2抑制剂APL-1202在ASCO GU2024年会上公布与PD-1抑制剂替雷利珠单抗联合新辅助治疗肌层浸润性膀胱癌(MIBC)II期临床积极数据。期中结果显示,与替雷利珠单抗单药相比,APL-1202联合用药达到的病理完全缓解率(pCR)更高(39%vs21%);而且联合治疗安全性可控。该项试验将按计划继续进行下一阶段的评估。
国内药讯
1.三迭纪3D打印胃滞留药物获批临床。三迭纪公司3D打印药物T22获FDA临床许可。这是一款改良型新药,由三迭纪采用其创新的熔融挤出沉积联合微注塑工艺,并基于3D微结构胃滞留递送技术平台开发而成,拟开发用于治疗动脉性肺动脉高压(PAH)和慢性血栓栓塞性肺动脉高压(CTEPH)。在临床前研究中,T22每日1次给药与对照制剂每日3次给药具有可比拟的药代动力学参数。
2.爱科瑞思5T4靶向ADC获批实体瘤临床。杭州爱科瑞思生物自主研发靶向抗原5T4的抗体偶联药物(ADC)“注射用ACR246”获国家药监局临床许可,拟开发用于治疗晚期实体瘤,包括但不限于食管癌、结直肠癌、非小细胞肺癌、前列腺癌、卵巢癌、宫颈癌、胰腺癌、肾癌、乳腺癌。在临床前研究中,ACR246已在10多种肿瘤模型中显示出超越5T4-Dxd ADC的潜力。爱科瑞思预计在今年一季度启动这项I期临床。
3.上海原启GPRC5D靶向CAR-T获批临床。原启生物靶向GPRC5D的CAR-T产品OriCAR-017获FDA批准新药临床申请(IND),用于治疗复发/难治性多发性骨髓瘤(R/R MM)患者。OriCAR-017用于治疗R/R MM患者已在研究者发起的Ⅰ期临床中显示治疗潜力。最新数据显示,中位随访时间为280天,总体缓解率(ORR)达到100%,严格意义的完全缓解(sCR)达到80%。FDA此前已授予OriCAR-017孤儿药资格。
4.天泽云泰帕金森基因疗法报IND。上海天泽云泰生物1类生物制品VGN-R09b的临床试验申请获CDE受理。VGN-R09b是一款基因治疗产品,使用重组AAV作为基因治疗载体,以递送有功能的AADC为基础恢复多巴胺的生成,从而发挥相应的潜在的治疗作用。该产品拟开发用于原发性帕金森病(PD)和芳香族L-氨基酸脱羧酶缺乏症(AADCD)。
5.来凯AKT抑制剂卵巢癌Ⅱ期临床未达终点。来凯医药AKT抑制剂afuresertib联合紫杉醇治疗铂耐药卵巢癌(PROC)的国际Ⅱ期临床(PROFECTA -II)未达到主要终点。与紫杉醇相比,afuresertib联合治疗改善患者PFS,降低疾病进展或死亡的风险(HR为0.744(95 % CI:0.502–1.102),但不具统计学意义;在生物标志物阳性亚组(AKT磷酸化阳性,IHC>1)中,联合治疗显著改善PFS,HR为0.352(95 % CI:0.125–0.997)。此外,药物安全性良好。
国际药讯
1.TKI联合PD-L1治疗mCRPC临床积极。Exelixis公司激酶抑制剂卡博替尼联合PD-L1抑制剂阿替利珠单抗治疗转移性去势抵抗性前列腺癌(mCRPC)的Ⅲ期临床CONTACT-02积极结果公布于ASCO GU2024年会上。中位随访为14.3个月时,这一组合疗法较新型激素治疗降低了疾病进展或死亡风险35%(HR=0.65,95% CI:0.50-0.84;p=0.0007),两组中位PFS分别为6.3个月和4.2个月;总生存期(OS)也显示改善趋势,但数据尚未成熟。此外,药物安全性良好。
2.O药皮下注射剂型肾癌III期临床积极。百时美施贵宝皮下注射PD-1纳武利尤单抗(Opdivo)治疗晚期或转移性透明细胞肾细胞癌(ccRCC)的III期CheckMate-67T研究达到共同主要终点。与静脉输注相比,Opdivo皮下注射在28天内平均血清浓度和稳态血清低谷浓度指标上达到非劣效性;客观缓解率也达到非劣效性(24.2%vs18.2%)。此外,Opdivo两种给药方案安全性一致。
3.AZ/第一三共HER2-ADC实体瘤sBLA获优先审评。阿斯利康与第一三共开发的HER2靶向抗体偶联药物(ADC)Enhertu的补充生物制品许可申请(sBLA)获FDA受理,用于治疗不可切除或转移性HER2表达实体瘤患者。FDA同时还授予其优先审查资格。在II期DESTINY-PanTumor02研究中,中位随访为12.75个月时,Enhertu达到37.1%的确认客观缓解率(ORR),中位缓解持续时间(DOR)为11.3个月,中位PFS和中位OS分别为6.9个月和13.4个月。
4.微生物组免疫疗法胃癌Ⅱ期临床积极。Genome & Company公司在ASCO GI 2024年会上公布其口服乳酸乳球菌疗法GEN-001与PD-L1抑制剂Bavencio联合治疗难治性胃癌的Ⅱ期临床积极结果。在接受过PD-1/PD-L1抑制剂治疗后疾病进展的难治性患者中,GEN-001联合治疗达到37.5%的总缓解率(ORR);中位无进展生存期(PFS)为1.7个月,中位总生存期(OS)为7.9个月;而且联合治疗安全性可控。
5.诺和诺德拟2.35亿欧元引进口服减肥药。诺和诺德宣布与瑞士生物技术公司EraCal Therapeutics就后者减重口服小分子新药达成合作与许可协议,获得该新药的所有独家开发和商业化权益。根据协议,EraCal将获得预付款、开发与商业化里程碑后期付款,以及产品的销售分成。这项交易金额总计达2.35亿欧元(当前汇率折合人民币约18.34亿元)。
6.默沙东布局AI新药开发。默沙东与Variational AI公司将利用后者的Enki生成式人工智能(AI)平台,合作开发创新和选择性小分子候选药物。Enki技术平台基于生成式AI算法,可以根据用户提供化合物的目标产品特征(TPP,包括靶点、脱靶效应等对小分子化合物的要求),在几天内生成符合TPP要求的多样化、具选择性、可合成的创新小分子结构,加速进入先导化合物优化阶段。
7.AOC药物公司Dyne拟寻求合作伙伴。彭博社消息日前透露Dyne Therapeutics正在探讨被收购或者寻求合作伙伴的可能性。受此消息影响,Dyne Therapeutics当天股价大涨18%。就在两星期前,Dyne公司已宣布完成总额达3.451亿美元融资,以用于支持其抗体偶联寡核苷酸(AOC)DYNE-101和DYNE-251的临床进展。在Ⅰ/Ⅱ期ACHIEVE试验中,DYNE-101在强直性肌营养不良1型(DM1)患者中表现出剂量依赖性的剪接矫正、肌肉递送和DMPK敲除。在Ⅰ/Ⅱ期DELIVER试验中,接受DYNE-251治疗的杜氏肌营养不良(DMD)患者的平均抗肌萎缩蛋白表达为0.88%。
医药热点
1.世界首例克隆西藏濒危牛诞生。 近日,中国农科院北京畜牧兽医研究所余大为研究团队将分布在青藏高原的濒危牛种樟木牛和阿沛甲咂牛通过体细胞克隆技术,成功实现人工繁殖并获得了8头克隆牛。余大为研究员表示:接下来,我们将在西藏本地开展樟木牛和阿沛甲咂牛克隆胚胎移植,将克隆技术与常规保种技术相结合,构建完善的遗传资源保护利用体系。
2.上海3款单抗药物纳入医保。1月26日,上海市医药集中招标采购事务管理所发布通知,公布3款纳入本市医保支付药品参考采购价,分别为:神州细胞工程有限公司的贝伐珠单抗注射液,参考采购价:1298元/盒;海正生物制药有限公司的注射用曲妥珠单抗,参考采购价:1588元/盒;安徽安科生物工程(集团)股份有限公司的注射用曲妥珠单抗,参考采购价:1575元/盒。自2024年1月29日起执行。
3.全面消除麻风危害可持续发展规划出台。近日,国家疾控局印发《全面消除麻风危害可持续发展规划(2024-2030年)》提出,到2025年,进一步巩固基本消除麻风危害成果,实现全国麻风患病率大于1/10万的县(市、区)数少于1%;麻风患者完成治疗时新发生2级畸残比控制在3%以下。到2030年,达到全面消除麻风危害目标,全国麻风患病率大于1/10万的县(市、区)数为0;麻风患者完成治疗时新发生2级畸残比为0。
评审动态
1. CDE新药受理情况(01月29日)
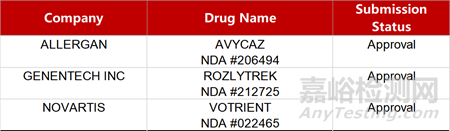
2. FDA新药获批情况(北美01月26日)