在眼科技术取得突破性进展的一年中,2023年见证了一系列高端医疗设备的推出,这些设备有望重塑眼部诊疗护理的格局,为眼科领域带来切实的临床获益。
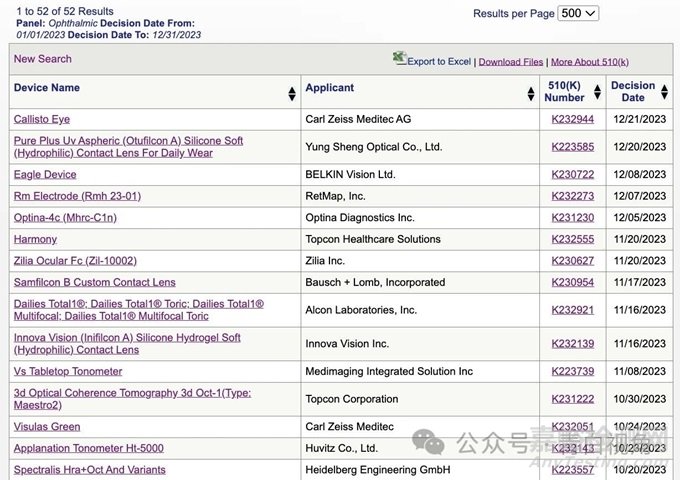
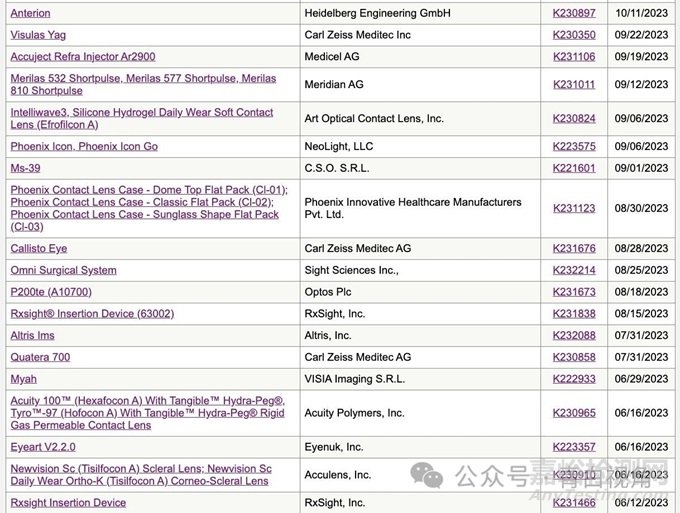
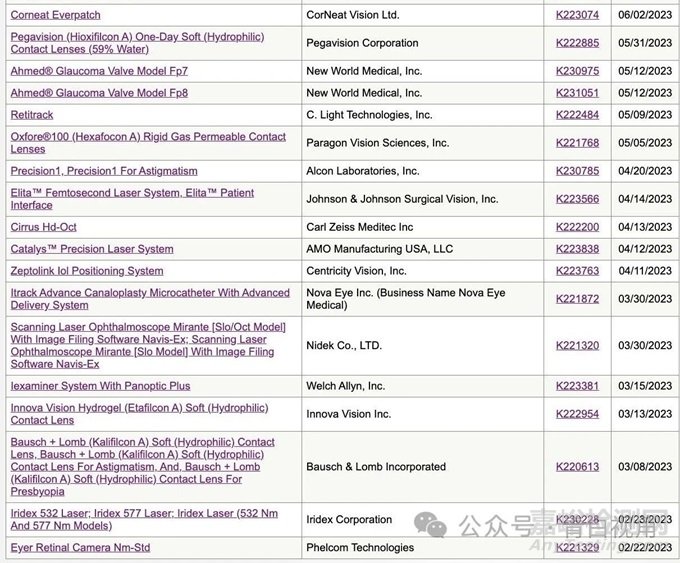
510 (k)为医疗器械在美国上市的主要途径之一,大部分的II类医疗器械和部分I类、III类医疗器械通过此途径清关上市。截至2023年12月31日,共有52款眼科医疗设备获得510(k)批准。见下图。
以下列出了9款笔者认为值得再次回顾的创新医疗设备,以审批时间从近及远排序。
1 、Belkin / Eagle / 青光眼
2023年12月,Belkin Vision(贝尔金视觉)的Eagle系统获得了FDA510(K)许可。相较于传统的SLT治疗,Belkin Vision的非接触、操作简便的一键式Eagle设备,作为青光眼激光治疗领域的革命性创新技术,有望成为轻/中度青光眼患者的一线治疗方案。Eagle在2022年5月获得CE Mark认证。
2 、Zilia/ Ocular™ FC / 视网膜
2023年11月,Zilia 宣布美国 FDA 已为其视网膜相机 Zilia Ocular FC 授予 510(k) 许可。该公司表示,现在将重点关注获得眼血氧饱和度(视网膜氧合测量)的从头分类。公司表示此类测量可以对青光眼、糖尿病性视网膜病变和年龄相关性黄斑变性进行早期诊断。
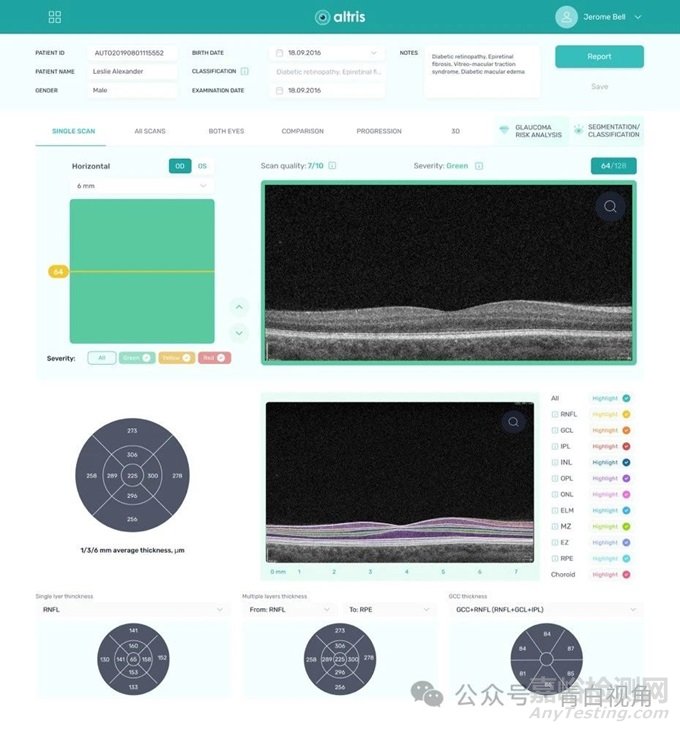
3、Altris/ Altris IMS/ 视光
2023年7月,Altris 的 Altris IMS(该公司的图像和数据管理平台)获得了 FDA 510(k) 许可。Altris 平台旨在存储、组织和支持光学相干断层扫描 (OCT) 扫描的深入分析。据公司新闻稿称,该平台提供安全、云端、基于网络的访问,以促进眼科和视光领域更方便、更准确的 OCT 扫描分析。
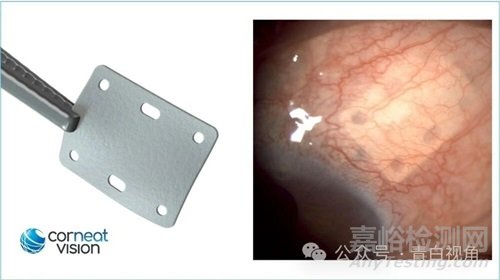
4、CorNeat/ EverPatch/ 眼表重建
2023年6月,FDA 向 CorNeat Vision 的 EverPatch 授予 510(k) 许可,该公司将其描述为世界上第一个用于眼科手术的合成、不可降解的组织整合基质。它可与周围组织融为一体从而加固巩膜并帮助眼表的物理重建。这种突破性的合成组织替代品旨在满足眼外科医生的关键需求,为世界各地的患者提供无菌且不可降解的解决方案。CorNeat EverPatch 有望取代供体和加工组织的使用,这些组织通常用于眼科手术,但存在疾病传播的风险。
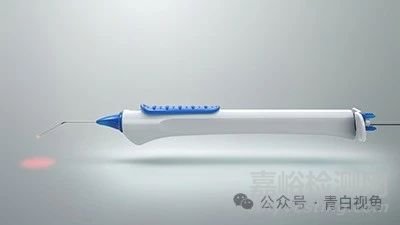
5、C. Light/Retitrack/视网膜
2023年5月,C. Light 宣布其名为 Retitrack 的视网膜眼动监测器已获得美国 FDA 的 510(k) 许可。C. Light 是一家神经技术和人工智能公司,使用视网膜眼动追踪技术研究神经退化和治疗效果。研究人员一直在研究眼球运动异常及其与创伤性脑损伤、自闭症谱系障碍、多发性硬化症和其他神经系统疾病的潜在联系。Retitrack 是第一个被批准用于医疗保健的视网膜眼动监测器。Retitrack 是一款紧凑型桌面设备,可记录 10 秒的非侵入性视网膜视频扫描,并使用分析和眼动追踪技术来检测、测量和分析微米级的注视和扫视眼动。
6、Norlase/Echo /视网膜
2023年5月,Norlase 宣布其Echo 绿光激光光凝仪已获得美国 FDA 510(k) 许可和欧洲 CE 认证。Norlase 说 Echo 是“真正便携的”,将激光和扫描仪集成到一个连接到兼容裂隙灯的单一传输设备中。其他功能包括:最小的可用物理足迹;模式和参数的语音控制;包含网格、圆形和三重弧形的完整图案调色板;用于组织保留治疗的微秒模式;无光纤设计可最大限度地减少昂贵的维修和服务中断。Norlase 还销售 Leaf,这是一种直接安装在裂隙灯上的激光光凝仪;Lion,一种完全集成到 Keeler 间接检眼镜耳机中的绿色激光光凝器。
7、Centricity/ZeptoLink/白内障
2023年5月,Centricity 宣布其下一代 ZeptoLink IOL 定位系统已获得美国 FDA 510(k) 许可。该平台现在与任何超声乳化系统集成,该公司表示这将节省手术室的时间和空间,同时为外科医生提供通过超声乳化脚踏板的完全控制。最初的 Zepto 于 2017 年 6 月获得美国许可,用于在白内障手术期间进行前囊切开术。该系统旨在创建具有一致的 360 度人工晶状体重叠的即时囊切开术,以实现最佳晶状体定位和改善结果。Centricity 表示计划5月开始分阶段推出 ZeptoLink,并在 2023 年晚些时候进行更广泛的商业发布。
8、强生视觉/Elita/近视
2023年4月,强生视觉宣布其 Elita 飞秒激光器已获得美国 FDA 510(k) 许可,用于制作 LASIK 皮瓣。Elita 激光器将于今年提供给美国眼科医生。Elita 具有单脉冲低能量、超快激光重复率和小光斑尺寸(约 1 微米)的特点,并提供光滑的基质床,可以毫不费力地提起皮瓣。已在欧洲获得 CE 标志。新型激光将使外科医生能够通过 SILK手术对近视患者进行屈光矫正,无论有无散光。此前该微透镜摘除手术系统在美国尚未获得批准。
9、Nova/Track Advance/青光眼
2023年3月,Nova Eye Medical 宣布其新型粘小管成形术手术器械 iTrack Advance 已获得 FDA 510(k) 许可,降低原发性开角型青光眼成年患者的眼压。粘小管成形术于 2008 年首次引入美国市场,是一种无支架微创青光眼手术 (MIGS),可根据患者生理情况降低青光眼患者的眼压,已在全球超过 120,000 例粘小管成形术中使用。