您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-11-16 10:50
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
国内药讯
1.石药rt-PA类溶栓药脑梗死适应症报产。国家药监局受理石药集团旗下石药明复乐递交的注射用重组人TNK组织型纤溶酶原激活剂(铭复乐,rhTNK-tPA)的新适应症上市申请,推测适应症可能是针对急性缺血性卒中(脑梗死)的治疗。今年8月,铭复乐在用于治疗急性缺血性卒中的III期临床(TRACE II)中达到主要终点,铭复乐与阿替普酶相比,90天mRS评分0-1分的患者比例达到非劣性标准。
2.君实PD-1抑制剂在欧洲报产。君实生物PD-1抑制剂特瑞普利单抗向欧洲药品管理局(EMA)提交两项上市申请(MAA),联合顺铂和吉西他滨一线治疗局部复发或转移性鼻咽癌(NPC);以及联合紫杉醇和顺铂一线治疗不可切除局部晚期/复发或转移性食管鳞癌(ESCC)。今年7月,FDA也受理该新药重新提交的上市申请,联合吉西他滨/顺铂一线治疗晚期复发或转移性NPC患者,以及单药二线及以上治疗复发或转移性NPC,PDUFA日期为今年12月23日。
3.恒瑞「吡咯替尼」新适应症拟纳入优先审评。恒瑞医药HER1/HER2/HER4酪氨酸激酶抑制剂马来酸吡咯替尼片的新适应症上市申请获CDE拟纳入优先审评,拟用于一线治疗HER2阳性复发/转移性乳腺癌患者。今年8月,该新药联合曲妥珠单抗和多西他赛一线治疗HER2阳性复发/转移性乳腺癌的III期临床(HR-BLTN-III-MBC-C研究)达到主要终点,吡咯替尼联合治疗显著改善患者的无进展生存期(24.3vs10.4个月,HR=0.41)。
4.基石引进三抗实体瘤早期临床积极。基石药业在SITC2022年会上公布从Numab公司引进的PD-L1/4-1BB/HSA多特异性抗体CS2006(NM21-1480)治疗先前已接受过多种方案治疗的晚期实体瘤的I期剂量递增研究结果。在23例可评估患者中,大多数患者能观察到临床获益,有1例患者(晚期结直肠癌)显示部分缓解。24-800mg剂量组患者的8周疾病控制率(DCR)为57%。大多数治疗相关的不良事件(TRAE)的严重程度为轻中度。
5.固安鼎泰三靶点DNA肿瘤疫苗报IND。固安鼎泰海规生物公司1类生物制品"NMM肿瘤治疗性DNA疫苗裸质粒注射液"临床试验申请获CDE受理(受理号:CXSL2200571),推测这是一款靶向3个肿瘤抗原靶点的DNA疫苗,拟通过局部注射用于多种实体瘤的治疗。今年4月,该公司获得一项名为《 一种抗肿瘤重组NMM融合抗原质粒DNA疫苗》的专利授权(CN109081873B);该项发明设计和构建了一种融合有3个肿瘤抗原靶点(NY-ESO-1, MUC1,MAGE-A3)的重组质粒DNA(pNMM)疫苗。
6.豪森引进一款临床前EGFR/cMet双抗。翰森制药附属公司翰森(上海)健康与普米斯生物就后者一款临床前期EGFR/cMet双抗药物PM1080订立合作许可协议,获得PM1080在中国的开发、注册审批、生产及商业化授权。PM1080具有能够同时阻断EGFR和c-Met的信号传导,抑制肿瘤生长和存活等作用的巨大治疗潜力。根据协议,普米斯将获得5000万人民币首付款,和高达14.18亿人民币的潜在里程碑付款,以及产品的销售分成。
国际药讯
1.创新ADC治疗难治性卵巢癌获FDA加速批准。ImmunoGen公司靶向FRα的抗体偶联药物Elahere(mirvetuximab soravtansine)获FDA加速批准上市,用于单药治疗FRα高表达、对含铂疗法耐药的晚期卵巢癌经治患者。在关键Ⅲ期临床SORAYA中,该新药经研究者评估的客观缓解率达到31.7%(95% CI:22.9%,41.6%),中位缓解持续时间为6.9个月(95% CI:5.6,8.1)。华东医药拥有该新药在大中华区的独家授权。
2.体内CRISPR基因编辑治疗HAE早期临床积极。Intellia Therapeutics公司在ACAAI2022年会上公布CRISPR/Cas9候选疗法NTLA-2002治疗遗传性血管水肿(HAE)的Ⅰ/Ⅱ期临床最新结果。数据显示,25mg和75mg剂量队列患者的激肽水平降幅分别为64%与92%,且持续时间分别达到32与16周;其中25mg剂量组在第1周至第16周平均HAE发病率降低91%,在第5周至第16周平均HAE发病率降低89%,并且在单次给药后5.5~10.6个月无进展。NTLA-2002总体耐受性良好。
3.肿瘤反应性CAR-NK疗法临床前研究积极。CytoImmune公司在STIC 2022年会上公布其双机制、工程化CAR-NK细胞疗法CYTO-102的临床前数据。研究结果显示,CYTO-102在体外模型中产生了对淋巴瘤和非小细胞肺癌(NSCLC)的连续杀伤;当与肿瘤抗原导向的单抗联用时,能够有效增强NK细胞的连续杀伤能力并让不敏感NK细胞系在体外转化为敏感细胞系;TRACK-NK细胞能够有效地“循环”表达CD16,并且其连续杀伤能力可在细胞静息或冷冻保存后迅速恢复表达。
4.罗氏Aβ单抗两项III期研究失败。罗氏皮下注射Aβ单抗Gantenerumab治疗早期阿尔茨海默病的两项III期GRADUATE研究(GRADUATE I 和II)没有达到主要终点。116周治疗数据显示,两个试验Gantenerumab组痴呆严重程度评分(CDR-SB)较基线分别降低-0.31(p=0.0954)和-0.19(p=0.2998),均无统计学意义。此外,Gantenerumab清除Aβ蛋白水平低于预期。药物的总体耐受性良好。
5.内分泌多肽药物公司完成新一轮融资。MBX Biosciences公司宣布完成金额达1.15亿美元的B轮融资,以推动其先导项目MBX 2109治疗甲状旁腺功能减退症的Ⅰ期临床开发,以及用于支持包含MBX 1416在内的临床前管线和其他内分泌疾病项目的发现与开发。MBX 2109是一款长效甲状旁腺内分泌多肽前体,能够以一周一次的剂量,提供长效的甲状旁腺激素(PTH)活性。该药物今年7月已获得FDA的孤儿药资格。
医药热点
1.中国高血压临床实践指南发布。11月13日,由国家心血管病中心、中国医师协会等学术机构共同制定的《中国高血压临床实践指南》正式颁布,推荐将我国成人高血压诊断界值由140/90mmHg下调至130/80mmHg,与五年前美国高血压协会/美国心脏病协会发布的标准平齐。以新标准估算,中国高血压患者数将由2.45亿增至近5亿,超1/3国人都将成为高血压病患者。
2.新疆防疫一线医务人员可提前申报高级职称。日前,新疆维吾尔自治区人力资源和社会保障厅发布消息称,自治区人社厅结合当前疫情防控工作需要和职称评审工作实际,提早研判、精准施策,采取放宽继续教育学习时间、延长职称申报期限等五项工作举措,稳步有序推进专业技术人员职称评审工作。其中,为关心关爱抗疫一线医护人员,新疆明确在2022年卫生健康系列高级职称评审工作中,疫情防控一线医务人员可提前一年申报职称。
3.全球人口达到80亿。联合国《世界人口展望2022》报告预计,全球人口在2022年11月15日达到80亿。根据此前联合国人口基金会的统计,全球人口在2011年10月31日达到了70亿。世界人口从70亿增长到今天的80亿,用了11年零半个月。根据联合国最新预测,到本世纪80年代,全球人口将达到约104亿的峰值,并保持这个水平到2100年。
评审动态
1. CDE新药受理情况(11月15日)
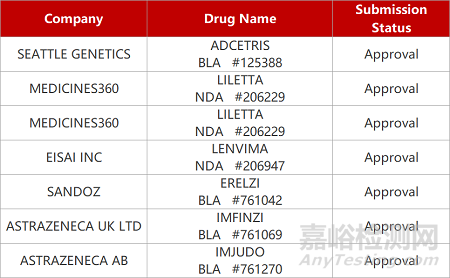
2. FDA新药获批情况(北美11月10日)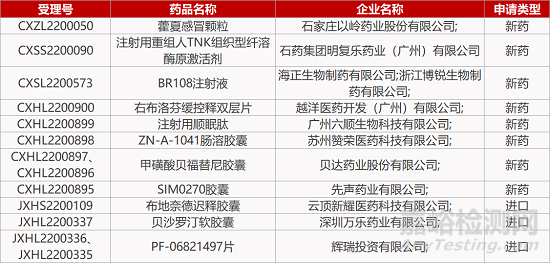

来源:药研发


