您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-11-09 11:21
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
润新“一靶多点”新药上肝癌Ⅱ期临床。润新生物Na+/K+-ATP酶抑制剂RX108治疗晚期肝细胞癌的Ⅱ期临床日前在复旦大学附属肿瘤医院完成首例患者给药。RX108具有“一靶多点”的作用机制,旨在通过多种途径发挥抗肿瘤作用。目前该新药正在中国、澳大利亚和美国针对不同实体瘤开展多项临床研究,适应症涉及复发胶质母细胞瘤、复发转移性头颈部鳞癌等恶性实体瘤。
国内药讯
1.K药治疗早期三阴性乳腺癌在华获批。默沙东重磅PD-1抑制剂帕博利珠单抗注射液(Keytruda,可瑞达)获国家药监局批准新适应症,推测适应症为用于经充分验证的检测评估肿瘤表达PD-L1(综合阳性评分(CPS)≥20)的早期高危三阴性乳腺癌(TNBC)患者的治疗。在III期临床(KEYNOTE-522)中,中位随访39.1个月时,帕博利珠单抗联合化疗较单纯化疗显著改善患者EFS,HR=0.63(95%CI 0.48~0.82,P=0.00031)。这是帕博利珠单抗在中国获批的第10项适应症。
2.信达PCSK9单抗降脂III期临床成功。信达生物PCSK-9抑制剂托莱西单抗(IBI306)将在AHA 2022会议上公布在中国非家族性高胆固醇血症患者中的III期CREDIT-1研究积极结果。与安慰剂组相比,托莱西单抗(450mg Q4W和600mg Q6W)治疗组第48周时其LDL-C水平较基线百分比变化的组间差异分别为−65.0%(P<0.0001)和−57.3%(P<0.0001),LDL-C水平降低50%以上的患者比例分别为87.8%和71.8%。药物总体安全性良好。2022年6月,该新药的上市申请已获CDE受理。
3.诗健FIC抗体新药获批临床。诗健生物1类生物药ESG206注射液获国家药监局临床试验默示许可,拟开发用于治疗B细胞恶性肿瘤。ESG206是一款潜在“First-in-Class”单抗药物,特异性靶向一个未披露的B细胞特异靶点,全球尚无针对该靶点的药物获批应用于临床治疗。ESG206经过糖基化修饰,加强了抗体介导的细胞杀伤作用。目前该新药正在澳大利亚开展首次人体试验。
4.中科拓苒2款小分子抗肿瘤新药获批临床。安徽中科拓苒公司自主研发的两款1类化药TR115片和TR64片分别获国家药监局临床试验默示许可。TR115是一款针对表观遗传学靶点的小分子药物,拟开发用于非霍奇金性淋巴瘤的治疗;TR64是一款针对肿瘤免疫微环境靶点的新型小分子抑制剂,拟开发用于晚期恶性实体瘤的治疗。
5.岸迈TAA/CD3双抗在华报IND。岸迈生物1类生物制品EMB-07注射液的临床试验申报获NMPA受理。EMB-07是基于岸迈生物专有FIT-Ig®平台开发的一款靶向肿瘤相关抗原(TAA)和CD3的T细胞重定向双特异性抗体,它通过连接肿瘤细胞和T细胞,并激活T细胞,介导T细胞特异性杀伤实体肿瘤的作用。此前,该公司FIT-Ig®平台开发的四款新药PD-1/LAG-3双抗EMB-02、BCMA/CD3双抗EMB-06、EGFR/cMET双抗EMB-01和PD-L1/OX40双抗EMB-09均提交了IND申请。
国际药讯
1.杨森双重ET拮抗剂降压III期临床成功。杨森与Idorsia共同开发的新型口服双重内皮素(ET)受体拮抗剂aprocitentan,在治疗难治性高血压的III期PRECISION研究达到主要研究终点和关键次要终点。与标准抗高血压疗法相比,Aprocitentan(12.5mg、25mg)联合标准抗高血压疗法显著降低患者坐位收缩压,组间差异分别为-3.8mmHg(p=0.0042)和-3.7mmHg(p=0.0046)。该研究中最常见的不良事件是轻中度液体潴留。
2.安进RNAi疗法降血脂Ⅱ期临床积极。安进RNAi疗法olpasiran(AMG 890)治疗动脉粥样硬化性心血管疾病(ASCVD)的Ⅱ期临床(OCEAN(a)-DOSE)达到主要终点。在36周时,与安慰剂相比,每12周接受一次olpasiran(75mg、225mg)的患者其Lp(a)水平降幅分别为97.4%和101.1%,olpasiran治疗组有超过98%的患者其Lp(a)水平下降至标准值125 nmol/L或更低。预计今年12月启动Ⅲ期试验。
3.乙肝RNAi疗法联合用药Ⅱ期临床积极。Vir Biotechnology公司潜在功能性治愈乙肝的RNAi疗法VIR-2218联合干扰素α(IFN-α)治疗慢性乙肝的Ⅱ期临床结果积极。与VIR-2218单药相比,VIR-2218与长效干扰素α联用能更有效地降低乙肝表面抗原(HBsAg);最高剂量联合治疗组48周治疗后,有30.8%的患者体内检测不到HBsAg,患者同时体内出现抗乙肝蛋白的抗体(抗乙肝抗体>10 mIU/mL),显示出免疫系统对乙肝蛋白产生免疫反应的迹象。
4.CD30/16A双抗联合NK细胞疗法最新数据积极。Affimed公司先天性细胞衔接器(ICE®)AFM13(CD30/CD16A双抗)预先与脐带血来源的自然杀伤细胞(cbNK)结合,在用于治疗CD30阳性复发或难治性霍奇金淋巴瘤和非霍奇金淋巴瘤的I/II期临床最新数据积极。共有30例患者参与这项研究。数据显示,联合疗法达到100%的客观缓解率(ORR)和70.8%的完全缓解率;中位随访为8个月时,无事件生存率(EFS)为57%,总生存率为83%。此外,联合治疗总体安全性可控。
5.靶向放射疗法联合用药早期临床积极。Actinium公司CD33靶向放射疗法Actimab-A联合挽救性化疗方案CLAG-M治疗复发或难治性急性髓系白血病(AML)的Ⅰ期试验结果积极。联合治疗的总缓解率(ORR)为67%,达到细胞遗传学完全缓解(CRc)的患者中,有72%为微小残留病灶(MRD)阴性;中位总生存期(OS)为12个月(n=21),1年总生存率为53%,2年总生存率为32%,约为现有治疗方法的两倍。
6.葛兰素史克BCMA-ADC头对头III期临床失败。葛兰素史克BCMA靶向ADC药物Blenrep(belantamab mafodotin)与pomalidomide联合低剂量地塞米松(PomDex)相比,在治疗复发或难治性多发性骨髓瘤(RRMM)的头对头III期研究(DREAMM-3)未达到PFS优效性主要终点。Blenrep组和PomDex组的中位PFS分别为11.2个月和7个月(HR=1.03);两组ORR分别为41%和36%;两组中位OS分别为21.2个月和21.1个月(HR=1.14)。
医药热点
1.上海一医院实施“主诊医师负责制”。11月起,上海市长宁区妇幼保健院正式实施“主诊医师负责制”。今后,到该院建卡的每一位孕妇,从孕期到产时,再到产后的整个医疗过程,无论是产检、手术、住院,还是产后随访都将由一个团队完成。据悉,该保健院产科被分为W、X、F、C四个主诊医疗小组;每个医疗小组由1名主诊医师、1名副主诊医师,以及若干名住院医师组成。每个小组在本组主诊医师的率领下,全权负责实施患者门诊、住院、手术、会诊、出院后随访等一系列医疗活动。
2.国家检验医学中心设置标准发布。11月7日,国家卫健委官网发布《国家检验医学中心设置标准》,明确国家检验医学中心应依托检验学科特色突出的三级甲等综合医院,并具有与检验医学密切相关的10个及以上国家临床重点专科建设项目科室;临床常规开展检验项目数≥800项、年总检测工作量≥2500万项次等六大基本条件。
3.国家自科基金累计资助21341项中医药项目。11月5日,国家自然科学基金委员会医学部常务副主任孙瑞娟透露,截至2022年,国家自然科学基金累计资助中医药项目21341项。其中,2013—2022年,中医药领域获得国家自然科学基金资助项目共计14567项,占医学科学部资助项目总数量的14.53%;获得国家自然科学基金资助金额超64亿元,占医学科学部资助总金额的12.87%;中医药领域国家自然科学基金项目申请资助率为14.02%。
评审动态
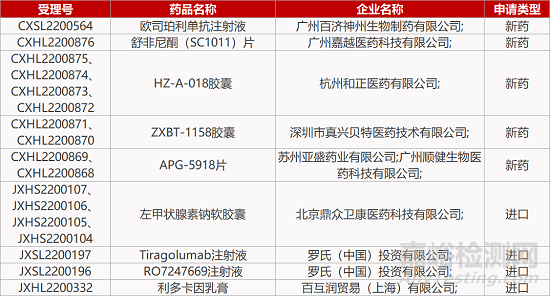
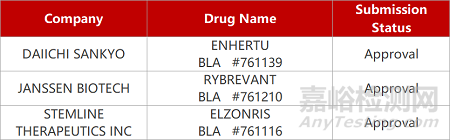

来源:药研发


