您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-07-10 22:37
摘要 在“十四五”行业规划发展的背景下,制药行业迎来了战略转型的关键时期。药物辅料是药品中除药效物质外另一大类成分,其产业技术研究、创新型产品研发等对药品高质量发展具有决定性作用。儿童专用药是新时代医药行业关注热点,规范辅料的应用是区别成人用药与儿童专用药的关键一步。该文将结合国内政策背景,综述辅料行业现状、技术瓶颈、儿科药物辅料应用问题及其发展热点,解读适用于儿科制剂的辅料创新研究发展战略布局,为其未来发展技术路线提出展望,以期为行业转型奠定坚实基础。
药用辅料被定义为 “在完整的药物制剂中,除活性药物或前药以外的任何物质”,具有增加药物稳定性、提高药品生物利用度、保证药物使用安全、增强患者顺应性等。药物辅料虽不具有明显的药物活性,但不能完全将其认为“惰性物质”,其与药物一同进入人体,在体内发生吸收、代谢、转运和消化等过程,因此药物辅料对人体的作用也不容忽视。我国制药行业一直以来是“重原料药,轻辅料”,导致药物辅料行业的发展起步晚、发展缓,在国内市场份额较低,与国外辅料发展无法抗衡。随着 2020 年版《中国药典》颁布、《中华人民共和国药品管理法》等一系列相关政策的落实,在国家鼓励医药行业发展的大背景下,药物辅料行业迎来了转型的好时机。同时,近年来《药品管理法》《药品注册管理法》等相关法案重点鼓励儿童专用药物的研究与开发,儿童较成人相比,其生理特征更为特殊,身体各内脏器官、体质功能等处于发育阶段,尚未成熟,并且新陈代谢较快,儿童表现出与成人不同的药动学特征。笔者认为研发儿童专用药物辅料,聚焦辅料在儿童群体中的运用特点与现存问题,具有十分良好的发展前景,因此本文通过对国家相关政策进行解读,对现今药物辅料行业发展热点与待突破的瓶颈、儿童药物辅料应用问题、发展热点进行综述,并结合医药行业的发展走向及国内市场需求对药物辅料技术路线进行展望。
1药物现代化发展背景下制剂辅料研发战略布局
随着我国全面开启建设社会主义现代化国家,医药行业进入现代化发展的大背景下,药品辅料的高质量发展逐渐成为药品发展中的关键一环。同时,随着国内外市场需求不断增加,多条药物辅料相关政策相继颁布,为医药制剂蓬勃发展奠定坚实基础并指明方向。
1.1 药物辅料质量监测与药品检查关联
2016 年 8 月,国家药品监督管理局[1]发布《关于药包材、药用辅料与药品关联审评审批有关事项的公告》,在此公告发布前,药品与药用辅料在审批过程中为相互独立的流程,而此版《公告》中明确规定:国家食品药品监督管理总局按照风险管理的原则在审批药品注册申请时对药包材、药用辅料实行关联审评审批;自本公告发布之日起,药包材、药用辅料应按程序与药品注册申请关联申报和审评审批,《药包材及药用辅料申报资料要求》另行公布,各级食品药品监督管理部门不再单独受理药包材、药用辅料注册申请,不再单独核发相关注册批准证明文件;药包材、药用辅料生产企业应对产品质量负责;应在满足相应生产质量管理要求的条件下组织生产;应配合药品生产企业开展供应商审计。此公告的发布意味着药用辅料单独审批的时代已经过去,其质量等问题将成为决定制剂审批的重要因素。同时,2020 年版《中国药典》中加强了药用辅料通用技术要求的制定,为关联审评审批制度做好技术支持,并完善了辅料功能性评价的方法[2]。关注药物辅料,对药物制剂的质量监管具有重要意义,着力于药用辅料质量提高以及安全性检查是未来制剂发展的重要发展趋势与方向。
1.2 加强“原辅包”有机结合,促进国内制度与国际高水平标准接轨
最新修订(2019 年版)《中华人民国和国药品管理法》[3],对药物辅料、包材及容器等一并与原料药合并审评审批,保障药物质量管理规范。其中将原材料、包材、药物辅料视为一个有机整体,“原辅包关联”审批审评制度细则更加接近美国 DMF 标准和欧盟 CEP 认证等,与国际发达国家逐步接轨。制定高标准要求及高水平管理制度,都有利于促进国内医药产业改革转型同时调动全行业研发的积极性。
1.3 健全药物辅料审评审批机制,促进药品产业高质量发展
“十四五”规划意味着我国进入开启全面建设社会主义现代化国家,是具有重大历史使命和意义的开局规划。根据“十四五”发展目标,其中提出“保障药品用药安全,促进药品高质量发展,推进药品监管体系和监管能力现代化,保护和促进公众健康”。《“健康中国 2030”规划纲要》和《十四五”国家药品安全及促进高质量发展规划》均聚焦于我国药品高质量发展,明确要求我国要向制药大国迈进[4-5]。药物辅料是药物制剂中占比约 80%的组成成分,同时自“原辅包”审评结合后,药物辅料与药品质量发展具有不可分割的关系,推动辅料质量发展、促进新型辅料研发、加快相关监管制度落实都对药品行业高质量发展具有重大意义。
2药用辅料行业发展热点与突出瓶颈
我国药用辅料行业发展相较于药品产业起步较晚,由于我国传统制剂历史悠久,常用辅料多为传统辅料。与国际发达国家药物辅料产业发展相比仍然具有较大差距,我国药用辅料产业专业化水平较低,低端产品产能过剩,高端产品市场保持空白,同时新型辅料研发匮乏,药物辅料质量标准及审评制度待进一步完善。
2.1 行业标准处于初期阶段,质量标准待完善
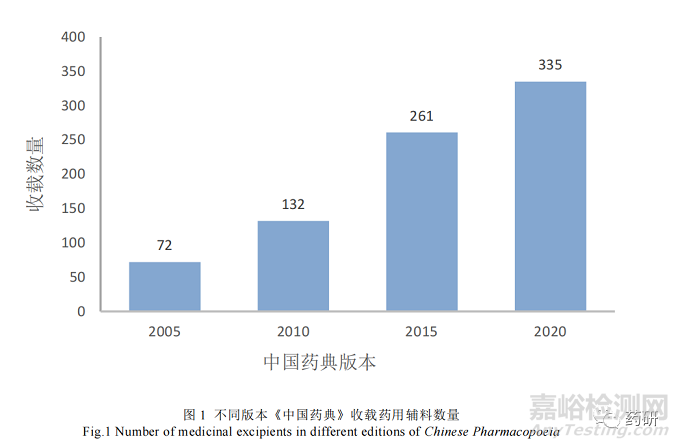
由于我国辅料生产加工行业被重视的历史不足 20 年,多种因素导致国内辅料行业呈现混乱无序的现状。大多数辅料生产企业仍处于初期阶段,辅料产品的统一标准化程度低。我国药典收载辅料相关标准变化见图 1,《中国药典》中收载药物辅料数量呈上升趋势,但就最新一版中收载辅料标准数量为 335 种,仅占市场所用辅料的 60%左右,而同期美国和欧洲市场已有统一质量标准的药物辅料数量已达 1 500~3 000 种,收载于《美国药典》药物辅料数量为我国药典的数倍[6]。说明国内质量标准管理建设仍与国际水平仍然具有一定差距,实现全行业标准的统一,促使产业有序健康发展。
2.2 辅料加工企业离散度大,专业辅料加工企业少
国外药用辅料占整个药品制剂产值的 10%~20%,由于国内市场起步晚、发展缓慢,相比于国外市场,辅料行业在我国医药行业市场占比较低,为国外辅料市场占比的 20%~30%[7]。在我国大多制药加工企业通常以收益较高的原料药为主要产品,国内辅料加工企业约有 400 多家,大多数为小型企业或以食品加工厂、化工厂等演变而来,生产加工和质量标准参差不齐,见表 1,国内稍有规模企业中近 80%都为非专业辅料加工企业,以原料药或其他产品为主,而且大多企业所生产辅料仍为低端产品,包括口服制剂的相关辅料例如糊精、淀粉等传统辅料为其主要生产产品。其中以药用辅料为主要产品的企业中,年净利润过亿元的代表性企业仅有湖南尔康制药、安徽山河药辅、湖南九典制药、南京威尔药业等少数规模较大的企业,其中山河药辅为辅料专业化研究企业的代表,其着眼于高端辅料市场,研制进口替代品种、功能性辅料、复合辅料等,并提高产品质量监管,为国内辅料加工行业未来的发展提供了崭新的思路。

2.3 药用辅料品种少、结构单一,新型辅料产品成为研发热点
我国药物辅料行业集中于中、低端产品的生产加工,其中国内企业生产集中于口服制剂中填充剂:淀粉类衍生物(包括糊精等)、甘露醇、纤维素类衍生物等;固体制剂包衣材料:薄膜包衣材料、药用明胶、肠溶包衣、胃溶包衣材料等,见表 1。而对于外用制剂中所用新型基质、渗透促进剂、成膜材料等;缓控释制剂所用骨架材料、高分子囊材、药物载体等在国内药辅企业中存在生产空白,仍然依靠大量进口产品。而近年来随着相关政策鼓励,药品研发市场出现勃勃生机,传统辅料制剂产业已不满足药物生产,专业性辅料生产、复合型辅料研制、进口辅料替代产品以及功能性辅料需求大大提高,成为未来药物辅料行业的研发热点。
3儿童药物制剂所用辅料现状
我国儿童专用药物相对于国际水平较为短缺,我国常用制剂近 4 000 余种,其中儿科药物不足 2%[8]。儿童较成人相比,其生理特征更为特殊,身体各内脏器官、体质功能等处于发育阶段,尚未成熟,并且新陈代谢较快,儿童表现出与成人不同的药动学特征[9-10],因此儿科专用药物的开发,成为近年来的研究热点。随着药物一致性评价、“原辅包”关联审评审批政策、“十四五”国家药品安全规划等相关政策的颁布,药物辅料的添加与运用引起了广泛的关注,在儿童制剂研发领域,药物辅料多种现状亟待解决。
3.1 儿童药物辅料重视度不足
根据 2021 年最新人口普查数据显示,0~14 岁儿童占全国总人口为 17%,儿童用药占全国药物市场的较大份额。儿童常用药物主要集中于传统口服剂型例如颗粒剂、片剂、口服液等,新型剂型相关研发较少,甚至常用剂型中儿科专用药品也寥寥无几。儿童处于生长发育初期,身体脏器功能等与成人差异较大,其药代动力学特征与成人也有很大不同[11],儿童对药物的敏感性更强,药物中除原料药外,药物辅料是影响药物的另一大原因,其品种、用量、适用人群等都对儿童用药安全性产生影响。然而,即便在儿科专用药中,大多辅料的选择仍与成人保持一致,儿童用药中与辅料相关的不良反应事件已有报道[12],儿童专用药物辅料的重视程度明显不足。
2013 年,欧洲和美国的儿科制剂倡议会合作创建了儿科辅料安全性和毒性网络数据库(STEP),其汇总了儿科制剂安全性、毒性数据,为儿童尤其是新生儿药物制剂辅料的合理应用具有重要贡献[13-14],FDA 对儿童药物中所用辅料颁布了相关规定[15]。而国内由于辅料行业起步晚,“重原料,轻辅料”的思想的影响,导致儿童用药辅料相关规定、文案以及政策法案等缺失,以至于儿童药物辅料发展落后于国际发达国家,相关研究存在空白。
3.2 药物制剂说明书中辅料标注率低
2006 年国家食品药品监督管理部门颁布了《药品说明书和标签管理规定》,其中第十一条明确规定了:药品说明书应当列出全部活性成份或者组方中的全部中药药味;注射剂和非处方药还应当列出所用的全部辅料名称,药品辅料的不良反应可作为参考信息一并标注在药物说明书中[16]。在一项儿童中成药使用情况的调查研究中发现,明确标注辅料信息的中成药占比比不到 1/2,儿童专用中成药无明确辅料信息标注的近 15%[17]。某三甲医院儿科统计了 47 种儿童常用中成药说明书标注情况,仅有 36.17%的品种标明了辅料成分,OTC 药品和注射剂药品中辅料标注率仅 64.71%、42.86%[18]。儿科药物辅料标注不完整,则会对儿童安全使用产生影响,其对儿童的毒性作用、不良反应等应引起重视。
3.3 儿童制剂辅料现存安全问题的辅料
通常在药物制剂中,因对成人无毒性作用或不良反应较小,药物辅料常被视为“惰性物质”。然而,儿童处于生长发育阶段,不能简单的将儿童视为“缩小版成人”,儿童器官发育不成熟,同时其代谢能力较弱,肝肾消除能力不如成年人,药物及药物辅料可能在体内产生蓄积,例如甜味剂山梨糖醇在婴儿体内蓄积则会导致糖尿病并发症,例如视网膜病变和白内障[19]。儿童免疫力较低,部分药用辅料还会导致其发生过敏反应,例如苯甲酸钠可能导致接触性荨麻疹和其他过敏反应,因成人随着身体的发育以及产生耐受性等则不会出现过敏的症状。儿童血脑屏蔽功能差,一些药物辅料容易进入脑脊液等引起中枢神经系统疾病[20],见表 2,所以一些成人可承受的药物不良风险应在儿童应用过程中引起重视。


STEP 数据库中收载了近 40 种儿童药物辅料的基础信息,其中包括药物辅料的安全性和毒性评价。苯甲酸钠是常见的防腐剂,应用于药物制剂种,可以抑制某些细菌、霉菌和酵母菌的生长,研究人员通过给予雌性大鼠不同剂量的苯甲酸钠水溶液,给药一段时间后,进行了遗传毒性研究(骨髓细胞染色体畸变、彗星实验和肝细胞 DNA 图谱),对苯甲酸钠在大鼠体内的遗传毒性进行了评价,结果表明苯甲酸钠具有潜在的遗传毒性,因此其用于儿童药物制剂中应严格控制用量[30]。为便于儿童服用,儿科制剂中常添加甜味剂等矫正药物,尤其是中药的不良气味,有研究通过彗星试验对常用的甜味剂——阿斯巴甜和糖精在艾姆斯/沙门氏菌/微粒体试验中的致突变性以及其在小鼠骨髓细胞中的遗传毒性潜力进行了评价,揭示其对人体的潜在危害作用,应该在后续药物辅料的应用中引起注意[31]。
聚山梨醇酯 80(吐温 80),是一种表面活性剂,广泛应用于液体、半固体、固体制剂中,作 O/W型乳化剂、增溶剂、湿润剂、分散剂和稳定剂等。研究者使用 MTT 法评价了聚山梨醇酯 80 作为呼吸系统药物辅料时的毒性,在 MTT 测定中,其表现出明显的浓度依赖性毒性,给未来药物辅料的选用及剂量筛选提供了参考[32]。
4儿科中药及天然制剂中辅料的应用
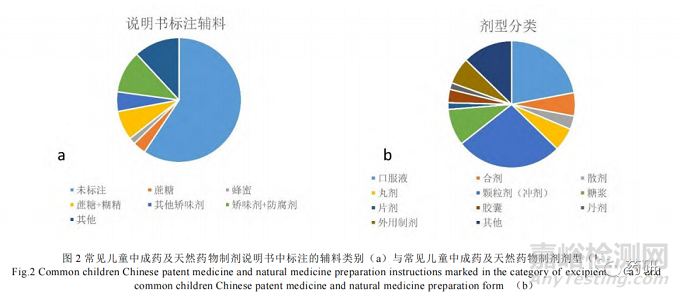
中医儿科治疗与成人近似,但由于小儿生理特征存在差异、机体功能不成熟、发病变化快等特点,用药剂型与剂量的要求相对灵活[33]。儿科中药常见剂型以颗粒、糖浆、口服液或合剂为主(图2),多为儿童适宜剂型,另有外用制剂、吸入制剂、注射剂等[34]。中药制剂常伴有味苦、量大、起效慢等缺点,应用于儿童药物时常通过添加辅料等方式改善,以便于儿童服用,文中统计了常见中药制剂及天然药物制剂的剂型以及说明书中标注的辅料添加情况,见图 2。儿童药物常以口服制剂为主,例如口服液、颗粒剂等,为提高儿童服药的顺应性,改善中药味苦气冲的缺点,常添加矫味剂,例如蔗糖、糊精等;液体制剂还常添加防腐剂防止药物成分变质等,例如使用苯甲酸钠、苯甲醇。
中药药用物质具有易吸湿、黏度大、用量大、流动性差、可压性差等特点,制备颗粒剂后常存在吸湿性较强,溶化性较差等问题[35],除选择适合的药物粉碎粒径和制备工艺外,还应通过添加适宜的辅料来调节药物的吸湿性和溶化性,例如可溶性淀粉、微晶纤维素、预胶化淀粉、糊精、羧甲基纤维素钠、玉米糊精等对颗粒剂吸湿性影响程度不同[36]。口服液体制剂为保证药液澄清度、药物稳定性等常添加防腐剂和增溶剂等辅料。如喉咽清口服液添加苯甲酸钠作为防腐剂,加入蔗糖调节药物口味;小儿解表口服液加入山梨酸钾作为防腐剂用于防止或抑制微生物的生长与繁殖。藿香正气口服液中加入吐温-80 来提高中广藿香油、紫苏叶油的溶解度。
为保证中药注射液的澄清度、药物稳定性以及有效性需加入适宜的辅料。但由于中药成分复杂、辅料性质特殊且儿童吸收代谢功能尚未发育完全,儿科中药注射剂的不良反应事件频发[37]。痰热清注射液的辅料丙二醇,用于提高药物稳定性和溶解度,可能引起局部静脉炎、渗透压升高、接触性皮炎等不良事件[38];热毒宁注射液使用葡萄糖或氯化钠混合稀释后会增加不溶性微粒的数量,由于小儿毛细血管比较细,若中药注射剂中产生较大微粒时容易在血管中沉积,可能会导致造成局部循环障碍,引起血管栓塞进而产生静脉炎,引发过敏等不良反应[39]。
因中药成分复杂,所以挑选合适的辅料对降低中药皮肤给药的毒性反应、提高药物药效作用等都具有重要意义。例如小儿退热贴剂中添加甘油作为保湿剂,加入对羟基苯甲酸作为防腐剂。与成人相比,儿童皮肤较薄、娇嫩、透皮吸收率高,且儿童药物代谢速率与成人有差异,因此中药透皮给药制剂常选择皮肤刺激性较小的月桂氮酮作为药物渗透促进剂。药用辅料的合理添加,对药物有效性、安全性起到了重要作用。
为解决中药成分与辅料的问题引入了“药辅合一”的理念[40]。例如中药传统制剂——王氏保赤丸,用于小儿乳滞疳积、痰厥惊风、喘咳痰鸣、乳食减少、吐泻发热、大便秘结、四时感冒以及脾胃虚弱、发育不良等症。王氏保赤丸基于原方汤剂的基础,选用姜淀粉和荸荠淀粉作为辅料,不仅起到赋形的作用,还能协助主药促进大肠蠕动,发挥健运脾胃的功效[41]。
5新时代儿童药物辅料发展体系
2018 年国家卫生健康委员会进行第三轮《国家基本药品目录》,其中儿童用药类别、品种、剂型、规格被重点修订,在 2021 年第四次草案修订公开征求意见,草案明确提出,国家基本药物包括化学药品和生物制品目录、中药目录和儿童药品目录,其中儿童药品主要依据儿童专用适用药分类。2019—2020 年国家相继颁布《药品管理法》《药品注册管理法》,其中明确标注国家将采取有效措施鼓励儿童药物审批上市。在儿童用药市场一片光明的新时代背景下,药物辅料的未来发展体系应引起高度关注。
5.1 规范药物辅料添加剂量
小儿正处于生长发育时期,在每个阶段都有他们各自不同的生理特点,现有研究已对不同年龄段儿童药物在体内 ADME 过程进行了研究[20]。然而据文献报道,药物中使用乙醇作为辅料,在100 mg·dL-1的剂量时会出现低血糖、酸中毒和水电解改变,更高的摄入量会导致昏迷、昏迷、呼吸抑制和心血管衰竭等严重不良反应;使用高剂量丙二醇为辅料可能会影响儿童中枢神经系统,尤其是新生儿和 4 岁以下儿童,因为他们的半衰期很长,近乎成人半衰期的 3 倍之多,大量蓄积的丙二醇引起毒性反应;儿科制剂中常添加蔗糖作为矫味剂,质量分数高于 35%的制剂会导致儿童牙齿受损,剂量更高者有致癌的风险[19]。因此儿童用药中辅料未来的发展中,其用量问题不容小视,应根据不同用药年龄段儿童生理特征的差异开展用量研究,对常见辅料种类制订用量标准规范,保证儿童制剂开发的合理性、安全性。
5.2 创新思维指导儿童制剂辅料的开发
与国际市场相比,我国药物辅料发展仍存在较大差距,现有辅料品种远远无法满足国内儿童药物需求。同时,传统辅料选择不当导致不良反应事件常有报道,例如中药液体制剂中常添加增溶性辅料吐温-80,研究发现吐温-80 可导致溶血、外周神经毒性、肝毒性等不良反应的发生[42]。儿科常用制剂多为口服制剂,其中以口服液、糖浆剂为代表,此类液体制剂为保证药物的安全性和稳定性以及防止药物霉变腐败等,常添加适量防腐剂,例如苯甲醇、苯甲酸钠、苯扎氯铵等。而文献报道了苯甲醇作为辅料成分会引起低出生体重早产儿的严重呼吸道和代谢并发症甚至死亡、苯扎氯铵局部应用于耳部的耳毒性,皮肤刺激以及会诱发过敏性哮喘 患者的支气管收缩[30]。这些不良反应说明已有药物辅料的种类、安全、规范等方面存在很多问题。药用辅料的开发应用体系的改革,除可通过提高已有药物辅料的质量安全外,创新思维的引入则是儿童药用辅料的技术体系升级发展的另一可靠途径。儿童正值生长发育期,其身体功能和器官发育的健康与否对未来成长具有至关重要的作用,因此儿童用药所用的药物辅料应引起高度重视,创新研究的药物辅料应符合儿童生长发育特点,保证其用药安全,避免药物及其辅料的不良反应,提高药物疗效。
长期以来中药多糖多被认作能量资源或结构材料,在研究中多糖常被当作“无效成分”或“杂质”而除去[43]。随着研究的深入,发现了多糖类成分不仅具有多种药理作用,同时对中药难溶性成分具有良好的增溶效果,例如李畅等[44]发现淫羊藿多糖可能通过与难溶性黄酮组分形成胶束形式的复合物进而显著增加淫羊藿苷、宝藿苷Ⅰ的溶解度。结合“药辅合一”的中医药传统理念,开发多糖增溶辅料可推动中药制剂的改革与创新发展,并具有广阔前景[45]。天然矫味剂(蔗糖、甜菊素等)仅适用于小剂量中药的矫味,人工矫味剂(阿斯巴甜、纽甜等)会引发人体肠道菌群的紊乱,在一项研究中发现两亲性嵌段共聚物可作为中药液体制剂的新型苦味掩蔽剂,并且其口服后可在体内降解,对药物药效与体内吸收过程无显著影响,并且对人体肠道菌群无影响[46]。中药汤剂是中医临床最传统的口服剂型,其具有易吸收、起效快、疗效好的特点,而由于中药汤剂口味苦涩,存在顺应性差的问题,困扰了中药汤剂在儿童人群中的发展。陈少芳等提出新构想,以矫味剂、苦味阻滞剂的芳香剂等科学配比组合,创新性的提出制备小袋包装的“中药伴侣”,以便解决中药汤剂味苦、顺应性差的问题[47]。在我国大力推进儿童用药的新形势下,聚焦新型儿童药物辅料研发,为儿童药物合理发展奠定坚实基础。
5.3 聚焦儿童药物辅料安全标准建设
为保证药物辅料的安全性和规范性,在加工生产应遵循统一标准,在未来的行业中,出台儿科药物辅料质量标准相关政策是发展的前提。同时还要加强儿科中药制剂中辅料的质量检测,王亚琼等[48]建立了 HPLC-CAD 测定中成药中甜味剂及其蜂蜜类辅料的质量评价,对小儿咳喘灵口服液及颗粒剂中甜味剂的含有量进行测定,对其中矫味剂的使用标准、辅料质量等进行检测;张楠等[49]建立HPLC 波长切换联合梯度洗脱(HPLC-DVD)同时测定茵栀黄口服液中 14 种活性成分和辅料成分苯甲酸的含量。除建立质量检测方法外,还可引入“多维结构过程动态质量控制技术体系”思想[50],将质控检测贯穿药物辅料加工生产的每一环节中,为辅料用量的合理性、安全性提供保障。
6儿童制剂辅料未来发展新趋势
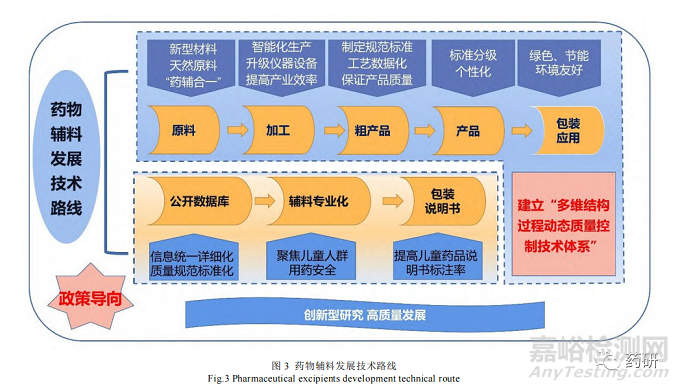
在国家鼓励儿童药品规范化、创新型发展的背景下,药物辅料将实现从低成本、低标准向高质量、高稳定性的跨越式发展,见图 3。转换原有药物辅料品种加工的低级模式,摒弃“重原料药,轻辅料”的思想,可通过模仿中药饮片智能化生产开发路线[51]:①将药物辅料加工工艺数据化,规范其工艺过程,保证药物辅料用于儿童药物时质量可控、安全可溯。②做好同一辅料类别中不同辅料品种的个性化质量标准建立工作,保证不同品种的辅料所制定的质量标准更具专属性、科学性、合理性。③建立药物辅料规格分级标准,以满足不同药品中使用的辅料的作用,尤其是在不同年龄段儿童的药品中细化辅料添加标准等级,保证儿童用药安全,同时也为医生科学用药提供依据。
已有研究人员对儿童使用药物中可能涉及的辅料及其已知的安全性问题,回顾国内外儿童用药辅料使用现状等进行了总结[25],但由于相关研究较分散,不利于儿童辅料未来的研究发展,可仿照STEP 数据库,纳入药物辅料体内动物实验、体外实验、人体安全性和毒性研究以及流行病学数据的实验细节和结果,以及药物监管信息和毒理学审查,副作用、给药年龄、研究类型和/或给药途径、用量等。同时还应该注意结合我国传统用药特色,包括传统中药制剂用于儿童治疗时选用的辅料,例如丸剂中的粘合剂、润湿剂;“药辅合一”思想的应用,以及药物与辅料间的配伍、相互作用等特点,建立具有中国传统特色的儿童药物辅料数据库[8-9]。
我国进入全面建成小康社会决胜阶段,加快推进健康中国建设,离不开药物创新研究及辅料高质量发展,同时要坚持绿色发展理念,对发展规律做出科学反应,可通过选用“绿色辅料”、创新工艺以缩减原料用量、积极寻找易消耗原料的替代产品、坚持可持续发展,使用环保材料、开发新型环保设备以提高生产效率等方法,促进制药行业创新驱动转型顺利进行。

来源:中国中药杂志