您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2022-06-29 11:10
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
今日头条
国内药讯
1.纳武利尤单抗获批两项食管癌适应症。百时美施贵宝PD-1纳武利尤单抗(欧狄沃)获NMPA批准新增两项食管癌适应症,联合氟嘧啶类和含铂化疗一线治疗晚期或转移性食管鳞癌患者,以及用于经新辅助放化疗(CRT)及完全手术切除后仍有病理学残留的食管癌或胃食管连接部癌患者的辅助治疗。此次获批,标志着纳武利尤单抗及其联合化疗方案成为中国首个同时覆盖食管癌辅助治疗与晚期一线治疗的PD-1/PD-L1抑制剂;以及首个覆盖上消化道肿瘤一线治疗的PD-1/PD-L1抑制。
2.海创德恩鲁胺前列腺癌Ⅲ期临床积极。海创药业1类新药德恩鲁胺(HC-1119)用于治疗转移性去势抵抗性前列腺癌(mCRPC)的III期临床(HC-1119-04)达到主要研究终点。与安慰剂相比,HC-1119治疗组患者的影像学无进展生存期(rPFS)的改善具有显著统计学意义,显著降低患者的疾病进展风险;总生存(OS)数据尚不成熟,但观察到临床获益趋势。该公司计划近期向NMPA递交上市前的沟通交流申请。
3.和铂B7H4/4-1BB双抗获FDA临床许可。和铂医药自主研发的双抗药物HBM7008获FDA临床试验默示许可。HBM7008是一款靶向B7H4和4-1BB的双特异性抗体,由于其高度依赖以肿瘤相关抗原为介导,与T细胞活化进行交叉链接,因此在T细胞共刺激及抑制肿瘤生长方面具有显著效果,有望在PD-L1阴性或对PD-1/PD-L1治疗产生耐药的患者中产生更好的疗效。目前HBM7008已获NMPA批准开展临床试验,并正在澳大利亚开展Ⅰ期临床。
4.海昶mRNA新冠疫苗在美报IND。浙江海昶生物自主研发的新冠mRNA疫苗HC009的临床试验申请获FDA受理,拟用于前期已接种初始序列新冠疫苗的人群加强接种,以预防包括奥米克戎在内的多种新冠变异株感染。目前,该公司在国内也正在布局针对空白人群的临床试验,并计划在验证HC009安全性、耐受性以及免疫原性(体液免疫+细胞免疫)之后,以无缝衔接、适应性设计的方式迅速推进国际多中心临床试验以加速审批和商业化。
5.华药康明溶瘤痘苗病毒报IND。CDE受理深圳华药康明生物自主研发的KM1溶瘤痘苗病毒注射液的临床试验申请(CXSL2200292)。KM1溶瘤痘苗病毒注射液是华药康明第一个痘苗病毒产品,目前已完成病毒设计与构建、细胞实验、动物实验和部分临床前研究。目前尚未有资料披露KM1溶瘤痘苗病毒注射液针对何种适应症。该公司另一主打产品溶瘤腺病毒KMAd1预计2023年第二季度申报IND。
国际药讯
1.第一三共HER2-ADC在日本报新适应症。第一三共重磅HER2-ADC新药Enhertu在日本递交了新适应症上市申请,用于HER2低表达乳腺癌的治疗。在关键III期DESTINY-Breast04试验中,Enhertu与化疗相比,将HR阳性、HER2低表达转移性乳腺癌患者的疾病进展或死亡风险降低49%(HR=0.51,p<0.001);Enhertu组中位PFS为10.1个月(vs5.4个月),中位OS为23.4个月(vs16.8个月)。药物的安全性与之前的临床试验一致。
2.抗精神病药物治疗AD激越将报sNDA。Otsuka公司与灵北联合开发的非典型抗精神病药物brexpiprazole在治疗阿尔茨海默病患者激越的Ⅲ期临床达到主要终点指标。与安慰剂组相比,brexpiprazole治疗组12周后评估激越症状的CMAI评分的改善具有统计学显著性(p=0.0026);评估患者疾病严重程度的CGI-S评分也具有显著改善(p=0.0055);brexpiprazole总体耐受性良好。预计今年向FDA递交补充新药申请(sNDA)。
3.心源性细胞疗法DMD临床长期疗效积极。Capricor公司基于心脏来源细胞(CDCs)的同种异体细胞疗法CAP-1002,在治疗晚期杜氏肌营养不良症(DMD)的Ⅱ期临床HOPE-2扩展研究结果积极。OLE数据显示,接受CAP-1002治疗的患者与在原先试验接受安慰剂治疗的患者相比,患者测试上肢功能的指标(PUL v2.0)获得统计上有显著的进步。CAP-1002的安全性与耐受性与之前的试验结果一致。此前FDA已授予CAP-1002再生医学先进疗法认定与孤儿药资格。
4.FGFR2靶向新药胆管癌早期临床积极。Relay公司口服小分子FGFR2抑制剂RLY-4008在治疗胆管癌(CCA)的Ⅰ期临床中获积极结果。中期结果显示,RLY-4008在带有FGFR2基因融合的CCA患者中达到确认部分缓解的患者比例为62%(8/13),包含4例以每天70毫克剂量治疗的病患。药物的安全性结果与之前结果一致。Relay已与FDA达成下一阶段临床试验设计方面的共识,这一试验有望支持RLY-4008的加速批准。
5.益普生收购表观遗传学公司Epizyme。益普生拟斥资约2.47亿美元收购Epizyme公司,并获得该公司的抗肿瘤新药Tazverik(tazemetostat)、在研口服SETD2抑制剂EZM0414和靶向表观遗传学靶点的一系列临床前项目。Tazemetostat是FDA批准的首款EZH2抑制剂,用于治疗携带EZH2突变的复发或难治性滤泡性淋巴瘤患者和软组织肉瘤患者。EZM0414目前正在Ⅰ期临床中评估用于治疗复发或难治性多发性骨髓瘤和弥漫性大B细胞淋巴瘤的潜力。
6.安斯泰来庞贝病基因疗法Ⅰ/Ⅱ期研究暂停。FDA日前叫停了安斯泰来(Astellas)腺相关病毒基因疗法AT845治疗晚发型庞贝病(LOPD)的Ⅰ/Ⅱ期FORTIS试验。该项临床中有1例受试者发生1级的严重不良事件 (SAE) 。目前,安斯泰来正在与现场调查员合作,密切关注患者的临床过程,并将继续收集和审查所有相关数据。AT845是安斯泰来以30亿美元收购Audentes公司所获得的其中一款基因疗法。
医药热点
1.湖南:103家核酸检测机构被责令整改。为进一步加强新冠核酸检测实验室质量控制,确保检测结果准确可靠、报告及时,湖南省按照国务院联防联控机制《关于进一步强化新冠病毒核酸检测质量监管的通知》精神,于2022年6月6日-6月15日期间对全省657家开展核酸检测的医疗卫生机构进行集中排查整顿。其中排查结果合格547家,责令整改103家,暂停业务资质4家,未开展业务3家。
2.四部门部署新时代中医药人才工作。国家中医药管理局、教育部、人力资源社会保障部、国家卫健委联合印发《关于加强新时代中医药人才工作的意见》,聚焦人才培养、使用、评价、激励等体制机制改革提出相关政策措施。力争到2025年,实现二级以上公立中医医院中医医师配置不低于本机构医师总数的60%,全部社区卫生服务中心和乡镇卫生院设置中医馆、配备中医医师。这也是首个多部门共同出台的系统部署中医药人才工作的政策性文件。
3.北京金准医学检验实验室4名犯罪嫌疑人被批捕。据“北京检察”微博消息,近日,北京市公安局海淀分局以北京金准医学检验实验室有限公司王某某、夏某某等4名犯罪嫌疑人涉嫌妨害传染病防治罪,提请北京市海淀区人民检察院批准逮捕。检察机关经审查,于2022年6月28日,依法以涉嫌妨害传染病防治罪对王某某、夏某某等4人作出批准逮捕决定。
4.最新版新冠肺炎防控方案发布。《新型冠状病毒肺炎防控方案(第九版)》28日正式公布,方案主要做出以下四方面调整:一是优化调整风险人员的隔离管理期限和方式;二是统一封管控区和中高风险区划定标准;三是完善疫情监测要求;四是优化区域核酸检测策略。其中,密切接触者、入境人员隔离管控时间从“14天集中隔离医学观察+7天居家健康监测”调整为“7天集中隔离医学观察+3天居家健康监测”;密接的密接管控措施从“7天集中隔离医学观察”调整为“7天居家隔离医学观察”。
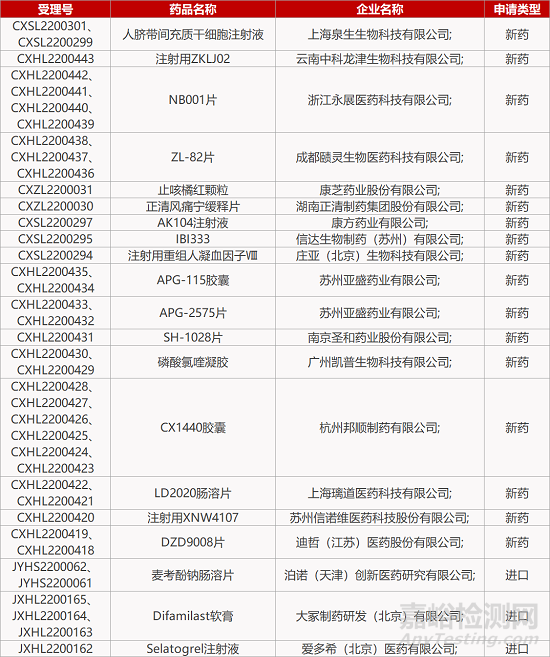
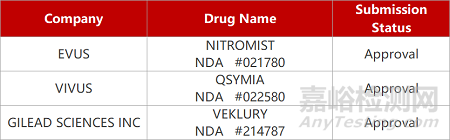
评审动态

来源:药研发


