您当前的位置:检测资讯 > 科研开发
嘉峪检测网 2020-03-06 09:41
更多医药技术资讯,请点击医药专栏:http://drug.anytesting.com/ 欢迎关注文末微信公众号:药研检测drugtest
「本文共:15条资讯,阅读时长约:3分钟 」
世界首项体内CRISPR基因编辑临床试验首例患者给药。由著名学者张锋博士创建的Editas Medicine公司与艾尔建联合宣布,评估在研CRISPR基因编辑疗法AGN-151587(EDIT-101)用于Leber先天性黑朦10(LCA10)患者安全性与疗效的Ⅰ/Ⅱ期临床试验Brilliance已完成首例患者给药。AGN-151587是世界首款在患者体内给药的CRISPR基因编辑疗法。该研究将入组18例患者,他们的一只眼睛将接受一剂AGN-151587的视网膜下注射。入组患者可能被分为5个队列,接受3种不同剂量的基因编辑疗法。
1.两家企业的右佐匹克隆片通过一致性评价。上海上药中西制药和康弘药业两家企业的仿制药右佐匹克隆片通过一致性评价。右佐匹克隆片是新一代非苯二氮卓类镇静催眠药,临床上用于失眠的一线治疗。右佐匹克隆属于国家医保目录药品。根据 IQVIA CHPA数据,右佐匹克隆2018年度国内样本医院用药销售额为2.09亿人民币,较2017年同期增加29.5%。
2.石药欧意利伐沙班片通过一致性评价。3月5日,石药欧意按新4类申报的利伐沙班片获得国家药监局批准,视同通过一致性评价,为继正大天晴之后国内第2家该品种通过一致性评价的企业。利伐沙班是一种新型口服抗凝药,广泛用于静脉血栓栓塞性疾病的预防与治疗,以及非瓣膜性房颤的卒中预防。该药原研药由拜耳/强生联合开发(商品名为Xarelto ),已于2009年3月获批进口中国(商品名为拜瑞妥)。2019年,利伐沙班全球销售额超过69亿美元。
3.药友制药度洛西汀拟纳入优先审评。药友制药盐酸度洛西汀肠溶胶囊的上市申请(20mg、30mg、60mg)拟被CDE纳入优先审评公示名单。度洛西汀为抗抑郁药,其原研企业为礼来,2019年全球销售额为7.25亿美元。目前国内该品种获批的厂家除原研厂家礼来外,还有恩华药业和上药中西制药。米内网数据显示,2018年中国公立医疗机构终端度洛西汀销售额为9.33亿元,同比增长23.38%。礼来占据54.2%的市场份额。
4.挚盟医药乙肝新药美国Ⅰ期临床首次人体给药。挚盟医药自主研发的用于治疗慢性乙型肝炎的新一代病毒核衣壳抑制剂ZM-H1505R在美国进入首次人体试验并完成第一个剂量组给药。该项Ⅰ期研究(ZM-H1505R-101) 在健康受试者中评估ZM-H1505R的安全性、耐受性,以及药代动力学,全部结果预计将在第三季度获得。挚盟医药计划今年下半年在中国启动该药物在乙型肝炎病毒感染患者中的安全性和初步药效学临床研究。
5.和黄医药2019年业绩报告发布。和黄医药公布2019年业绩报告,公司全年收入2.049亿美元,同比下降4.3%;净亏损1.06亿美元;研发费用1.38亿美元,同比下降3%。报告显示,其重磅结直肠癌治疗药物呋喹替尼2019年销售额为1760万美元,但Q4仅收入50万美元。2019年约有3000例患者接受了呋喹替尼的治疗。
1.罗氏肝癌早期诊断评分检测系统获FDA突破性认定。FDA授予罗氏的Elecsys系列GALAD评分检测系统突破性医疗器械认定,以支持肝细胞癌(HCC)患者的早期诊断。Elecsys GALAD检测的算法将患者的性别,年龄,以及AFP,AFP-L3(AFP的一种亚型),des-γ-羧基凝血酶原(PIVKA-II)的生物标志物水平结合在一起,帮助患者尽早诊断肝细胞癌。它是基于血液中的生物标记物对患者进行诊断,对患者的侵入性非常小。
2.强生S1P1调节剂ponesimod欧洲申请上市。强生旗下杨森宣布,已向欧洲药品管理局提交了一份营销授权申请,寻求批准其选择性鞘氨醇-1-磷酸受体1(S1P1)调节剂ponesimod用于复发型多发性硬化症(RMS)成人患者的治疗。在一项评估ponesimod与Aubagio(奥巴捷,teriflunomide,特立氟胺)治疗RMS患者的III期OPTIMUM研究(NCT02425644)中,与Aubagio治疗组相比,ponesimod治疗组年复发率(ARR)在统计学上显著降低30.5%(ARR:0.202 vs 0.290,p=0.0003);ponesimod在多个次要终点方面均显示出优越性。
3.Incyte公司JAK1/2抑制剂ruxolitinib乳膏剂III期临床成功。Incyte公司JAK1/JAK2抑制剂ruxolitinib乳膏剂在治疗青少年和成人(年龄≥12岁)特应性皮炎患者的关键性III期TRuE-AD1研究(NCT03745638)中获积极结果。与赋形剂组相比(15.1%),0.75%乳膏组和1.5%乳膏组分别有50.0%、53.8%的患者达到主要终点IGA-TS,p值均<0.0001。同时,0.75%乳膏组(56%)和1.5%乳膏组(62.1%)的患者实现主要的次要目标EASI75的比例更高(湿疹面积和严重程度指数评分较基线水平改善≥75%:赋形剂组为24.6%,p值均<0.0001)。今年1月,该药治疗特应性皮炎首个关键III期TRuE-AD2研究(NCT03745651)同样取得了积极结果。
4.Pliant Therapeutics公司完成C轮融资。专注于纤维化疾病领域的Pliant Therapeutics公司宣布完成由诺华领投的1亿美元C轮融资,以支持其候选药物PLN-74809、PLN-1474的临床开发,以及其他针对纤维化疾病的药物开发计划。该公司的主打候选药物PLN-74809是一种整合素αvβ1/αvβ6双重小分子选择性抑制剂,拟开发用于治疗特发性肺纤维化(IPF)和原发性硬化性胆管炎(PSC),目前处于Ⅱa期临床开发阶段。第二款候选药物PLN-1474是一款口服选择性αvβ1小分子抑制剂,是非酒精性脂肪性肝炎相关肝纤维化的潜在治疗药物。
5.拜耳2019财报发布。拜耳公布2019年财务业绩:集团全球总销售额达435亿欧元(约481.1亿美元),同比增长3.5%;净收入强劲增长141.4%,达到40.91亿欧元。报告期内,拜耳全球药品销售总额为184亿欧元(203.5亿美元),同比增长6%。其中,中国市场是业绩主要驱动因素之一,销售额同比增长25%(具体数额尚未公布)。中国市场的畅销药物主要有抗凝血剂拜瑞妥(利伐沙班片)和肝癌药物拜万戈 (瑞戈非尼)。首席财务官Wolfgang Nickl预测,2020年,中国市场将再次出现25%左右的增长。
1.欧美多国口罩短缺 价格离谱。据西班牙媒体报道,能够有效阻挡新冠病毒的FFP2型和FFP3型口罩自疫情爆发以来价格一直上涨。药房的FFP2型口罩单价已经达到300欧元,约合人民币2200元;60个一包的口罩在当地亚马逊网站上的价格已经达到960欧,约合人民币7400元。美国同样出现一罩难求的情况,目前亚马逊等线上各大电商平台已经断货,线下各家药店也断货,当地口罩价格高得离谱,5个149美元,按人民币算的话近209元/个,并且很多药店都缺货。
2.北京地坛医院首次证实:新冠病毒攻击中枢神经系统。据北京地坛医院官方微信消息,其收治的一例56岁新冠肺炎患者,通过基因测序证实脑脊液中存在SARS-CoV-2病毒,临床诊断为病毒性脑炎,患者中枢神经系统受病毒侵袭。目前来说,新冠肺炎患者可合并重度呼吸窘迫综合征(ARDS)、心肌损害、凝血功能异常、肾脏损伤、肝脏损害等多脏器损害,但尚未发现有中枢神经系统受累的报道,此病例报道在全球尚属首例。
3.武汉火速上线国家医保电子凭证。2月26日,武汉医保局为微医互联网总医院开通了医保支付,向武汉市10种门诊重症(慢性)疾病的参保人员,提供线上诊断、处方外配、在线支付和线下药品配送上门服务。为了解决使用线上医保支付功能时参保人员信息校验的快速办理,武汉市医保局在微医互联网总医院上火速上线了国家医保电子凭证,武汉市参保患者均可通过刷脸校验身份,领取自己的“电子身份”,不出门、不拿卡即可享受线上复诊购药、医保结算等便捷服务。
4.湖北:磷酸氯喹有15万人份,市场供应充分。3月4日下午,工信部消费品工业司副司长曹学军在国务院联防联控机制新闻发布会上表示, 从药品生产销售和库存监测情况看,《新型冠状病毒肺炎诊疗方案(试行第七版)》中阿尔法干扰素、激素类药物、检测试剂盒等重点品种目前能够满足湖北省一线需求。已运抵湖北的磷酸氯喹有15万人份,市场供应充分;阿比朵尔的生产也恢复正常,能够满足临床使用需要。下一步,将结合各省市使用需求做好药品对接、以及做好生产衔接。
【广生堂】公司乙肝治疗全球创新药乙肝表面抗原(HBsAg)抑制剂GST-HG131获得临床试验通知书,GST-HG131成为中国首个获批临床的乙肝表面抗原抑制剂。适应症为慢性乙型肝炎。根据世界卫生组织发布的《2017年全球肝炎报告》,全球范围内的乙肝病毒感染者约为2.57亿。据估算,我国乙肝病毒感染者约8,600万人,其中约有2,800万慢性乙肝患者,约占全球三分之一。迄今为止,全球范围内尚无批准任何药物或组合方案用于乙肝治愈。
【九强生物】第二期限制性股票激励计划首次授予的限制性股票第三个解除限售期的解除限售条件已成就,11名激励对象可解除限售的限制性股票数量为34.65万股,占公司股本总额的0.0690%;其中,实际解除限售并可上市流通股份数量为32.52万股(总股本0.0648%)。上市流通日为2020年3月10日。
【卫光生物】(1)公司2019年度实现营业收入8.21亿元(+19.41%),归母净利润1.71亿元(+9.39%),扣非归母净利润1.63亿元(+10.60)。(2)公司普通股利润分配预案为:每10股派发现金红利3.2元(含税),送红股5股(含税),不以公积金转增股本。
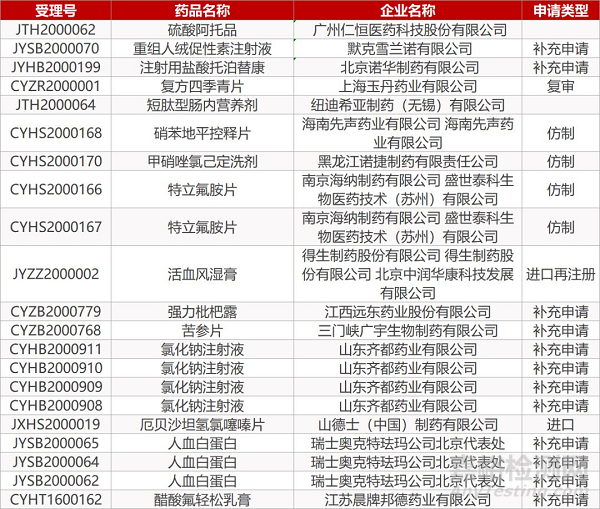
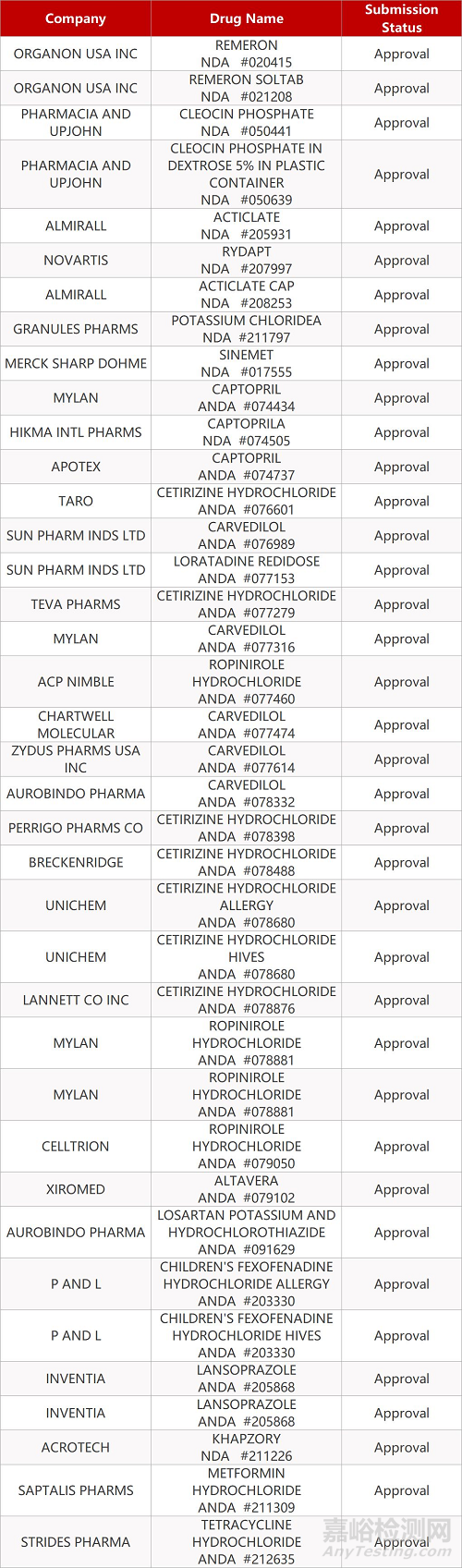

来源:药研发


